Szokásos aminosavak és fehérjeszintézis
Az élő szervezetek fehérjeszerkezeteiben leggyakrabban megjelenő aminosavakat közönséges vagy proteinogén aminosavaknak nevezzük. Bár a természetben több mint 500 féle aminosav ismert, csak húszat nevezünk közönségesnek. Velük együtt vannak olyan ritkábbak is, amelyeket alkalminak neveznek, amelyek általában a közönségesek anyagcseréjéből származnak, miután bekerültek a fehérje láncba. A kollagénben például a lizin és a prolin, két közönséges aminosav található hidroxilezett formában (hidroxiprolin és hidroxilizin).
A többi nem szokványos aminosav többsége elsősorban a fehérje jellegű enzimek és hormonok, vagy inkább peptidek összetételébe tartozik (ne feledje, hogy ahhoz, hogy ilyennek tekintsék, a fehérjének több mint 100 aminosavból kell állnia, míg egy oligo és egy polipeptid 2-9 és 10-100).
A 20 hétköznapi aminosav közül emlékszünk
Alanin, arginin, aszparagin, aszparaginsav, cisztein, glicin, glutaminsav, glutamin, hisztidin, izoleucin, leucin, lizin, metionin, fenilalanin, prolin, szerin, treonin, triptofán, tirozin, valin
Példák a nem szokványos aminosavakra:
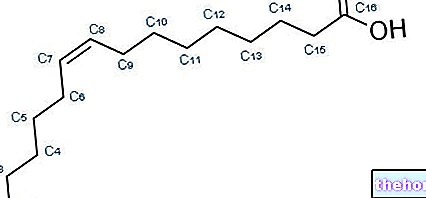
karnitin (részt vesz a hosszú láncú zsírsavak szállításában a mitokondriumban, ahol energiát termelnek);
ornitin, citrullin és homocisztein (részt vesz az aminosavak metabolizmusában - karbamid ciklus);
hidroxiprolin és hidroxilizin (a kollagén és egyes fehérjék összetételének részét képezik);
szarkozin (vagy metil -glicin).
Egyes aminosavaknak kereskedelmi vagy farmakológiai jelentősége is lehet.
- A nátrium -glutamátot az élelmiszeriparban ízfokozóként használják (lásd húsleveskockát).
- Az L-dihidroxi-fenilalanin (L-DOPA) a Parkinson-kór kezelésére használt gyógyszer.
- Az 5-hidroxi-triptofánt (5-HTP) a fenilketonuriával (örökletes anyagcsere-betegség, amely megakadályozza a fenilalanin, egy esszenciális aminosav használatát, bizonyos enzimatikus hiányok miatt; neurológiai tünetek kezelésére) alkalmazták; a fenilalanin felhalmozódása a szövetekben felelős a súlyos bőr- és neurológiai károsodásért).
A növények és baktériumok képesek bizonyos aminosavak előállítására, amelyek megtalálhatók a peptid antibiotikumokban, mint például a nizin és az alameticin.
Esszenciális aminosavak
A 20 közönséges aminosav közül néhányat esszenciálisnak neveznek, mivel a szervezet nem tudja szintetizálni más vegyületekből, hanem étellel kell bevenni.
Az emberek számára ezek fenilalanin, leucin, izoleucin, lizin, metionin, treonin, triptofán, valin, gyermekeknél pedig hisztidin és arginin.
Szokásos aminosavak, kémiai jellemzők

Az R gyök (nem túl hosszú láncot alkotó atomcsoport) kémiai jellemzői alapján az aminosavak különböző kategóriákba sorolhatók.
Apoláris R aminosavak (nem képesek hidrogénkötéseket kialakítani):
alifás lánccal: alanin, leucin, izoleucin, valin, prolin
aromás lánccal: fenilalanin, triptofán
kénatomot tartalmazó lánccal: metionin
Poláris R aminosavak:
OH csoporttal: szerin, treonin, tirozin
SH csoporttal: cisztein
CO-NH2 csoporttal: aszparagin, glutamin
H-val: glicin (az egyetlen nem királis aminosav)
Bázikus R aminosavak:
lizin, arginin, hisztidin
R savval rendelkező aminosavak:
glutaminsav, aszparaginsav