kalcium és szervetlen savak, például salétromsav, sósav vagy kénsav.
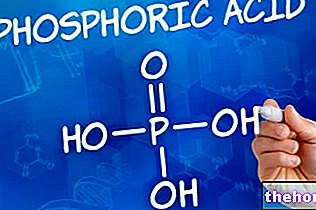
Ca3 (PO4) 2 + 3 H2SO4 → 3 CaSO4 + 2 H3PO4
A termikus eljárás viszont magában foglalja az elemi foszforból kiindulva foszfor -anhidrid előállítását. A keletkezés után az anhidridet addig kell hidratálni, amíg ortofoszforsavat nem kapunk, amint azt a következő reakció szemlélteti:
P2O5 + 3 H2O → 2 H3PO4
Ez utóbbi eljárás általában tisztább ortofoszforsavat eredményez, mint a nedves eljárás.
környezeti szempontból fehér szilárd anyagnak tűnik, amely körülbelül 42 ° C hőmérsékleten olvad.
A foszforsavat azonban általában tömény 85% -os vizes oldat formájában forgalmazzák. Színtelen, szagtalan és nem illékony oldat, de maró hatású és meglehetősen sűrű, szinte "szirupos" állagú.
Amellett, hogy az ortofoszforsav vízben oldódik, etanolban is oldódik, nem robbanásveszélyes és nem gyúlékony, de a bőrre és a nyálkahártyákra gyakorolt maró hatása miatt óvatosan kell kezelni.
annak érdekében, hogy elősegítsék a cementáló anyagok tapadását kapszulákhoz, hidakhoz, furnérokhoz, tömésekhez stb. Ebben az összefüggésben az ortofoszforsavat általában 37% -os oldatokban használják.