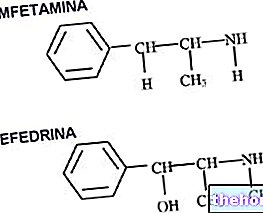
Hatóanyagok: Podofillotoxin
Condyline 0,5% -os bőroldat
Indikációk Miért használják a Condyline -t? Mire való?
A Condyline hatóanyaga a podophyllotoxin, egy növényből származó kivonat, amely az "antivirális" gyógyszerek csoportjába tartozik.
A Condyline egy helyi gyógyszer, amelyet bizonyos típusú szemölcsök kezelésére írnak fel, amelyek a nemi szervek külső bőrén képződnek (külső éles szemölcsök).
Beszéljen orvosával, ha a tervezett kezelési időszak után nem érzi magát jobban vagy rosszabbul.
Ellenjavallatok, amikor a Condyline -t nem szabad használni
Ne használja a Condyline -t
- ha allergiás a podofillotoxinra vagy a gyógyszer (6. pontban felsorolt) egyéb összetevőjére
- gyermekeknél
- ha terhes (lásd a "Terhesség és szoptatás" részt)
- ha szoptat (lásd a "Terhesség és szoptatás" részt)
- ha más, podofillint tartalmazó gyógyszereket szed.
Használati óvintézkedések Mit kell tudnia a Condyline szedése előtt?
A Condyline alkalmazása előtt beszéljen kezelőorvosával vagy gyógyszerészével.
- Kerülje a Condyline oldat érintkezését a nyálkahártyával vagy az egészséges bőrrel a szemölcsök közelében vagy alján, mivel ez helyi irritációt és / vagy a nyálkahártya vagy az egészséges bőr károsodását okozhatja. Annak elkerülése érdekében, hogy a kezelés megkezdése előtt az egészséges terület véletlenül ne érintkezzen a Condyline oldattal, megvédheti az egészséges területet semleges kenőcs vagy krém alkalmazásával, vazelin vagy cink -oxid alapján.
- Kerülje a gyógyszer szembe jutását, mert súlyos irritációt okozhat. Ha ez véletlenül történik, azonnal öblítse ki a szemét vízzel hosszú ideig, és forduljon orvosához.
- Kerülje a gyógyszer nagy területeken történő alkalmazását, mivel ez mellékhatásokat okozhat a test különböző szerveiben.
- Ha Ön nő, és ennek a gyógyszernek a használata nehéz, mivel a seb nem elérhető öngyógyításra, forduljon orvosához a Condyline alkalmazásához.
- Ha ennek a gyógyszernek a hatása nem nyilvánvaló az előírt kezelési időszak után, orvosa alternatív gyógymódokat mérlegel.
Gyermekek
A Condyline nem alkalmazható gyermekeknél.
Kölcsönhatások Mely gyógyszerek vagy élelmiszerek módosíthatják a Condyline hatását
Egyéb gyógyszerek és a Condyline
Feltétlenül tájékoztassa kezelőorvosát vagy gyógyszerészét a jelenleg vagy nemrégiben szedett, valamint szedni tervezett egyéb gyógyszereiről.Különösen tájékoztassa kezelőorvosát, ha bármilyen más, podofillint tartalmazó gyógyszert szed, mivel ebben az esetben nem használhatja ezt a gyógyszert (lásd "Ne alkalmazza a Condyline -t" című részt).
Figyelmeztetések Fontos tudni, hogy:
Terhesség és szoptatás
Ne használja a Condyline-t, ha terhes, ha úgy gondolja, hogy terhes, vagy ha szoptat.
A készítmény hatásai a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre
Ez a gyógyszer nem befolyásolja a gépjárművezetéshez és gépek kezeléséhez szükséges képességeket.
Adagolás, az alkalmazás módja és ideje A Condyline használata: Adagolás
Ezt a gyógyszert mindig pontosan az orvos vagy a gyógyszerész által elmondottaknak megfelelően alkalmazza. Ha kétségei vannak, forduljon orvosához vagy gyógyszerészéhez.
Felnőttek
Az ajánlott adag naponta kétszer egy alkalmazás, reggel és este.
A kezelés időtartama
Alkalmazza ezt a gyógyszert reggel és este, 3 egymást követő napon. A kezelési séma hetente legfeljebb 5 egymást követő hétig megismételhető, így az egyik hét és a másik között 4 napos intervallumot kell hagyni kezelés nélkül A terméket rövid ideig és orvosi felügyelet mellett kell használni.
Utasítások a helyes használathoz
- A palack "gyermekbiztos" biztonsági zárral rendelkezik. A palack kinyitásához nyomja meg a kupakot és csavarja le egyidejűleg a nyíllal jelzett irányba (az ábrán látható módon).
- Vigye fel az oldatot a kezelendő bőrfelületre a csomagolásban található egyik applikátor segítségével, elkerülve az egészséges bőrrel való érintkezést (lásd a "Figyelmeztetések és óvintézkedések" bekezdést).
- Az alkalmazás után hagyja az oldatot levegőn megszáradni, nehogy az oldat érintkezzen egészséges területekkel, különösen akkor, ha a szemölcsök a fitymán helyezkednek el (férfiaknál a pénisz hegyét borító bőrredő).
- Az alkalmazás után dobja el a használt applikátort, és alaposan mosson kezet.
- Használat után csukja le a kupakot.A palack zárt gyermekbiztos, ha kattanást hall, amikor le nem csavarja a kupakot.
Túladagolás Mi a teendő, ha túl sok Condyline -t vett be?
Ha az előírtnál több Condyline -t alkalmazott
Nem jelentettek mellékhatásokat a túl sok Condyline alkalmazásakor. Ha azonban véletlenül az előírtnál több Condyline -t alkalmazott, és bármilyen mellékhatást észlel, azonnal forduljon orvosához vagy a legközelebbi kórházhoz. Orvosa ezt fogja vállalni.
Ha elfelejtette alkalmazni a Condyline -t
Ne használjon kétszeres adagot a kihagyott adag pótlására.
Ha abbahagyja a Condyline használatát
Ha bármilyen további kérdése van a gyógyszer alkalmazásával kapcsolatban, kérdezze meg kezelőorvosát vagy gyógyszerészét.
Mellékhatások Mik a Condyline mellékhatásai?
Mint minden gyógyszer, így ez a gyógyszer is okozhat mellékhatásokat, amelyek azonban nem mindenkinél jelentkeznek.
A helyi mellékhatások többnyire a kezelés második vagy harmadik napján jelentkeznek, amikor a szemölcshalál kezdődik. Általában a mellékhatások enyheek és jól tolerálhatók.
Az alábbi mellékhatások gyakorisága nem ismert.
A bőrt és a nyálkahártyákat érintő nemkívánatos hatások
- erythema (bőrirritáció) enyhe fájdalommal és / vagy felületes bőrelváltozásokkal a kezelt területen. Ebben az esetben a Condyline alkalmazása fájdalmas lehet
- ödéma (duzzanat) és balanoposthitis (a pénisz végtagjának fertőzése). Ez a hatás a fityma üregében lévő nagy szemölcsök esetén jelentkezik.
A termék helytelen alkalmazása esetén a következők is előfordulhatnak:
- gyomor és bél rendellenességek
- leukopenia (csökkent fehérvérsejtszám a vérben)
- thrombocytopenia (a vérlemezkék számának csökkenése a vérben)
- változások a májműködésben
- a veseműködés változásai
- perifériás neuropátiák (perifériás idegrendszeri betegségek)
- általában szerény érzékszervi zavarok (enyhe mentális zavartság), ezek a hatások előrehaladhatnak és bonyolulttá válhatnak a központi idegrendszert érintő komolyabb képekkel.
Mellékhatások bejelentése
Ha Önnél bármilyen mellékhatás jelentkezik, tájékoztassa erről kezelőorvosát, beleértve a betegtájékoztatóban fel nem sorolt bármilyen lehetséges mellékhatást is. A mellékhatásokat közvetlenül a hatóság részére is bejelentheti a www.agenziafarmaco.gov.it/it/responsabili címen. A mellékhatások bejelentésével Ön is hozzájárulhat ahhoz, hogy minél több információ álljon rendelkezésre a gyógyszer biztonságosságáról.
Lejárat és megőrzés
A gyógyszer gyermekektől elzárva tartandó!
25 ° C alatt tárolandó.
A dobozon feltüntetett lejárati idő (EXP) után ne alkalmazza ezt a gyógyszert. A lejárati idő az adott hónap utolsó napjára vonatkozik.
Semmilyen gyógyszert ne dobjon a szennyvízbe vagy a háztartási hulladékba. Kérdezze meg gyógyszerészét, hogy mit tegyen a már nem használt gyógyszereivel. Ez elősegíti a környezet védelmét.
Összetétel és gyógyszerforma
A csomagolás tartalma és egyéb információk
- a hatóanyag: podofillotoxin (1 ml oldat 5 mg podofillotoxint tartalmaz)
- egyéb összetevők: tejsav, nátrium -laktát, vízmentes etanol, víz.
A Condyline külleme és a csomagolás leírása
A Condyline oldatot helyi használatra készítik, 3,5 ml oldatot tartalmazó palackba csomagolva.
A doboz két, a terápiához szükséges 15 applikátor csomagját tartalmazza.
Forrás betegtájékoztató: AIFA (Olasz Gyógyszerügynökség). A tartalom 2016 januárjában jelent meg. A jelenlévő információk nem feltétlenül naprakészek.
A legfrissebb verzióhoz való hozzáféréshez ajánlatos az AIFA (Olasz Gyógyszerügynökség) webhelyét elérni. Jogi nyilatkozat és hasznos információk.
01.0 A GYÓGYSZER MEGNEVEZÉSE
CONDYLINE® 0,5% BŐRMEGOLDÁS
02.0 MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL
1 ml tartalmaz: 5 mg podofillotoxint.
03.0 GYÓGYSZERFORMA
Bőroldat.
04.0 KLINIKAI INFORMÁCIÓK
04.1 Terápiás javallatok
A külső akuminált szemölcsök helyi kezelése.
04.2 Adagolás és alkalmazás
Vigye fel az oldatot a szemölcsökre a csomagban található egyik applikátor segítségével, elkerülve az egészséges bőrrel való érintkezést.
Az alkalmazást naponta kétszer, reggel és este, 3 egymást követő napon kell elvégezni.Ez a kezelési séma hetente, legfeljebb 5 egymást követő hétig megismételhető, így 4 napos kezelés nélküli szünetet kell hagyni az egyik hét között.
Az oldat felhordása után hagyja jól megszáradni a levegőben, nehogy elterjedjen a betegség által nem érintett területekre; különösen akkor, ha a szemölcsöket a fityma lokalizálja.
Az alkalmazás után dobja ki a használt applikátort, és alaposan mosson kezet.
04.3 Ellenjavallatok
Ismert túlérzékenység az összetevőkkel szemben.
A Condyline alkalmazása ellenjavallt gyermekeknél és nőknél terhesség és szoptatás alatt. Használata ellenjavallt podofillin alapú termékekkel együtt.
04.4 Különleges figyelmeztetések és a használathoz szükséges óvintézkedések
A terméket rövid ideig és orvosi felügyelet mellett kell használni.
A készítmény viszonylag nagy nyálkahártya -felületeken történő alkalmazása szisztémás reakciókat okozhat, ezért kerülni kell.
A Condyline nem érintkezhet a szemmel, mivel súlyos irritáló megnyilvánulásokat okozhat. Ha ez véletlenül történik, azonnal öblítse ki a szemét vízzel hosszú ideig, és forduljon orvosához.
Gyermekektől elzárva tartandó!
Azoknál a nőbetegeknél, akiknél a lézió nem elérhető öngyógyításra, a kezelést közvetlen orvosi felügyelet mellett kell végrehajtani.
A nyálkahártya vagy az egészséges bőr helyi irritáló megnyilvánulásai és / vagy fekélyei a szemölcsök közelében vagy az alján, amelyeket véletlenül a Condyline oldattal való érintkezés okoz, elkerülhetők az egészséges terület semleges kenőccsel vagy krémmel történő védelmével. , vazelin vagy cink -oxid alapú, amelyet a Condyline -kezelés előtt kell alkalmazni.
Ha a készítmény hatékonysága a tervezett kezelési időszak után nem nyilvánvaló, alternatív terápiákat kell mérlegelni.
04.5 Kölcsönhatások más gyógyszerekkel és más interakciók
Ne használja a Condyline -t a kezelés során podofillint tartalmazó termékekkel.
04.6 Terhesség és szoptatás
Ne használja a Condyline -t terhesség és szoptatás alatt.
04.7 Hatások a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre
A termék nem veszélyezteti a gépjárművezetéshez és gépek kezeléséhez szükséges képességeket.
04.8 Nemkívánatos hatások
A helyi másodlagos reakciók főként az optimális terápiás hatással együtt jelentkeznek, többnyire a kezelés második vagy harmadik napján, amikor a szemölcsök nekrózisa kezdődik. Ezek a másodlagos reakciók általában enyhén jelentkeznek, és a betegek jól tolerálják, ha az orvos figyelmezteti őket a kezelés megkezdése előtt Előrelátható, hogy a kezelt területen erythema jelentkezik enyhe érzékenységgel és / vagy a hám felületes fekélyesedésével, ezért a Condyline alkalmazása fájdalmas lehet.
Ödémát és balanoposthitis -t figyeltek meg néhány olyan betegnél, akiknél nagy szemölcsök voltak a fityma üregében.
A termék helytelen alkalmazása a szisztémás felszívódás megnyilvánulásaihoz vezethet, például gyomor -bélrendszeri rendellenességek, leukopenia, trombocitopénia, máj- vagy vesefunkciós elváltozások, perifériás neuropátiák, általában szerény érzékszervi zavarok (enyhe mentális zavartság), amelyek azonban előrehaladhatnak és súlyosbodhatnak befolyásolja a központi idegrendszert.
04.9 Túladagolás
A podofillotoxin túladagolásából származó nemkívánatos hatásokat nem jelentettek. Ilyen hatások nem várhatók a Condyline helyes használatával, tekintettel a készítmény nagy biztonsági tartalékára.
Ha azonban a túladagolás szisztémás hatása jelentkezik, a podophyllin túladagolása esetén előírtakhoz hasonló terápiás intézkedéseket kell végrehajtani, amelyek célja a tünetek (hányás és görcsök) szabályozása; a nyomást és a diurézist szoros megfigyelés alatt kell tartani, szem előtt tartva, hogy akut podofillin -mérgezés esetén a folyadék helyreállítása és a hemoperfúzió indokolt lehet.
05.0 FARMAKOLÓGIAI TULAJDONSÁGOK
05.1 Farmakodinámiás tulajdonságok
A Podophyllotoxin, a Condyline hatóanyaga kémiailag a lignánok csoportjába tartozik.
ATC kód: D06BB04.
Ez a podofillin fő terápiás összetevője, amelyből egy különleges extrakciós eljárással nyerik, amely biztosítja a termék nagyfokú tisztaságát és szabványosítását. A podofillotoxin kifejezett antimitotikus és citolitikus aktivitással rendelkezik, amely gyorsan kiváltja az akuminált szemölcsök nekrózisát. A podofillotoxin aktivitása gyorsabb és hatékonyabb, mint a podofilliné, nagyfokú tisztasága és szabványosítása miatt. Ez lehetővé teszi a megfelelő dózisok beadását alacsonyabb mellékhatások kockázatával, és lehetővé teszi a beteg otthoni kezelését magas gyógyulási arány mellett.
05,2 "Farmakokinetikai tulajdonságok
Akut toxicitás
Az akut toxicitási vizsgálatok kimutatták, hogy 25 mg / kg-nál kisebb podophyllotoxin egyszeri adagjának orális adagolása patkányokban és egerekben nem mérgező.
A podofillotoxin akut toxicitását számos állatfajban és különböző beadási módokon vizsgálták.
Az LD50 egerekben 40 mg / kg (szájon át), 19-33 mg / kg intravénásan, 31 mg / kg szubkután és 4,6 mg / kg intravénásan; patkányokban 14 mg / kg szubkután, 3 mg / kg intramuszkulárisan és 15 mg / kg intramuszkulárisan; nyulaknál 5 mg / kg intravénásan; kutyában szubkután 10-30 mg testtömegtől függően.
Akut toxicitási vizsgálatok a Condyline 24 órán át tartó hosszan tartó epikután alkalmazására (határvizsgálatok) 2 ml / testtömeg -kilogramm dózisban (ami 10 mg / kg podofillotoxinnak felel meg), egerek és patkányok borotvált hátán (az alábbiakban) elzáródás), kimutatták, hogy a termék nem mutat szisztémás toxicitást.
Szubakut vagy krónikus toxicitási vizsgálatok
Miután egereken, hetente kétszer, 74 héten keresztül, 2,5% -os podophyllotoxin polietilén -glikolban készített oldatát 2,5 cm2 -es dorzális területen epikután, hetente kétszer 74 héten keresztül alkalmazták, kiderült, hogy 29 hetes kezelés után a halálozások száma 0/ 25, 50 hét után 5/25 volt, 74 hét után pedig 12/25 -re emelkedett (48%).
Az alkalmazott dózis 50 mcl volt, ami körülbelül 1,25 mg -nak felel meg egérenként.
A 20 g -os testtömeget figyelembe véve a helyi dózis 62,5 mg / kg.
Emberben a Condyline 0,5% -át körülbelül 10-100 mcl dózisban alkalmazták, ami 0,0007-0,007 mg / kg-nak felel meg.
Mivel a Condyline helyi termék, a Magnusson-Klingman "maximalizálási tesztet" tengerimalacokon végezték el, 0,5% podofillotoxint propilénglikolban és 0,01-0,5% oldatokat használva az indukciós fázisban.
A 0,1% és 0,5% koncentrációjú provokációs teszt nem allergiás irritáló reakciót váltott ki.
Egyik kísérletben sem jelentkezett allergiás reakció.
A helyi irritáló hatást 0,01%, 0,05%, 0,1% és 0,5% podophyllotoxin 70% -os etanolban történő ismételt (napi 2 alkalommal, 10 napon át tartó) alkalmazása után nyulakon vizsgálták (szemben a csak 70% -os etanollal kezelt kontrollcsoporttal) ), mind a bőrredő vastagságának mérésével, mind pedig olyan paraméterek vizuális értékelésével, mint a bőrpír, a váladék és a kéreg jelenléte.
Az eredmények lineáris korrelációt mutattak a podofillotoxin koncentrációjának növekedése és a redő vastagságának növekedése között, valamint exponenciális összefüggést mutattak a gyógyszerkoncentráció növekedése és a bőrreakció között.
A podofillotoxin embriotoxikus, miközben nem mutat rákkeltő vagy mutagén hatást.
05.3 A preklinikai biztonságossági adatok
A jelzett podofillotoxinnal végzett farmakokinetikai vizsgálatokat egészséges és daganatot hordozó egereken végezték. 4 órás szubkután alkalmazás után a radioaktivitás nagy része egyenlően oszlott el a bél és a vizelet között, míg csak nyomok voltak a májban, az epehólyagban és a vesékben, valamint az agyban, a mellékvesekéregben és a herékben. A 180 -as szarkómát hordozó egerekben a radioaktivitás nagy része a vizeletben található.
Az utóbbi állatoknál a podofillotoxin eliminációja sokkal gyorsabb volt. A daganat nem tartalmazott jelentős mennyiségű radioaktivitást. A vizeletből visszanyert radioaktivitás szintje jóval alacsonyabb volt az Ehrlich -féle ascites -karcinómát hordozó egereknél. Minden állat esetében viszonylag magas koncentrációban kezelték radioaktivitást találtak az epében, amely a vese emunctoriummal együtt a podophyllotoxin és metabolitjai legfontosabb kiválasztási útjának tűnik.
A perkután felszívódási vizsgálatokban 0,5% -os podophyllotoxinnal kezelt betegeknél 0,01-0,05 ml dózisban 3 napon keresztül nem lehetett kimutatni a gyógyszert a szérumban az alkalmazás utáni ½-1 órában.
0,1 ml -es dózisok alkalmazásával (4 cm2 összterületű szemölcsökön) a podophyllotoxin szérumszintjét
0,15 ml -es dózis esetén a szérumszintek megközelítőleg megegyeztek, míg 5 betegnél 12 órával az alkalmazás után ≤ 1 ng / ml.
Azoknál a betegeknél, akiket 0,1-1,5 ml-rel kezeltek nagyon kiterjedt léziók esetén, a maximális szintek 1-12 óra elteltével 1-17 ng / ml voltak. Kimutatták azonban, hogy a klinikai gyakorlatban ritkán van szükség 0,1 ml -nél nagyobb oldatmennyiségre. Ha az alkalmazás után, naponta kétszer, 0,1 ml 0,5% -os oldat után viszonylag hosszú idő után felszabadulunk, az azt jelzi, hogy az elosztás kétkamrás modell szerint történik. Az elvégzett vizsgálatok alapján a szérum felezési ideje 1-től 1-ig extrapolálható 4½ óra A podofillotoxin felhalmozódását nem figyelték meg.
06.0 GYÓGYSZERÉSZETI INFORMÁCIÓK
06.1 Segédanyagok
Tejsav, nátrium -laktát, vízmentes etanol, víz.
06.2 Inkompatibilitás
Nem ismertek.
06.3 Érvényességi idő
3 év.
06.4 Különleges tárolási előírások
25 ° C alatt tárolandó
06.5 A közvetlen csomagolás jellege és a csomag tartalma
Kartondoboz 3,5 ml -es palackkal, biztonsági zárral.
06.6 Használati utasítás
Nem releváns.
07.0 FORGALOMBA HOZATALI ENGEDÉLY
Astellas Pharma S.p.A. - Via delle Industrie 1 - 20061 Carugate (Milánó)
08.0 A FORGALOMBA HOZATALI ENGEDÉLY SZÁMA
027136011
09.0 Az első forgalomba hozatali engedély kiadásának időpontja
Regisztráció 1990. május 2. - Az engedély megújítása 2010. június 1
10.0 A SZÖVEG FELÜLVIZSGÁLÁSÁNAK DÁTUMA
2011. szeptember