A glikogén egy α-glükóz makromolekula (körülbelül 400 millió dalton molekulatömegű), amelyben főként α-1,4 glikozid kötések és elágazások találhatók 1:10 arányban, az α-1,6 glikozidos kötések miatt.
A glikogén tartalék anyag, és folyamatosan lebomlik és felépül; a teljes test sejttömegében körülbelül 100 g glikogén található: legtöbbje a májban van, ahol mozog, és ezért más szervek tartalékaként használható (az izmokban lévő glikogén nem mobil).
A glikogén lebomlását és szintézisét katalizáló enzimek mind a citoplazmában vannak, ezért olyan szabályozási rendszerre van szükség, amely az egyik utat inaktívvá teszi, amikor a másik aktív: ha rendelkezésre áll glükóz, az utóbbit glikogénné alakítják (anabolizmus). tartalék, fordítva, ha c "szükséges a glükózhoz, akkor a glikogén lebomlik (katabolizmus).

Az enzim, amely főként a glikogén lebontásában vesz részt, az glikogén -foszforiláz; ez az enzim képes egy glikozidos α-1,4 kötést lehasítani, szervetlen ortofoszfátot használva lítikus szerként: a hasítás foszforolitikus úton történik, és glükóz-1-foszfátot kapunk.
Öt -hat egységnyi távolságra az elágazási ponttól a glikogén -foszforiláz enzim már nem képes hatni, ezért leválik a glikogénről, és helyébe egy deramifikáló enzim lép, transzferáz: ennek az enzimnek a katalitikus helyén c "egy" hisztidin, amely lehetővé teszi három szacharid egység átvitelét a legközelebbi glikozid láncba (a hisztidin megtámadja a glükózmolekula első szénét). Az imént említett enzim glikoziltranszferáz; ezen enzim hatásának végén csak egy glükóz egység marad az oldalláncban, az első szén a fő lánc glükóz hatodik szénéhez kötődik. Az oldallánc utolsó glükóz egysége felszabadul a "enzim α-1,6 glikozidáz (ez az enzim alkotja a deramifikáló enzim második részét); mivel a glikogén ágak 1:10 arányban vannak, a makromolekula teljes lebomlása után körülbelül 90% glükóz-1-foszfátot és körülbelül 10% -ot kapunk szőlőcukor.
A fent említett enzimek hatása lehetővé teszi egy oldallánc eltávolítását a glikogén molekulából; ezen enzimek aktivitása megismételhető mindaddig, amíg a lánc teljesen le nem bomlik.
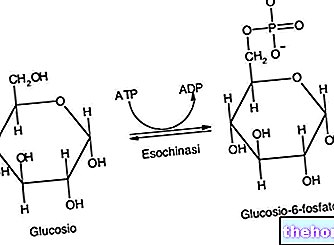
Tekintsünk egy hepatocitát; glükóz (a táplálékkal asszimilálódik), amikor a sejtbe kerül, glükóz-6-foszfáttá alakul, és így aktiválódik. Glükóz-6-foszfát, hatására foszfoglukomutáz, glükóz-1-foszfáttá alakul: ez utóbbi a bioszintézis nem közvetlen előfutára; a bioszintézis során a cukrok aktivált formáját használják, amelyet a difoszfáthoz kapcsolódó cukor képvisel: általában uridildifoszfát (UDP). majd átalakul UDP-glükózzá, ez a metabolit a hatása alatt glikogén szintáz amely képes az UDP-glükózt a növekvő glikogén nem redukáló végéhez kötni: glükózid egység hosszúkás glikogénjét és UDP-t kapunk.
A glikogén lebomlása azáltal történik glikogén -foszforiláz amely egy glükózmolekulát szabadít fel és glükóz 1-foszfáttá alakítja. Ezt követően a foszfoglukomutáz glükóz-1-foszfátot glükóz-6-foszfáttá alakítja.
A glikogént mindenekelőtt a májban és az izmokban szintetizálják: a szervezetben 1-1,2 hektogram glikogén található az izomtömegben.
A miocita glikogénje csak ennek a sejtnek jelent energiatartalékot, míg a májban található glikogén tartalék más szövetek számára is, azaz glükózként más sejtekhez is eljuttatható.
A glikogén lebomlásakor az izmokban kapott glükóz-6-foszfátot energiaigény esetén glikolízisre küldik; a májban a glükóz-6-foszfát a hatására glükózzá alakul glükóz-6-foszfát-foszfatáz (a hepatociták jellegzetes enzimje), és a véráramba kerül.
A glikogén-szintáz és a glikogén-foszforiláz egyaránt működnek a glikogén nem redukáló egységein, ezért hormonális jelnek kell lennie, amely az egyik útvonal aktiválását és a másik blokkolását parancsolja (vagy fordítva).
A laboratóriumban meg lehetett hosszabbítani a glikogénláncot a glikogén-foszforiláz kiaknázásával és a glükóz-1-foszfát nagyon magas koncentrációjú felhasználásával.
A sejtekben a glikogén -foszforiláz csak katalizálja a bomlási reakciót, mivel a metabolitok koncentrációja olyan, hogy jobbra tolja a következő reakció egyensúlyát (azaz a glikogén lebomlása felé):

Lássuk a glikogén -foszforiláz hatásmechanizmusát: az acetál -oxigén (amely hídként működik a glükóz -egységek között) kötődik a foszforil -hidrogénhez: reakcióközbenső képződik egy karbokációval (a glükózra, amely minden) végtagok), amelyekhez a foszforil (Pi) nagyon gyorsan kötődik.
A glikogén -foszforilázhoz kofaktorra van szükség, amely piridoxál -foszfát (ez a molekula a transzaminázok kofaktora is): részben protonált foszforilcsoportot tartalmaz (a piridoxál -foszfátot hidrofób környezet veszi körül, ami indokolja a hozzá kötött protonok jelenlétét). A foszforil (Pi) képes protont átvinni a glikogénbe, mert ez a foszforil újra megszerzi a protont a piridoxál -foszfát részben protonált foszforil -csoportjából. Nagyon kicsi annak a valószínűsége, hogy fiziológiai pH -n a foszforil elveszíti protonját és teljesen deprotonálódik.
Nézzük most, hogyan működik a foszfoglukomutáz. Ez az enzim a katalitikus helyen foszforilezett szerin maradékot mutat; a szerin foszforilt kap glükóz-1-foszfáttá (a hatodik pozícióban): glükóz 1,6-biszfoszfát keletkezik rövid ideig, majd a szerin újra foszforilálódik, az első pozícióban lévő foszforilcsoportot figyelembe véve. A foszfoglukóz-mutáz mindkét irányban működhet, azaz glükóz-1-foszfátot glükóz-6-foszfáttá alakíthat, vagy fordítva; ha glükóz-6-foszfát termelődik, akkor közvetlenül a glikolízisbe, az izmokba kerülhet, vagy a májban glükózzá alakítható.
Az enzim uridil -foszfoglukóz -transzferáz (vagy UDP -glükóz -pirofoszforiláz) katalizálja a glükóz 1-foszfát transzferreakciót az UTP-hez a foszforilhoz való kötődéssel.
Az imént leírt enzim egy pirofoszforiláz: ez a név annak a ténynek köszönhető, hogy az imént leírtal ellentétes reakció a pirofoszforiláció.
A leírás szerint előállított UDP glükóz egy monoszacharid egységgel képes meghosszabbítani a glikogénláncot.
Lehetőség van arra, hogy a reakciót az UDP glükóz képződése felé fejlesszük, ha eltávolítunk egy terméket, amely pirofoszfát; az enzimet pirofoszfatáz a pirofoszfátot két ortofoszfát -molekulává alakítja (anhidrid hidrolízise), és ezáltal olyan alacsonyan tartja a pirofoszfát koncentrációját, hogy az UDP -glükóz képződési folyamatát termodinamikailag előnyössé tegye.
Mint említettük, az UDP glükóz a glikogén szintáz hatásának köszönhetően meghosszabbíthatja a glikogénláncot.
A következmények (1:10 arányban) annak a ténynek köszönhetők, hogy amikor a glikogénlánc 20-25 egységből áll, akkor egy elágazó enzim (amelynek "katalitikus helyén" hisztidin van) beavatkozik, és képes egy sor 7-8 glikozidos egység tovább 5-6 egység után: így új elágazás jön létre.
Ideges eredetű okokból, vagy ha fizikai erőfeszítés miatt energiára van szükség, az adrenalin kiválasztódik a mellékvesékből.
Az adrenalin (és a noradrenalin) célsejtjei a máj, az izmok és a zsírszövetek sejtjei (utóbbiban a trigliceridek lebomlása és a zsírsavak keringése következik be: következésképpen a glükóz termelődik a mitokondriumok 6 -foszfátjában) glikolízisre kerül, míg az adipocitákban a glükóz-6-foszfát a glükóz-6-foszfát-foszfatáz enzim hatására glükózzá alakul, és a szövetekbe exportálódik).
Lássuk, most az adrenalin hatásmódjai. Az adrenalin a sejtmembránon elhelyezkedő receptorokhoz (myocyták és hepatociták) kötődik, és ez határozza meg a jel transzlációját kívülről a sejt belsejébe. A protein kináz aktiválódik, amely egyidejűleg hat a glikogén szintézisét és lebontását szabályozó rendszerekre:
A glikogén szintáz két formában létezik: defoszforilezett (aktív) és foszforilált (inaktív) formában; A protein -kináz foszforilálja a glikogén szintetázt és blokkolja annak hatását.
A glikogén -foszforiláz két formában létezhet: aktív formában, amelyben foszforilált szerin van jelen, és inaktív formában, amelyben a szerin defoszforilálódik. A glikogén -foszforilázt az enzim aktiválhatja glikogén -foszforiláz -kináz. A glikogén -foszforiláz -kináz aktív, ha foszforilezett, és inaktív, ha defoszforilezett; a protein -kináz szubsztrátja a glikogén -foszforiláz -kináz, azaz képes foszforilálni (és ezért aktiválni) az utóbbit, ami viszont aktiválja a glikogén -foszforilázt.
Miután az adrenalin jel véget ért, a sejtre gyakorolt hatásának is véget kell vetni: a foszfatáz enzimek ezután beavatkoznak a fehérjefajokba.