Hatóanyagok: Fentanyl
Abstral 100 mikrogramm nyelv alatti tabletta
Abstral 200 mikrogramm nyelv alatti tabletta
Abstral 300 mikrogramm nyelv alatti tabletta
Abstral 400 mikrogramm nyelv alatti tabletta
Abstral 600 mikrogramm nyelv alatti tabletta
Abstral 800 mikrogramm nyelv alatti tabletta
Miért alkalmazzák az Abstral -t? Mire való?
Az Abstral azoknak a felnőtteknek való kezelés, akiknek tartós fájdalomcsillapító gyógyszereket (opioidokat) kell rendszeresen szedniük tartós rákos fájdalom esetén, de akik áttöréses fájdalmat igényelnek. Ha kétségei vannak, forduljon orvosához.
Az áttöréses fájdalom olyan fájdalom, amely hirtelen jelentkezik, még akkor is, ha már bevette a szokásos opioid fájdalomcsillapító gyógyszert.
Az Abstral nyelv alatti tabletták hatóanyaga a fentanil. A fentanil az opiátoknak nevezett, hatékony fájdalomcsillapító gyógyszerek csoportjába tartozik.
Ellenjavallatok Amikor az Abstral nem alkalmazható
Ne szedje az Abstral -t
- ha allergiás a fentanilra vagy a gyógyszer (6. pontban felsorolt) egyéb összetevőjére.
- ha súlyos légzési problémái vannak
- ha rendszeresen nem használ orvosa által előírt opioid gyógyszert (például kodeint, fentanilt, hidromorfonot, morfint, oxikodont, petidint) minden nap, rendszeres időközönként, legalább egy hétig, a tartós fájdalom enyhítésére. Ha nem használja ezeket a gyógyszereket, ne használja az Abstral -t, mivel ez növelheti annak kockázatát, hogy légzése veszélyesen lelassul és / vagy megnehezül, vagy akár le is állhat.
- ha az áttörési fájdalomtól eltérő rövid távú fájdalmai vannak.
Az alkalmazással kapcsolatos óvintézkedések Mit kell tudnia az Abstral szedése előtt
Az Abstral szedése előtt beszéljen kezelőorvosával vagy gyógyszerészével, ha az alábbi események bármelyike van vagy volt a közelmúltban, mivel orvosának ezeket figyelembe kell vennie az adag felírása során:
- fejsérülés, mivel az Abstral elrejtheti a sérülés mértékét
- légzési problémák vagy myasthenia gravis (izomgyengeséggel jellemezhető állapot)
- ha szívproblémái vannak, különösen lassú szívverés
- alacsony vérnyomás
- vese- vagy májbetegség, mivel ez szükségessé teheti orvosától az adag gondosabb módosítását
- agydaganat és / vagy megnövekedett koponyaűri nyomás (megnövekedett agyi nyomás súlyos fejfájást, hányingert / hányást és homályos látást okoz)
- sebek a szájban vagy nyálkahártya -gyulladás (duzzanat és bőrpír a szájban)
- ha antidepresszánsokat vagy antipszichotikumokat szed, kérjük, olvassa el az "Egyéb gyógyszerek és az Abstral" részt
Ha az Abstral -kezelés alatt műtét előtt áll, kérjük, mondja el orvosának vagy fogorvosának, hogy ezt a gyógyszert szedi.
Azok számára, akik sporttevékenységet folytatnak: a gyógyszer terápiás szükségtelen használata doppingnak minősül, és mindenesetre pozitív doppingellenes tesztet eredményezhet.
Kölcsönhatások Milyen gyógyszerek vagy ételek módosíthatják az Abstral hatását
Feltétlenül tájékoztassa kezelőorvosát vagy gyógyszerészét a jelenleg vagy nemrégiben szedett, valamint szedni tervezett egyéb gyógyszereiről (a szokásos opioid fájdalomcsillapító gyógyszer kivételével).
A következő gyógyszerek fokozhatják az Abstral hatását:
- bizonyos típusú gombaellenes szerek, amelyek pl. ketokonazol vagy itrakonazol (gombás fertőzések kezelésére használják);
- bizonyos típusú fertőzések kezelésére használt antibiotikus gyógyszerek (makrolidoknak nevezett, például eritromicint tartalmazó gyógyszerek)
- bizonyos típusú vírusellenes gyógyszerek, az úgynevezett proteáz inhibitorok, amelyek pl. ritonavir (vírusok által okozott fertőzések kezelésére használják);
- alkoholtartalmú gyógyszerek;
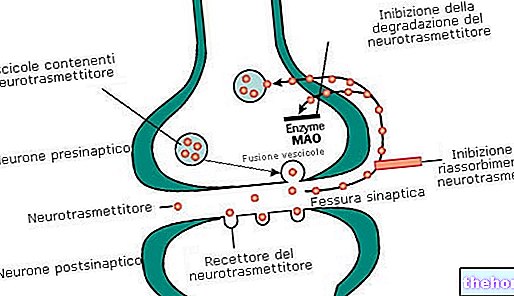
- monoamin -oxidáz (MAO) inhibitoroknak nevezett gyógyszerek, amelyeket súlyos depresszió és Parkinson -kór kezelésére alkalmaznak; tájékoztassa kezelőorvosát, ha az elmúlt két hétben szedett ilyen típusú gyógyszert.
A következő gyógyszerek csökkenthetik az Abstral hatását:
- Bizonyos típusú erős fájdalomcsillapítók, amelyeket részleges agonistáknak / antagonistáknak neveznek, például buprenorfin, nalbufin és pentazocin (fájdalomcsillapító gyógyszerek). Ezen gyógyszerek alkalmazásával összefüggésben elvonási tünetek (hányinger, hányás, hasmenés, szorongás, hidegrázás, remegés és izzadás) jelentkezhetnek.
Az Abstral fokozhatja az álmosságot okozó gyógyszerek hatását, például:
- egyéb erős fájdalomcsillapítók (opioid típusú gyógyszerek, pl. fájdalom és köhögés ellen)
- általános érzéstelenítők (műtétek során elaludnak)
- izomlazítók
- altatók
- kezelésére használt gyógyszerek
- depresszió
- allergiák
- szorongás és pszichózis
- klonidint tartalmazó gyógyszerek (magas vérnyomás kezelésére).
A mellékhatások kockázata nő, ha bizonyos antidepresszánsokat vagy antipszichotikumokat szed. Az Abstral kölcsönhatásba léphet ezekkel a gyógyszerekkel, és változásokat tapasztalhat a mentális állapotában (pl.izgatottság, hallucinációk, kóma) és egyéb hatások, például 38 ° C feletti testhőmérséklet, fokozott pulzusszám, instabil vérnyomás és túlzott reflexek, izommerevség, koordináció hiánya és / vagy gyomor -bélrendszeri tünetek (pl. hányinger, hányás, hasmenés). Kezelőorvosa megmondja, hogy az Abstral alkalmas -e Önre.
Az Abstral egyidejű bevétele étellel, itallal és alkohollal
Az Abstral egyes embereknél álmosságot okozhat. Ne fogyasszon alkoholt anélkül, hogy orvosával konzultálna, mert a szokásosnál álmosabbá teheti.
Ne igyon grapefruitlevet, ha felírták Önnel az Abstral kezelést, mivel ez fokozhatja az Abstral mellékhatásait.
Figyelmeztetések Fontos tudni, hogy:
Terhesség és szoptatás
Ne használja az Abstral -t terhesség alatt, kivéve, ha kezelőorvosa erre utasítja.
A fentanil bejuthat az anyatejbe, és mellékhatásokat okozhat a szoptatott csecsemőben. Ne szedje az Abstral -t szoptatás alatt, csak az utolsó Abstral adag bevétele után legalább 5 nappal kezdheti újra a szoptatást.
Mielőtt bármilyen gyógyszert szedne terhesség vagy szoptatás alatt, kérjen tanácsot orvosától vagy gyógyszerészétől.
A készítmény hatásai a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre
Az Abstral befolyásolhatja fizikai vagy mentális képességeit potenciálisan veszélyes tevékenységek elvégzésére, például gépjárművezetésre vagy gépek kezelésére.
Ha az Abstral szedése közben szédül, álmos vagy homályos a látása, ne vezessen gépjárművet és ne kezeljen gépeket.
Adagolás, az alkalmazás módja és ideje Az Abstral alkalmazása: Adagolás
Mielőtt először szedné az Abstral -t, orvosa elmagyarázza, hogyan kell szedni az áttörő fájdalom hatékony kezelésére.
Ezt a gyógyszert mindig az orvos által elmondottaknak megfelelően szedje. Ha kétségei vannak, forduljon orvosához vagy gyógyszerészéhez.
Ezt a terméket KIZÁRÓLAG használhatja, az orvos utasítása alapján. Senki más ne használja, mert Súlyos veszélyt jelenthet az egészségére, különösen a gyermekek számára.
Az Abstral különbözik más gyógyszerektől, amelyeket az áttöréses fájdalom kezelésére használt. Mindig az orvos által előírt Abstral adagot használja - ez eltérhet attól, amit más gyógyszerekkel együtt alkalmazott az áttöréses fájdalom kezelésére.
Kezdeti kezelés - megtalálja a legmegfelelőbb adagot
Ahhoz, hogy az Abstral működjön, orvosának meg kell határoznia az áttörő fájdalom kezelésére legmegfelelőbb adagot. Az Abstral számos erősségben kapható. Előfordulhat, hogy az áttörő fájdalom megnyilvánulásai során ki kell próbálnia az Abstral különböző erősségét, hogy megtalálja a legmegfelelőbb adagot. Orvosa segít megtalálni a legjobb adagot.
Ha nem kap megfelelő fájdalomcsillapítást egy adaggal, orvosa felkérheti Önt, hogy vegyen be egy extra adagot az áttörő fájdalom megnyilvánulásának kezelésére. Ne vegyen be második tablettát, kivéve, ha kezelőorvosa ezt mondja, mert túladagoláshoz vezethet.
Orvosa azt tanácsolhatja, hogy vegyen be egy adagot, amely egyszerre több tablettát tartalmaz. Ezt az adagot csak az orvos által előírt módon vegye be.
Várjon legalább 2 órát az utolsó adag bevétele után, mielőtt új áttörő fájdalmas eseményt kezelne az Abstral -lal. Folyamatos kezelés - miután megtalálta a megfelelő adagot Ha Ön és kezelőorvosa megtalálta az Abstral adagját, amely képes szabályozni az áttörő fájdalmat, akkor ezt az adagot legfeljebb napi négyszer vegye be. Az Abstral adagja egynél több tablettából állhat. Várjon legalább 2 órát az utolsó adag bevétele után, mielőtt új áttörő fájdalmas eseményt kezelne az Abstral -lal.
Ha úgy érzi, hogy az Ön által alkalmazott Abstral adag nem tudja kielégítően uralni áttörő fájdalmát, kérjük, tájékoztassa kezelőorvosát, mert szükség lehet az adag módosítására.
Ne változtassa meg az Abstral adagját, kivéve, ha orvosa ezt mondja.
A gyógyszer bevétele
Az Abstral -t szublingválisan kell alkalmazni. Ez azt jelenti, hogy a tablettát a nyelv alá kell helyezni, ahol gyorsan feloldódik, hogy a fentanil felszívódhasson a szájnyálkahártyán keresztül. Felszívódása után a fentanil elkezdi a fájdalomcsillapító hatását.
Ha áttörő fájdalmas epizódja van, vegye be az orvos által előírt adagot az alábbiak szerint:
- ha száraz a szája, igyon egy korty vizet, hogy megnedvesítse.
- közvetlenül a bevétel előtt vegyen ki egy vagy több tablettát a buborékcsomagolásból, az alábbiak szerint:
- válassza le a buborékcsomagolás egyik négyzetét a csomagolástól a pontozott vonalak mentén történő vágással (a buborékfólia többi négyzetét hagyja érintetlenül).
- Húzza le az alumínium fólia szélét, ahol a nyíl látható, és óvatosan vegye ki a tablettát. Ne próbálja átnyomni az Abstral nyelv alatti tablettákat a felső alumíniumrétegen, mert ez károsíthatja őket
- helyezze a tablettát a nyelv alá a lehető legmélyebbre, és hagyja teljesen feloldódni;
- Az Abstral gyorsan feloldódik a nyelv alatt, és felszívódik, hogy elvégezze fájdalomcsillapító hatását. Ezért fontos, hogy ne szívja, rágja vagy nyelje le a tablettát;
- ne igyon vagy egyen semmit, amíg a tabletta teljesen fel nem oldódott a nyelv alatt.
Ha idő előtt abbahagyja az Abstral szedését
Ha már nincs áttörő fájdalma, hagyja abba az Abstral szedését. Mindazonáltal továbbra is szedje a szokásos opiát alapú fájdalomcsillapító gyógyszert a tartós daganatos fájdalom kezelésére, az orvos utasítása szerint. Ha abbahagyja az Abstral szedését, az Abstral lehetséges mellékhatásaihoz hasonló gyógyszeres elvonási tüneteket tapasztalhat.
Beszéljen orvosával, ha elvonási tünetei alakulnak ki, vagy aggódik a fájdalmas tünetek enyhítése miatt. Kezelőorvosa dönti el, hogy felír -e gyógyszert az elvonási tünetek csökkentésére vagy megszüntetésére.
Ha bármilyen további kérdése van a gyógyszer alkalmazásával kapcsolatban, kérdezze meg kezelőorvosát vagy gyógyszerészét.
Túladagolás Mi a teendő, ha túl sok Abstral -t vett be?
Ha az előírtnál több Abstral -t vett be
- vegyen ki minden tablettát a szájából
- mondja el gondozójának vagy bárki másnak, hogy mi történt
- Önnek vagy gondozójának azonnal lépjen kapcsolatba orvosával, gyógyszerészével vagy a helyi kórházzal, és beszélje meg, mit tegyen
- az orvosra várva az embert ébren kell tartani beszélgetéssel vagy rázással
A túladagolás tünetei a következők:
- extrém álmosság
- lassulás és légzési nehézség
Ha ez megtörténik, azonnal sürgősségi orvosi ellátást kell kérni.
Ha úgy gondolja, hogy valaki véletlenül vette be az Abstral -t, azonnal kérjen sürgősségi orvosi ellátást.
Mellékhatások Mik az Abstral mellékhatásai?
Mint minden gyógyszer, így ez a gyógyszer is okozhat mellékhatásokat, amelyek azonban nem mindenkinél jelentkeznek.
Ha szokatlanul vagy rendkívül álmosnak érzi magát, vagy lassú vagy nehezen lélegzik, Önnek vagy gondozójának azonnal fel kell vennie a kapcsolatot orvosával vagy a helyi kórházzal sürgősségi orvosi beavatkozás érdekében (lásd még a 3. pontot "Ha több Abstral -t vett be, mint amennyi tartozik").
Nagyon gyakori mellékhatások (10 beteg közül több mint 1 beteget érinthet):
- hányinger
Gyakori mellékhatások (10 beteg közül legfeljebb 1 beteget érinthet):
- szédülés, fejfájás, túlzott álmosság
- zihálás / zihálás
- a szájnyálkahártya gyulladása, hányás, székrekedés, szájszárazság
- izzadás, fáradtság / fáradtság / energiahiány
Nem gyakori mellékhatások (100 beteg közül legfeljebb 1 beteget érinthet):
- allergiás reakció, remegés / remegés, zavart vagy homályos látás, gyors vagy lassú szívverés, alacsony vérnyomás, memóriavesztés
- depresszió, paranoia / motiválatlan félelemérzet, zavartság, tájékozódási zavar, szorongás / boldogtalanság / nyugtalanság, szokatlan boldogság / jó közérzet, hangulatingadozások
- mindig tele telt gyomor érzése, gyomorfájdalom, emésztési zavar
- szájfekély, nyelvproblémák, száj- vagy torokfájdalom, torokszűkület, ajak- vagy ínyfekély
- étvágytalanság, ízérzékelés / szaglás elvesztése vagy megváltozása
- alvászavar vagy alvászavar, figyelemzavar / könnyű figyelemelterelés, energiahiány / gyengeség / erővesztés
- bőrhibák, kiütések, viszketés, éjszakai izzadás, csökkent tapintási érzékenység, könnyű véraláfutások
- ízületi fájdalom vagy merevség, izommerevség
- kábítószer -elvonási tünetek (akkor fordulhatnak elő, ha a következő mellékhatások jelentkeznek: hányinger, hányás, hasmenés, szorongás, hidegrázás, remegés és izzadás), véletlen túladagolás, férfiaknál képtelenség az erekció elérésére és / vagy fenntartására, általános rossz közérzet
Ismeretlen gyakoriságú mellékhatások: (a gyakoriság nem becsülhető meg a rendelkezésre álló adatokból)
- nyelvduzzanat, súlyos légzési problémák, elesések, vörösség, nagyon meleg érzés, hasmenés, görcsök (görcsök), a karok vagy lábak duzzanata, nem látható dolgok látása vagy hallása (hallucinációk), láz.
Mellékhatások bejelentése
Ha bármilyen mellékhatást észlel, beleértve a betegtájékoztatóban fel nem sorolt bármilyen lehetséges mellékhatást is, forduljon orvosához vagy gyógyszerészéhez. A mellékhatásokat közvetlenül a hatóság részére is bejelentheti a www.agenziafarmaco.gov.it/it/responsabili webhelyen.
Lejárat és megőrzés
Az Abstral fájdalomcsillapító gyógyszere nagyon erős, és életveszélyes lehet, ha véletlenül gyermek veszi be. Az Abstral -t gyermekek elől elzárva tartandó!
A buborékcsomagoláson feltüntetett lejárati idő (EXP) után ne alkalmazza ezt a gyógyszert. A lejárati idő az adott hónap utolsó napjára vonatkozik.
Legfeljebb 25 ° C -on tárolandó.
A nedvességtől való védelem érdekében az eredeti buborékcsomagolásban tárolandó.
Javasoljuk, hogy az Abstral -t védett és zárt tárolóhelyen tárolja.
A fel nem használt készítményeket lehetőség szerint a gyógyszerésznek kell adni a biztonságos megsemmisítés érdekében. Semmilyen gyógyszert ne dobjon a szennyvízbe vagy a háztartási hulladékba, ez segít a környezet védelmében.
Határidő "> Egyéb információ
Mit tartalmaz az Abstral?
A készítmény hatóanyaga a fentanil.
Egy nyelv alatti tabletta a következőket tartalmazza:
- 100 mikrogramm fentanil (citrát)
- 200 mikrogramm fentanil (citrát)
- 300 mikrogramm fentanil (citrát)
- 400 mikrogramm fentanil (citrát)
- 600 mikrogramm fentanil (citrát)
- 800 mikrogramm fentanil (citrát)
Egyéb összetevők: mannit (E421), szilikátos mikrokristályos cellulóz, kroszkarmellóz -nátrium és magnézium -sztearát.
Milyen az Abstral külleme és mit tartalmaz a csomagolás?
Az Abstral egy kis fehér szublingvális tabletta, amelyet a nyelv alá helyeznek. Különböző erősségű és formájú változatban kapható. Kezelőorvosa előírja az Ön számára megfelelő erősségű (formájú) és számú tablettát.
- A 100 mikrogrammos tabletta fehér és kerek alakú
- A 200 mikrogrammos tabletta fehér és ovális alakú
- A 300 mikrogrammos tabletta fehér és háromszög alakú
- A 400 mikrogrammos tabletta fehér színű és ötszögletű
- A 600 mikrogrammos tabletta fehér és "D" alakú
- A 800 mikrogramm tabletta fehér és kapszula alakú
Az Abstral tabletta 10 vagy 30 tablettát tartalmazó dobozban kapható.
Nem feltétlenül mindegyik kiszerelés kerül kereskedelmi forgalomba.
Forrás betegtájékoztató: AIFA (Olasz Gyógyszerügynökség). A tartalom 2016 januárjában jelent meg. A jelenlévő információk nem feltétlenül naprakészek.
A legfrissebb verzióhoz való hozzáféréshez ajánlatos az AIFA (Olasz Gyógyszerügynökség) webhelyét elérni. Jogi nyilatkozat és hasznos információk.
01.0 A GYÓGYSZER MEGNEVEZÉSE -
ABSTRAL ALBERINGUAL TABLETTA
02.0 MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL -
Minden nyelv alatti tabletta tartalmaz
100 mcg fentanil (citrát formájában)
200 mcg fentanil (citrát formájában)
300 mcg fentanil (citrát formájában)
400 mcg fentanil (citrát formájában)
600 mcg fentanil (citrát formájában)
800 mcg fentanil (citrát formájában)
A segédanyagok teljes listáját lásd a 6.1 pontban.
03.0 GYÓGYSZERFORMA -
Nyelv alatti tabletta
A 100 mcg nyelv alatti tabletta fehér színű és kerek alakú
A 200 mcg nyelv alatti tabletta fehér színű és ovális alakú
A 300 mcg nyelv alatti tabletta fehér színű és háromszög alakú
A 400 mcg nyelv alatti tabletta fehér színű és rombusz alakú
A 600 mcg nyelv alatti tabletta fehér és "D" alakú
A 800 mcg nyelv alatti tabletta fehér és kapszula alakú
04.0 KLINIKAI INFORMÁCIÓK -
04.1 Terápiás javallatok -
Áttöréses fájdalom kezelése felnőtt betegeknél, akik krónikus rákfájdalom esetén opioid terápiát alkalmaznak. Az áttöréses fájdalom az egyébként kontrollált, tartós fájdalom átmeneti súlyosbodása.
04.2 Adagolás és alkalmazás
Az Abstral -t csak olyan betegeknek szabad adni, akik toleránsnak tekintik az opioid terápiát a tartós rákfájdalom miatt. A betegek akkor tekinthetők opioidtoleránsnak, ha naponta legalább 60 mg morfint, óránként legalább 25 mcg transzdermális fentanilt, naponta legalább 30 mg oxikodont, legalább 8 mg hidromorfonot szednek naponta. legalább egy hétig egy másik opioid egyenértékű fájdalomcsillapító adagját vette be.
Az alkalmazás módja:
Az Abstral szublingvális tablettákat közvetlenül a nyelv alatt, a legmélyebb részen kell beadni. Az Abstral nyelv alatti tablettákat nem szabad lenyelni, de hagyni kell teljesen feloldódni a nyelv alatti üregben, rágás vagy szopás nélkül. Tájékoztassa a betegeket, hogy ne egyenek vagy igyanak, amíg a tabletta teljesen fel nem oldódik.
Szájszáraz betegeknél az Abstral bevétele előtt vízzel lehet nedvesíteni a nyálkahártyát.
Dózis titrálás:
A dózistitrálás célja az optimális fenntartó dózis azonosítása az áttörő fájdalom megnyilvánulásainak folyamatos kezelésére. Ennek az optimális adagnak megfelelő fájdalomcsillapítást kell biztosítania, elfogadható szintű mellékhatásokkal.
Az Abstral optimális adagját minden egyes beteg esetében az adag fokozatos növelésével határozzák meg. A titrálás során számos erősség áll rendelkezésre. Az Abstral kezdő adagjának 100 mcg -nak kell lennie, szükség szerint növelve az adagot a rendelkezésre álló erősségek tartományában.
A betegeket gondosan ellenőrizni kell az optimális adag eléréséig.
A fentanilt tartalmazó készítményekről az Abstralra való áttérést nem szabad 1: 1 arányban elvégezni a különböző abszorpciós profilok miatt. Ha a betegek áttérnek egy másik fentanil-tartalmú készítményről, új titrálást kell végezni az Abstral-lal.
A titráláshoz az alábbi kezelési rend javasolt, bár az orvosnak minden esetben figyelembe kell vennie a beteg klinikai szükségleteit, életkorát és az egyidejű betegséget.
Minden betegnek el kell kezdenie a kezelést egyetlen 100 mikrogrammos nyelv alatti tabletta bevételével. Ha az egyetlen szublingvális tabletta beadását követő 15-30 percen belül nem érik el a megfelelő fájdalomcsillapítást, akkor egy további (második) szublingvális 100 mikrogrammos tablettát is be lehet adni. Ha az első adag beadását követő 15-30 percen belül nem érhető el megfelelő fájdalomcsillapítás, akkor a következő nagyobb adag tablettáját kell figyelembe venni az áttörő fájdalom későbbi megnyilvánulása szempontjából (lásd az alábbi ábrát).
Az adag módosítását fokozatosan kell folytatni, amíg a megfelelő fájdalomcsillapítást el nem érik a tolerálható mellékhatásokkal. A kiegészítő szublingvális tabletta (második tabletta) adagját 100 mikrogrammról 200 mikrogrammra kell emelni 400 mikrogrammos vagy annál nagyobb adagokra, az alábbi ábra szerint: ebben a titrálási fázisban ne adjon be két adagnál többet egy áttöréses fájdalom epizódra.
ABSZTRÁLIS TITRÁCIÓS ELJÁRÁS
Ha megfelelő fájdalomcsillapítás érhető el a legnagyobb dózissal, de a mellékhatásokat elfogadhatatlannak tartják, akkor közbenső dózist (szükség szerint 100 mikrogrammos szublingvális tablettát használva) lehet adni.
A titrálás során a betegeket utasíthatják arra, hogy a 100 mcg és / vagy 200 mcg tabletták többszörösét vegye be bármely egyszeri adaghoz. Négynél több tablettát soha nem szabad egyszerre használni.
A 800 mcg feletti dózisok hatékonyságát és biztonságosságát nem értékelték betegekkel végzett klinikai vizsgálatok során.
Az opioidokkal kapcsolatos mellékhatások kockázatának minimalizálása és a megfelelő dózis azonosítása érdekében elengedhetetlen, hogy a titrálási folyamat során az egészségügyi szakemberek szorosan monitorozzák a betegeket.
A titrálás során a betegeknek legalább 2 órát kell várniuk, mielőtt áttöréses fájdalom új megnyilvánulását kezelik az Abstral -lal.
Fenntartó terápia:
Miután megállapították a megfelelő dózist, amely több tablettából is állhat, a betegeknek továbbra is ezt az adagot kell alkalmazniuk, és legfeljebb napi négy Abstral adagra kell korlátozniuk a fogyasztást.
A fenntartó időszak alatt a betegeknek legalább 2 órát kell várniuk, mielőtt új áttöréses fájdalom -megnyilvánulást kezelnének az Abstral -lal.
Az adagolás módosítása:
Ha az Abstral titrált dózisára adott válasz (fájdalomcsillapítás vagy mellékhatások) jelentősen megváltozik, szükség lehet az optimális adag fenntartásának módosítására.
Ha naponta több mint négy áttöréses fájdalom epizód fordul elő, több mint négy egymást követő napon keresztül, akkor a tartós fájdalom kezelésére alkalmazott hosszú hatású opioid adagját újra kell értékelni. Ha a hosszú hatású opioidot vagy annak dózisát megváltoztatják, az Abstral adagját újra kell értékelni, és ismét titrálni kell annak biztosítása érdekében, hogy az optimális legyen a beteg számára.
Feltétlenül szükséges, hogy a fájdalomcsillapító új dózisának titrálását egészségügyi szakember ellenőrizze.
A terápia abbahagyása:
Az absztral terápiát azonnal abba kell hagyni, ha a beteg nem tapasztal áttörő fájdalmat. A tartós áttöréses fájdalom kezelését az orvos utasítása szerint kell folytatni.
Ha minden opioid terápiát abba kell hagyni, az orvosnak gondosan ellenőriznie kell a beteget a hirtelen megvonási hatások kockázatának kezelése érdekében.
Alkalmazása gyermekeknél és serdülőknél:
Az Abstral nem alkalmazható 18 év alatti betegeknél a biztonságosságra és a hatásosságra vonatkozó adatok hiánya miatt.
Alkalmazása idős embereknél:
Az adag titrálását különösen óvatosan kell megközelíteni, és a betegeket gondosan figyelni kell a fentanil toxicitás jeleire (lásd 4.4 pont).
Alkalmazása vese- és májelégtelenségben szenvedő betegeknél:
A máj- vagy veseelégtelenségben szenvedő betegeket gondosan ellenőrizni kell az Abstral dózisának titrálása során a fentanil -toxicitás jelei szempontjából (lásd 4.4 pont).
04.3 Ellenjavallatok -
A készítmény hatóanyagával vagy a 6.1 pontban felsorolt bármely segédanyagával szembeni túlérzékenység.
Opioid fenntartó terápia nélküli betegek, mivel fokozott a légzési depresszió kockázata.
Súlyos légzési depresszió vagy súlyos obstruktív tüdőbetegség.
Az áttöréses fájdalomtól eltérő akut fájdalom kezelése.
04.4 Különleges figyelmeztetések és a használattal kapcsolatos óvintézkedések -
A betegeket és gondozóikat tájékoztatni kell az Abstral olyan hatóanyagának olyan mennyiségben való jelenlétéről, amely halálos lehet a gyermek számára, és ezért minden tablettát gyermekektől elzárva kell tartani.
Az opioid terápia, például az Abstral szedése során fellépő potenciálisan súlyos mellékhatások miatt a betegeket és gondozóikat tájékoztatni kell az Abstral helyes alkalmazásának fontosságáról és arról, hogy mit tegyenek, ha mégis.
Az Abstral-kezelés megkezdése előtt fontos, hogy a tartós hatású opioidokkal végzett kezelést stabilizálják a tartós fájdalom csökkentése érdekében.
Az opioidok, például a fentanil ismételt alkalmazásával fizikai és / vagy pszichológiai függőség és függőség alakulhat ki. Az opiátok terápiás alkalmazását követően ritka az atrogénfüggőség.
Mint minden opioid esetében, az Abstral alkalmazása is klinikailag jelentős légzési depresszió kockázatával jár. Különös óvatossággal kell eljárni az Abstral adagjának titrálásakor krónikus obstruktív tüdőbetegségben vagy más légzési depresszióra hajlamos állapotban szenvedő betegeknél (pl. Myasthenia gravis). a további légzésdepresszió veszélye miatt, ami légzési elégtelenséget okozhat.
Az Abstral -t csak rendkívül óvatosan kell alkalmazni olyan betegeknél, akik különösen érzékenyek a hiperkapnia koponyaűri hatásaira, azaz azoknál, akiknél nyilvánvaló az intrakraniális nyomás növekedése, megváltozott tudatállapot, kóma vagy agydaganatok. Fejsérült betegeknél az opioidok alkalmazása elhomályosíthatja a klinikai lefolyást, ilyen esetekben az opioidokat csak feltétlenül szükséges alkalmazni.
Szívbetegség
A fentanil bradycardiát okozhat. A fentanilt óvatosan kell alkalmazni azoknál a betegeknél, akiknél korábban vagy folyamatban van bradyarrhythmiák.
A fentanil alkalmazásával végzett intravénás vizsgálatokból származó adatok azt mutatják, hogy az idős betegeknél a clearance csökkenhet és a felezési idő meghosszabbodhat, és érzékenyebbek lehetnek a hatóanyagra, mint a fiatalabb betegek. Idős, kaktikus vagy legyengült betegeket monitorozni kell. Gondos megfigyelés a fentanil toxicitás megnyilvánulása szempontjából és szükség esetén az adagokat csökkenteni kell.
Az Abstral -t óvatosan kell alkalmazni máj- vagy veseelégtelenségben szenvedő betegeknél, különösen a titrálási szakaszban. Az Abstral máj- vagy veseelégtelenségben szenvedő betegeknél történő alkalmazása növelheti a fentanil biohasznosulását és csökkentheti szisztémás clearance -ét, ami az opioid hatások felhalmozódásához, illetve fokozódásához vagy meghosszabbodásához vezethet.
Óvatosan kell eljárni a hypovolaemiában és hipotóniában szenvedő betegek kezelésében.
Az Abstral -t nem vizsgálták szájüregi elváltozásokban vagy nyálkahártya -gyulladásban szenvedő betegeknél. Ilyen betegeknél fennáll a fokozott szisztémás gyógyszer -expozíció veszélye, ezért fokozott óvatosság ajánlott a titrálás során.
Az Abstral -kezelés abbahagyásának nyilvánvaló hatásai nem lehetnek, de lehetséges elvonási tünetek a szorongás, remegés, izzadás, sápadtság, hányinger és hányás.
Szerotonin szindróma
• Óvatosság szükséges, ha az Abstral -t olyan gyógyszerekkel együtt adják, amelyek befolyásolják a szerotoninerg neurotranszmissziós rendszereket.
A szerotoninerg gyógyszerek, például a szelektív szerotonin-visszavétel gátlók (SSRI-k) és a szerotonin-norepinefrin-visszavétel-gátlók (SNRI-k) egyidejű használatával, valamint a szerotonin-anyagcserét gátló gyógyszerekkel (beleértve a monoamin-oxidáz-gátlókat [MAOI-k]) potenciálisan életveszélyes szerotonin kialakulása Ez előfordulhat az ajánlott dózistartományon belül.
A szerotonin szindróma magában foglalhatja a mentális állapot megváltozását (pl. Izgatottság, hallucinációk, kóma), autonóm instabilitást (pl. Tachycardia, labilis vérnyomás, hipertermia), neuromuscularis rendellenességeket (pl. Hyperreflexia, koordináció hiánya, merevség) és / vagy gyomor -bélrendszeri tüneteket (pl. Hányinger) , hányás, hasmenés).
Szerotonin -szindróma gyanúja esetén az Abstral -kezelést abba kell hagyni.
04.5 Kölcsönhatások más gyógyszerekkel és egyéb interakciók -
A fentanilt a CYP3A4 metabolizálja. Azok a gyógyszerek, amelyek gátolják a CYP3A4 aktivitást, mint például a makrolid antibiotikumok (pl. Eritromicin), azol gombaellenes szerek (pl. Ketokonazol, itrakonazol) vagy egyes proteáz inhibitorok (pl. Ritonavir) növelhetik a fentanil biohasznosulását, csökkenthetik szisztémás clearance -ét és potenciálisan fokozhatják vagy meghosszabbíthatják az opioidot hatások. A grapefruitlé a CYP3A4 ismert inhibitora is. Ezért a fentanilt óvatosan kell alkalmazni azoknál a betegeknél, akik egyidejűleg CYP3A4 -gátlókat szednek.
Más központi idegrendszeri depresszánsok, például más morfinszármazékok (fájdalomcsillapítók és köhögéscsillapítók), általános érzéstelenítők, mozgásszervi relaxánsok, nyugtató antidepresszánsok, nyugtató H1 antihisztaminok, barbiturátok, szorongásoldók (pl. Benzodiazepinek), altatók, antipszichotikumok, klonidin és rokon anyagok egyidejű alkalmazása fokozott depresszív hatást gyakorolhat a központi idegrendszerre. Légzési depresszió, hypotensio és mély szedáció léphet fel.
Az alkohol fokozza a morfin-alapú fájdalomcsillapítók nyugtató hatását, ezért alkoholos italok vagy alkoholtartalmú gyógyszerek egyidejű alkalmazása nem javasolt az Abstral-lal.
Az Abstral nem ajánlott azoknak a betegeknek, akik az elmúlt 14 napban monoamin -oxidáz (MAO) inhibitorokat szedtek, mivel a MAO -gátlók súlyos és előre nem látható potenciális fokozódásáról számoltak be opioid fájdalomcsillapítókkal.
A részleges opioid agonisták / antagonisták (például buprenorfin, nalbufin, pentazocin) egyidejű alkalmazása nem ajánlott. Ezek a gyógyszerek nagy affinitással rendelkeznek a viszonylag alacsony belső aktivitású opiátreceptorokkal szemben, ezért részben antagonista hatást fejtenek ki az analgetikus hatáshoz képest fentanilt, és kábítószer-elvonási tüneteket válthat ki opioidfüggő betegeknél.
Szerotonerg gyógyszerek
A fentanil egyidejű alkalmazása szerotoninerg szerrel, például szelektív szerotonin-visszavétel gátlóval (SSRI) vagy szerotonin-norepinefrin-visszavétel gátlóval (SNRI) vagy monoamin-oxidáz gátlóval (MAO) növelheti a potenciálisan életveszélyes szerotonin-szindróma kockázatát állapot.
04.6 Terhesség és szoptatás -
A fentanil biztonságosságát terhesség alatt nem állapították meg. Állatkísérletek reprodukciós toxicitást és károsodott fertilitást mutattak patkányokban (lásd 5.3 pont). Az emberre gyakorolt lehetséges kockázat nem ismert. A fentanil terhesség alatt nem alkalmazható, kivéve, ha feltétlenül szükséges.
A terhesség alatti hosszú távú kezelés elvonási tüneteket okozhat a csecsemőknél.
A fentanil nem alkalmazható szülés és szülés alatt (beleértve a császármetszést is), mivel a gyógyszer átjut a méhlepényen, és légzési depressziót okozhat a magzatban vagy az újszülöttben.
Etetési idő
A fentanil az anyatejbe vándorol, és nyugtatást és légzési depressziót okozhat a szoptatott csecsemőben. A fentanil nem alkalmazható szoptató nőknél, és a szoptatást csak a fentanil utolsó beadása után legalább 5 nappal lehet folytatni.
04.7 Hatások a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre -
Az Abstral alkalmazásával kapcsolatban nem végeztek vizsgálatokat a gépjárművezetéshez és gépek kezeléséhez szükséges képességekről.
Az opioid fájdalomcsillapítók azonban befolyásolják a potenciálisan veszélyes tevékenységek, például a gépjárművezetéshez és a gépek kezeléséhez szükséges fizikai vagy szellemi képességeket. Tájékoztatni kell a betegeket, hogy ne vezessenek gépjárművet vagy ne kezeljenek gépeket, ha szédülnek vagy álmosak, vagy homályos vagy kettős látásuk van az Abstral szedése alatt.
04.8 Nemkívánatos hatások -
Jellemző opioid mellékhatások várhatók az Abstral alkalmazásával; Az opioidok használatával kapcsolatos legsúlyosabb lehetséges mellékhatások a légzésdepresszió (ami légzésleállást okozhat), hipotenzió és sokk.
Az Abstral klinikai vizsgálatainak célja az áttöréses fájdalom kezelésének biztonságosságának és hatékonyságának értékelése volt rákos betegeknél. Minden beteg tartós fájdalom miatt egyidejűleg adott opioidokat, például elnyújtott hatóanyag-leadású morfint, retardált oxikodont vagy transzdermális fentanilt. az Abstral önmagában okozott hatásainak végleges azonosítása.
Az Abstral leggyakrabban megfigyelt mellékhatásai közé tartoznak a tipikus opioid mellékhatások, például hányinger, székrekedés, aluszékonyság és fejfájás.
Az Abstral és / vagy más fentanilt tartalmazó vegyületeknél észlelt mellékhatások táblázatos listája:
Az alábbi megfigyelt mellékhatásokat jelentették az Abstral és / vagy más fentanil-tartalmú vegyületeknél a klinikai vizsgálatokban és a forgalomba hozatalt követő tapasztalatokban. Szervrendszerek és gyakoriság szerint (nagyon gyakori ≥ 1/10; gyakori ≥ 1-től) /100, a
* Opioid elvonási tünetek, mint például hányinger, hányás, hasmenés, szorongás, borzongás, remegés és izzadás. fentanil nyálkahártya -beadásakor figyeltek meg
A feltételezett mellékhatások bejelentése
A gyógyszer engedélyezése után jelentkező feltételezett mellékhatások bejelentése fontos, mivel lehetővé teszi a gyógyszer előny / kockázat arányának folyamatos nyomon követését. Az egészségügyi szakembereket kérjük, hogy jelentsék be a feltételezett mellékhatásokat a nemzeti bejelentési rendszeren keresztül. "Cím www. agenziafarmaco.gov.it/it/responsabili.
04.9 Túladagolás -
A fentanil túladagolásának tünetei a farmakológiai hatások felerősödése, amelynek legsúlyosabb hatása a légzésdepresszió, amely légzésleállást okozhat.
Az opioid túladagolás azonnali kezelése magában foglalja a fennmaradó Abstral nyelv alatti tabletták eltávolítását a szájból, a beteg fizikai és verbális stimulációját, valamint a tudatosság felmérését. Szabadalmi légutat kell kialakítani és fenntartani. Ha szükséges, helyezzen be oropharyngealis légutat vagy endotracheális csövet, adjon be oxigént, és indítsa el a gépi lélegeztetést, ha szükséges. Tartsa fenn a megfelelő testhőmérsékletet és a parenterális folyadék beadását.
A véletlen túladagolás kezelésére opioidot még nem kapó egyéneknél a naloxont vagy más opioid antagonistákat klinikai indikációk szerint és a vonatkozó alkalmazási előírás alapján kell alkalmazni. Ha a légzésdepresszió időtartama meghosszabbodik, opioid antagonisták ismételt adására lehet szükség.
Óvatosan kell eljárni a naloxon vagy más opioid antagonisták alkalmazásával a túladagolás kezelésére az opioid terápiában részesülő betegeknél, mivel fennáll az akut elvonási szindróma veszélye.
Súlyos vagy tartós hipotenzió esetén fel kell mérni a hypovolaemiát, és megfelelő parenterális folyadékterápiával kezelni kell a problémát.
Légzést zavaró izommerevséget jelentettek fentanil és más opiátok esetén. Ebben a helyzetben szükség lehet endotracheális intubációra, asszisztált lélegeztetésre, valamint opiát antagonisták és izomrelaxánsok beadására.
05.0 FARMAKOLÓGIAI TULAJDONSÁGOK -
05,1 "Farmakodinamikai tulajdonságok -
Farmakoterápiás csoport: fájdalomcsillapítók, opiátok; fenil -piperidin -származékok.
ATC kód: N02AB03.
A fentanil erős mc-opioid fájdalomcsillapító, gyors fájdalomcsillapítással és rövid hatástartammal. A fentanil másodlagos hatásai a központi idegrendszerre (CNS), valamint a légzőrendszerre és a gyomor -bélrendszer működésére az opioid fájdalomcsillapítókra jellemzőek, és osztályhatásoknak minősülnek. Ide tartozhatnak a légzési depresszió, a bradycardia, a hipotermia, a székrekedés, a myosis, a fizikai függőség és az eufória.
A fentanil fájdalomcsillapító hatása a hatóanyag vérszintjéhez kapcsolódik; opioid-kezelésben nem részesült betegeknél a fentanil minimális hatékony fájdalomcsillapító szérumkoncentrációja 0,3 és 1,2 ng / ml között van, míg a 10-20 ng / ml vérszint sebészeti érzéstelenítést és mély légzési depressziót okoz.
Krónikus rákfájdalomban szenvedő betegeknél, akik stabil fenntartó dózisú opioidokat szedtek, statisztikailag szignifikánsan javult a fájdalom intenzitása közötti különbség az Abstral és a placebo között 10 perccel az adagolás után, szignifikánsan kevesebb terápiára volt szükség. Fájdalomcsillapító "szükség szerint".
Az Abstral biztonságosságát és hatékonyságát az áttöréses fájdalom kezdetén szedő betegeknél értékelték. Az Abstral megelőző alkalmazását a kiszámítható fájdalom epizódok megelőzésére klinikai vizsgálatokban nem vizsgálták.
A fentanil, mint minden opiát mc receptor agonista, dózisfüggő légzési depressziót okoz. Ez a kockázat nagyobb az opioidot még nem kapó betegeknél, mint azoknál a betegeknél, akik súlyos fájdalmat tapasztaltak, vagy krónikus opioid terápiában részesülnek. A hosszú távú opioid kezelés általában függőséget okoz mellékhatásaik miatt.
Míg az opiátok jellemzően növelik a húgyúti simaizom tónusát, a végső hatás általában változó, egyes esetekben sürgősséget, másokban pedig vizeletürítési nehézséget okoz.
Az opiátok növelik a tónusot és csökkentik a gyomor -bél traktus simaizmainak meghajtó összehúzódásait, ami meghosszabbítja a gyomor -bélrendszeri áthaladási időt, ami mögött a fentanil székrekedő hatása állhat.
05,2 "Farmakokinetikai tulajdonságok -
A fentanil erősen lipofil gyógyszer, nagyon gyorsan felszívódik a száj nyálkahártyáján és lassabban a gyomor -bél traktuson keresztül. A szájon át alkalmazott fentanil kifejezett máj- és bélrendszeri első lépést okoz.
Az Abstral gyorsan oldódó szublingvális tabletta. A fentanil gyors felszívódása az Abstral beadása után körülbelül 30 percen belül megtörténik. Az Abstral abszolút biohasznosulása 54%volt. A fentanil átlagos maximális plazmakoncentrációja 0,2-1,3 ng / ml (100-800 mcg Abstral beadása után), és eléri 22,5-240 percen belül.
A fentanil körülbelül 80-85% -a kötődik a plazmafehérjékhez, főként az 1-glikoproteinhez, és kisebb mértékben az albuminhoz és a lipoproteinhez. A fentanil egyensúlyi állapotú eloszlási térfogata körülbelül 3-6 l / kg.
A fentanil elsősorban a CYP3A4 útján metabolizálódik számos farmakológiailag inaktív metabolitra, beleértve a norfentanilt. A fentanil intravénás beadását követő 72 órán belül az adag körülbelül 75% -a választódik ki a vizelettel, elsősorban metabolitok formájában, kevesebb mint 10% -a változatlan gyógyszerként. Az adag körülbelül 9% -a a széklettel van jelen, főként metabolitok formájában. A fentanil teljes plazma clearance -e körülbelül 0,5 l / h / kg.
Az Abstral beadását követően a fentanil elsődleges eliminációs felezési ideje körülbelül 7 óra (3-12,5 óra tartomány), a végső felezési ideje pedig körülbelül 20 óra (tartomány 11,5-25 óra).
Az Abstral farmakokinetikája 100-800 mikrogramm dózistartományban a dózissal arányos volt. Farmakokinetikai vizsgálatok kimutatták, hogy több tabletta bioekvivalens az egyenértékű adag egyetlen tablettájával.
Vese- / májelégtelenség
Az elégtelen máj- vagy vesefunkció növelheti a szérumkoncentrációt. Idős, kaktikus vagy általában legyengült betegeknél a fentanil-clearance alacsonyabb lehet, ami hosszabb "végső felezési időt" okozhat (lásd 4.2 és 4.4 pont).
05.3 A preklinikai biztonságossági adatok -
A biztonságosságra és az ismételt dózisú toxicitásra vonatkozó farmakológiai adatok nem támasztanak alá különleges veszélyt az emberre, amelyre még nem tér ki ez az alkalmazási előírás. Állatkísérletek kimutatták, hogy a patkányok magzataiban csökkent a termékenység és a mortalitás. A teratogén hatásokat azonban nem igazolták.
A baktériumok és rágcsálók mutagenitási vizsgálatai negatív eredményeket adtak. Más opiátokhoz hasonlóan a fentanil is mutagén hatást fejt ki in vitro emlőssejteken. A mutagén kockázat terápiás alkalmazás esetén valószínűtlennek tűnik, mivel a hatásokat csak nagyon magas koncentrációban indukálták.
A fentanillal végzett karcinogenitási vizsgálatok (26 hetes alternatív dermális biológiai vizsgálat TgAC transzgenikus egereken; 2 éves szubkután karcinogenitási vizsgálat patkányokon) nem mutattak ki onkogén potenciálra utaló eredményeket. A patkányokon végzett karcinogenezis vizsgálatból származó agylemezek értékelése agyi elváltozásokat mutatott ki a fentanil -citrát nagy dózisaival kezelt állatoknál. Ezeknek az eredményeknek az emberre vonatkozó relevanciája nem ismert.
06.0 GYÓGYSZERÉSZETI INFORMÁCIÓK
06.1 Segédanyagok -
Mannit (E421)
Szilikált mikrokristályos cellulóz
Kroskarmellóz -nátrium
Magnézium-sztearát
06.2 Inkompatibilitás "-
Nem releváns.
06.3 Érvényességi idő "-
2 év.
06.4 Különleges tárolási előírások -
Legfeljebb 25 ° C -on tárolandó.
A nedvességtől való védelem érdekében az eredeti csomagolásban tárolandó.
06.5 A közvetlen csomagolás jellege és a csomagolás tartalma -
Az Abstral szublingvális tablettákat gyermekbiztos buborékcsomagolásba csomagolják, papír / poliészter / alumíniummal bélelt OPA / alumínium / PVC zsebbel, külső dobozban. Az Abstral szublingvális tabletták minden egyes erősségének csomagolása színkóddal van ellátva, egy adott azonosító szín szerint.
Kiszerelés: 10 vagy 30 szublingvális tablettát tartalmazó csomagolás. Nem feltétlenül mindegyik kiszerelés kerül kereskedelmi forgalomba.
06.6 Használati és kezelési útmutató -
A hulladék anyagokat biztonságosan kell ártalmatlanítani. A betegeket és gondozóikat arra kell ösztönözni, hogy a fel nem használt készítményeket vigyék vissza a gyógyszertárba, ahol azt a nemzeti és helyi előírásoknak megfelelően kell megsemmisíteni.
07.0 A „FORGALOMBA HOZATALI ENGEDÉLY” TULAJDONOSA -
Kyowa Kirin Kft
Galabank Üzleti Park
Galashiels
TD1 1QH
Egyesült Királyság
08.0 A FORGALOMBA HOZATALI ENGEDÉLY SZÁMA -
AIC n 038736031 - "100 McG szublingvális tabletta" 10 tabletta buborékcsomagolásban Opa / PVC / Al / Al
AIC n 038736043 - "100 McG szublingvális tabletta" 30 tabletta buborékcsomagolásban Opa / PVC / Al / Al
AIC n 038736056 - "200 McG szublingvális tabletta" 10 tabletta buborékcsomagolásban Opa / PVC / Al / Al
AIC n 038736068 - "200 McG szublingvális tabletta" 30 tabletta buborékcsomagolásban Opa / PVC / Al / Al
AIC n 038736070 - "300 McG szublingvális tabletta" 10 tabletta buborékcsomagolásban Opa / PVC / Al / Al
AIC n 038736082 - "300 McG szublingvális tabletta" 30 tabletta buborékcsomagolásban Opa / PVC / Al / Al
AIC n 038736094 - "400 McG szublingvális tabletta" 10 tabletta buborékcsomagolásban Opa / PVC / Al / Al
AIC n 038736106 - "400 McG szublingvális tabletta" 30 tabletta buborékcsomagolásban Opa / PVC / Al / Al
AIC n 038736118 - "600 McG szublingvális tabletta" 10 tabletta buborékcsomagolásban Opa / PVC / Al / Al
AIC n 038736120 - "600 McG szublingvális tabletta" 30 tabletta buborékcsomagolásban Opa / PVC / Al / Al
AIC n 038736132 - "800 McG szublingvális tabletta" 10 tabletta buborékcsomagolásban Opa / PVC / Al / Al
AIC n 038736144 - "800 McG szublingvális tabletta" 30 tabletta buborékcsomagolásban Opa / PVC / Al / Al
09.0 AZ ELSŐ ENGEDÉLYZÉS ÉS A JÓVÁHAGYÁS MEGÚJÍTÁSÁNAK DÁTUMA -
Az első engedélyezés dátuma: 2008-02-29
Utolsó megújítás dátuma: 2013.02.28
10.0 A SZÖVEG FELÜLVIZSGÁLÁSÁNAK DÁTUMA -
2016. május