Hatóanyagok: dipiridamol, acetilszalicilsav
AGGRENOX 200 mg + 25 mg módosított hatóanyag-leadású kemény kapszula
Indikációk Miért alkalmazzák az Aggrenox -ot? Mire való?
GYÓGYSZERÉSZETI KATEGÓRIA
Antitrombotikumok, vérlemezke -gátlók - dipiridamol / acetilszalicilsav kombinációja.
GYÓGYSZERJELZÉSEK
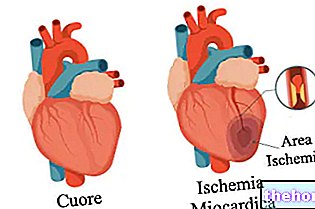
Az agyvérzés megelőzése olyan betegeknél, akiknél korábban átmeneti ischaemiás rohamok vagy trombózis miatti teljes ischaemiás stroke jelentkezett (másodlagos megelőzés).
Ellenjavallatok Amikor az Aggrenox -ot nem szabad alkalmazni
- Túlérzékenység a hatóanyagokra (dipiridamol és acetilszalicilsav), szalicilátokra vagy bármely segédanyagra.
- Aktív gyomor- vagy nyombélfekélyben vagy véralvadási zavarban szenvedő betegek.
- Terhesség és szoptatás: Az AGGRENOX általában ellenjavallt a terhesség első és második trimeszterében, valamint a szoptatás alatt; ellenjavallt a harmadik trimeszterben (lásd még "Különleges figyelmeztetések").
- A gyógyszer alkalmazása ellenjavallt gyermekeknél és tizenhat év alatti fiataloknál.
- Az acetilszalicilsav jelenléte miatt kerülni kell az AGGRENOX adását súlyos veseelégtelenségben (10 ml / perc alatti glomeruláris szűrési sebesség) szenvedő vagy májbetegekben.
Ritka örökletes állapotok esetén, amelyek összeegyeztethetetlenek a gyógyszer segédanyagával, ugyanez ellenjavallt.
Az alkalmazással kapcsolatos óvintézkedések Mit kell tudnia az Aggrenox szedése előtt?
Az acetilszalicilsavra vonatkozó figyelmeztetések
Az acetilszalicilsav jelenléte miatt az AGGRENOX-ot óvatosan kell alkalmazni asztmában, allergiás náthában, orrpolipokban, krónikus vagy visszatérő gyomor- vagy nyombélfájdalomban, vese- vagy májelégtelenségben vagy glükóz-6-foszfát-dehidrogenáz-hiányban szenvedő betegeknél. Az AGGRENOX-kezelés megkezdése előtt meg kell győződni arról, hogy a betegnek korábban nem voltak-e túlérzékenységi reakciói acetilszalicilsavval vagy más nem szteroid gyulladásgátlókkal szemben.
Szív- és érrendszeri patológiák
Többek között a dipiridamol értágító hatású. A dipiridamolt óvatosan kell alkalmazni súlyos koszorúér -betegségben szenvedő betegeknél, beleértve az instabil anginát vagy a közelmúltban bekövetkezett szívinfarktust, a kamrai kiáramlás elzáródását vagy a hemodinamikai instabilitást (pl. Pangásos szívelégtelenség).
Myasthenia gravis
Myasthenia gravisban szenvedő betegeknél szükség lehet a kezelési rend módosítására, ha a dipiridamol adagját megváltoztatják (lásd "Interakciók").
Az AGGRENOX -ban jelen lévő acetilszalicilsav dózisát nem vizsgálták a miokardiális infarktus másodlagos megelőzésében.
Gyermekek és serdülők
Lehetséges összefüggés van az acetilszalicilsav és a Reye -szindróma között, ha gyermekeknek adják be. Ezért az AGGRENOX nem alkalmazható lázas állapotú vagy lázas vagy anélküli vírusfertőzésben szenvedő gyermekeknél és serdülőknél a Reye -szindróma kockázata miatt. A Reye -szindróma nagyon ritka betegség, amely befolyásolja az agyat és a májat, és halálos lehet.
Idős államporgárok
A 70 év feletti emberek, különösen egyidejű terápia jelenlétében, csak orvosával folytatott konzultációt követően használhatják ezt a gyógyszert.
Kölcsönhatások Mely gyógyszerek vagy élelmiszerek módosíthatják az Aggrenox hatását
Tájékoztassa kezelőorvosát vagy gyógyszerészét, ha nemrégiben szedett más gyógyszereket, beleértve a vény nélkül kapható készítményeket is.
Nem szteroid gyulladáscsökkentők (NSAID-ok) / Kortikoszteroidok / Alkohol
Az emésztőrendszeri mellékhatások fokozódnak, ha az acetilszalicilsavat NSAID -okkal, kortikoszteroidokkal vagy krónikus alkoholfogyasztással kombinálják.
A dipiridamol és az acetilszalicilsav társulása nem növeli a vérzés gyakoriságát.
Az ibuprofen egyidejű alkalmazása, de természetesen nem más NSAID -ok vagy paracetamolé, korlátozhatja az aszpirin jótékony kardiovaszkuláris hatásait fokozott kardiovaszkuláris kockázatú betegeknél.
A véralvadást befolyásoló anyagok
Ha a dipiridamolt más véralvadást befolyásoló anyagokkal, például véralvadásgátlókkal és vérlemezkékkel kombinálva alkalmazzák, figyelembe kell venni az ezen gyógyszerek betegtájékoztatójában leírt óvintézkedéseket, figyelmeztetéseket és tolerálhatóságot.
Az acetilszalicilsavról kimutatták, hogy növeli a vérzés kockázatát, ha antikoaguláns, vérlemezke -gátló gyógyszerekkel, szelektív szerotonin -visszavétel -gátlókkal (SSRI -k) vagy anagreliddel együtt adják.
Ha a dipiridamolt warfarinnal együtt adják, a vérzés nem gyakoribb vagy intenzívebb, mint önmagában a warfarin.
Antikonvulzív szerek
Kimutatták, hogy az acetilszalicilsav fokozza a valproinsav és a fenitoin hatását, növelve a mellékhatások kockázatát.
Adenozin
A dipiridamol növeli az adenozin vérszintjét és kardiovaszkuláris hatásait, ezért mérlegelni kell az adenozin adagjának módosítását.
Vérnyomáscsökkentők
A dipiridamol fokozhatja a vérnyomáscsökkentő gyógyszerek vérnyomáscsökkentő hatását.
Kolinészteráz inhibitorok
A dipiridamol ellensúlyozhatja a kolinészteráz inhibitor gyógyszerek antikolinészteráz hatását, és potenciálisan súlyosbíthatja a myasthenia gravis eseteit.
Hypoglykaemics / Methotrexate
A hipoglikémiás gyógyszerek hatását és a metotrexát toxicitását fokozhatja az acetilszalicilsav egyidejű alkalmazása.
Spironolakton / Uricosuric szerek
Az acetilszalicilsav csökkentheti a spironolakton natriuretikus hatását, és gátolhatja az urikozúrikus gyógyszerek (például probenecid, szulfinpirazon) hatását.
A kezelés hatása módosulhat, ha az acetilszalicilsavat más gyógyszerekkel együtt alkalmazzák, mint például:
- antikoagulánsok (pl. warfarin);
- kilökődés elleni gyógyszerek (pl. ciklosporin, takrolimusz);
- vérnyomáscsökkentők (pl. vízhajtók és ACE -gátlók);
- fájdalomcsillapítók és gyulladásgátlók (pl. szteroidok, NSAID-ok);
- köszvény elleni gyógyszerek (probenecid);
- rákellenes és rheumatoid arthritis gyógyszerek (metotrexát).
Az acetilszalicilsav alkalmazása előtt tájékoztassa kezelőorvosát, ha bármilyen más gyógyszert szed (beleértve az öngyógyítást is).
Figyelmeztetések Fontos tudni, hogy:
Vérzés
A vérzés kockázata miatt, mint más vérlemezke -gátló szerekhez hasonlóan, az AGGRENOX -ot óvatosan kell alkalmazni fokozott vérzési kockázatú betegeknél, őket gondosan figyelemmel kell kísérni a vérzés jelei, beleértve az okkult vérzést is (lásd "Interakciók").
Azokat a betegeket, akik egyidejűleg olyan gyógyszereket szednek, amelyek növelhetik a vérzés kockázatát, mint például antikoagulánsok, vérlemezke -gátló szerek, szelektív szerotonin -visszavétel -gátlók (SSRI -k), anagrelid, óvatosan kell kezelni (lásd "Interakciók").
Epebetegségek
Kevés olyan esetet jelentettek, amikor a nem konjugált dipiridamolt különböző mennyiségben (a kő száraz tömegének akár 70% -áig) építették be az epekőbe. Ezek a betegek mind idősek voltak, emelkedő cholangitisben szenvedtek, és évek óta orális dipiridamollal kezelték őket. Ezeknél a betegeknél a dipiridamol nem bizonyította az epekő kiváltó okát. Lehetséges, hogy az epes konjugált dipiridamol bakteriális deglucuronidációja lehet az a mechanizmus, amely felelős a dipiridamol epekövekben való jelenlétéért.
Fejfájás vagy migrén
A fejfájást vagy migrént, amelyek különösen az AGGRENOX -kezelés kezdetén jelentkezhetnek, nem szabad acetilszalicilsav fájdalomcsillapító dózisokkal kezelni.
Stressz teszt intravénás dipiridamollal
A klinikai tapasztalatok azt sugallják, hogy az orális dipiridamollal kezelt betegeknek, akiknek intravénás dipiridamollal végzett gyógyszeres stresszteszten is részt kell venniük, 24 órával az intravénás dipiridamol-kezelés előtt le kell állítaniuk az orális dipiridamol-tartalmú gyógyszeres kezelést. intravénás dipiridamollal együtt ronthatja a teszt érzékenységét.
Terhesség vagy szoptatás alatt alkalmazza
Mielőtt bármilyen gyógyszert elkezdene szedni, kérjen tanácsot orvosától vagy gyógyszerészétől.
Terhesség
Nincs elegendő bizonyíték a dipiridamol és az alacsony dózisú acetilszalicilsav terhesség alatti biztonságosságára. Ezért az AGGRENOX -ot a terhesség első és második trimeszterében csak akkor szabad alkalmazni, ha az orvos elengedhetetlennek tartja a várható előnyök szempontjából a lehetséges kockázatokhoz képest. Ezenkívül az AGGRENOX -ot nem szabad alkalmazni a terhesség harmadik trimeszterében (lásd "Ellenjavallatok").
Etetési idő
A dipiridamol és a szalicilátok kiválasztódnak az anyatejbe. Ezért az AGGRENOX csak szoptató nőknél alkalmazható, ha feltétlenül szükséges.
Termékenység
Nem végeztek vizsgálatokat a gyógyszer emberi termékenységre gyakorolt hatásáról.
Hatások a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre
A gyógyszer gépjárművezetéshez és gépek kezeléséhez szükséges képességekre gyakorolt hatását nem vizsgálták.
A klinikai vizsgálatok során azonban olyan tüneteket jelentettek, mint a szédülés és a zavartság (lásd "Mellékhatások"). Ezért a betegeknek azt tanácsolják, hogy legyenek óvatosak gépjárművezetés vagy gépek kezelése közben.
Ha a betegek ilyen tüneteket tapasztalnak, kerülniük kell a potenciálisan veszélyes tevékenységeket, például a gépjárművezetést vagy a gépek kezelését.
Fontos információk az AGGRENOX egyes összetevőiről
Az AGGRENOX laktózt és szacharózt tartalmaz. Ha kezelőorvosa korábban már figyelmeztette Önt, hogy bizonyos cukrokra érzékeny, keresse fel orvosát, mielőtt elkezdi szedni ezt a gyógyszert.
Adagolás és alkalmazás Az Aggrenox alkalmazása: Adagolás
Orális adagolásra. Az ajánlott adag 1 kapszula naponta kétszer, általában 1 reggel és 1 este, lehetőleg étkezés közben.
A kapszulákat egészben, rágás nélkül kell lenyelni.
Ha bármilyen további kérdése van az AGGRENOX alkalmazásával kapcsolatban, kérdezze meg kezelőorvosát vagy gyógyszerészét.
Túladagolás Mi a teendő, ha túl sok Aggrenoxot vett be?
Ha véletlenül lenyeli / beveszi az AGGRENOX túlzott adagját, azonnal értesítse orvosát, vagy menjen a legközelebbi kórházba.
Tünetek
Tekintettel a dipiridamol és az acetilszalicilsav dózisarányára, a túladagolást a dipiridamol jelei és tünetei uralják.
A bejelentett esetek kis száma miatt a dipiridamol túladagolásával kapcsolatban kevés tapasztalat áll rendelkezésre. Olyan tünetek várhatók, mint a forró érzés, kipirulás, izzadás, nyugtalanság, gyengeségérzés, szédülés és anginafájdalmak. Vérnyomásesés és tachycardia figyelhető meg.
Az acetilszalicilsav szerény akut túladagolásának jelei és tünetei a hiperventiláció, zümmögés, hányinger, hányás, látás- és hallászavar, szédülés és zavartság. Súlyos mérgezés esetén delírium, remegés, nehézlégzés, izzadás figyelhető meg. Vérzés, kiszáradás, zavarok a sav-bázis egyensúlyban és a vér elektrolit összetételében, hipotermiában és kómában. A szédülés és a fülcsengés a túladagolás tünete lehet, különösen idős betegeknél.
Terápia
Javasolt tüneti terápia. A xantin -származékok (pl. Aminofillin) beadása ellensúlyozhatja a dipiridamol túladagolásának hemodinamikai hatásait. Széles szöveti eloszlása és túlnyomó hepatikus eliminációja miatt a dipiridamol alig áll rendelkezésre. Gyorsított eltávolításra.
Ha bármilyen további kérdése van az AGGRENOX alkalmazásával kapcsolatban, kérdezze meg kezelőorvosát vagy gyógyszerészét.
Mellékhatások Melyek az Aggrenox mellékhatásai?
Mint minden gyógyszer, így az AGGRENOX is okozhat mellékhatásokat, amelyek azonban nem mindenkinél jelentkeznek.
Az AGGRENOX nemkívánatos hatásai szisztémás-szerves osztályok szerint felsorolva:
A vér és a nyirokrendszer zavarai
Trombocitopénia (csökkent vérlemezkeszám), vérszegénység, vashiányos vérszegénység okkult gasztrointesztinális vérzés miatt.
Az immunrendszer zavarai
Túlérzékenységi reakciók, beleértve a kiütést, csalánkiütést, súlyos hörgőgörcsöt és angioödémát.
Idegrendszeri betegségek
Koponyaűri vérzés, szédülés, fejfájás, sőt migrén (különösen a kezelés kezdetén).
Szembetegségek
A szem vérzése.
Szív patológiák
Tachycardia, a koszorúér -betegség tüneteinek súlyosbodása, ájulás.
Érpatológiák
Hipotenzió, hőhullámok.
Légzőrendszeri, mellkasi és mediastinalis betegségek
Orrvérzés.
Emésztőrendszeri betegségek
Hányás, hányinger, hasmenés, dyspepsia, gyomorfekély, nyombélfekély, eróziós gastritis, gyomor -bélrendszeri vérzés, hasi fájdalom.
A bőr és a bőr alatti szövet betegségei
Bőrvérzés, beleértve a zúzódásokat, véraláfutásokat és hematómákat.
Az izom -csontrendszer, a kötőszövet rendellenességei
Mialgia.
Diagnosztikai tesztek
Hosszan tartó vérzési idő.
Sérülés, mérgezés és eljárási komplikációk
Az eljárás utáni vérzés, eljárási vérzés.
Az egyes hatóanyagokra vonatkozó további ismert nemkívánatos hatások a következők, és ezeket szintén az AGGRENOX -ra szánták.
Dipiridamol:
A dipiridamol önmagában alkalmazott mellékhatásai a következők:
A dipiridamolt jelentették az epekövekbe.
Acetilszalicilsav:
Az acetilszalicilsav önmagában történő alkalmazása során jelentett további mellékhatások a következők:
A vér és a nyirokrendszer zavarai
Disszeminált intravaszkuláris koaguláció, koagulopátia.
Az immunrendszer zavarai
Anafilaxiás reakciók (különösen asztmás betegeknél).
Anyagcsere- és táplálkozási rendellenességek
Hipoglikémia (gyermekek), hiperglikémia, szomjúság, kiszáradás, hiperkalémia, metabolikus acidózis, légúti alkalózis.
Pszichiátriai rendellenességek
Zavaros állapot.
Idegrendszeri betegségek
Izgatottság, agyi ödéma, letargia, görcsök. Fül- és labirintuszavarok Tinnitus, süketség.
Szív patológiák
Aritmia.
Légzőrendszeri, mellkasi és mediastinalis betegségek
Légszomj, ínyvérzés, gégeödéma, hiperventiláció, tüdőödéma, tachypnea.
Emésztőrendszeri betegségek
Perforált gyomorfekély, perforált nyombélfekély, melaena, haematemesis, pancreatitis.
Máj- és epebetegségek
Hepatitis, Reye -szindróma.
A bőr és a bőr alatti szövet betegségei
Polimorf erythema.
Az izom -csontrendszer, a kötőszövet rendellenességei
Rhabdomyolysis.
Vese- és húgyúti betegségek
Veseelégtelenség, intersticiális nephritis, vese papilláris nekrózis, proteinuria.
Terhesség, gyermekágyi időszak és perinatális állapotok
Hosszan tartó terhesség, elhúzódó szülés, kicsi csecsemők, halvaszületés, vérzés a terhesség alatt, szülés utáni vérzés.
Általános betegségek és az alkalmazás helyén fellépő állapotok
Láz, hipotermia.
Diagnosztikai tesztek
- kóros májfunkciós tesztek, emelkedett vér húgysav (köszvényes rohamokhoz vezethet), elhúzódó protrombin idő.
A betegtájékoztatóban található utasítások betartása csökkenti a nemkívánatos hatások kockázatát.
Mellékhatások bejelentése
Ha Önnél bármilyen mellékhatás jelentkezik, tájékoztassa erről kezelőorvosát vagy gyógyszerészét. Ez a betegtájékoztatóban fel nem sorolt bármilyen lehetséges mellékhatásra is vonatkozik. A mellékhatásokat közvetlenül a hatóság részére is bejelenthetik a www.agenziafarmaco.it/it/responsabili webhelyen. A mellékhatások bejelentésével Ön is hozzájárulhat ahhoz, hogy minél több információ álljon rendelkezésre a gyógyszer biztonságosságáról.
Lejárat és megőrzés
Figyelmeztetés: ne használja a gyógyszert a csomagoláson feltüntetett lejárati idő után.
A feltüntetett lejárati idő az ép csomagolású termékre vonatkozik, helyesen tárolva.
Tárolja 30 ° C alatt, tartsa zárva az üveget a nedvességtől való védelem érdekében.
AZ AGGRENOXOT GYERMEKEK ELLENŐRZÉSÉTŐL ELZÁRVA KELL TARTANI.
A gyógyszereket nem szabad a szennyvízzel vagy a háztartási hulladékkal együtt megsemmisíteni. Kérdezze meg gyógyszerészét, hogy mit tegyen a már nem használt gyógyszereivel. Ez segít a környezet védelmében.
Egyéb információk
FOGALMAZÁS
Egy kapszula tartalma: Hatóanyagok: 200 mg dipiridamol; acetilszalicilsav 25 mg.
Segédanyagok: borkősav, povidon, metakrilsav-metil-metakrilát kopolimer (1: 2), talkum, arab gumi, hipromellóz-ftalát, hipromellóz, triacetin, dimetikon 350, sztearinsav / palmitinsav, laktóz-monohidrát, alumínium-sztearát, kolloid szilícium-dioxid, , mikrokristályos cellulóz, szacharóz, E 171; kapszula (kemény): zselatin, E 171, E 172, tisztított víz.
GYÓGYSZERFORMA ÉS TARTALOM
Módosított hatóanyag-leadású kemény kapszulák. Kiszerelés: 50, 60 kapszula.
Nem feltétlenül mindegyik kiszerelés kerül kereskedelmi forgalomba.
Forrás betegtájékoztató: AIFA (Olasz Gyógyszerügynökség). A tartalom 2016 januárjában jelent meg. A jelenlévő információk nem feltétlenül naprakészek.
A legfrissebb verzióhoz való hozzáféréshez ajánlatos az AIFA (Olasz Gyógyszerügynökség) webhelyét elérni. Jogi nyilatkozat és hasznos információk.
01.0 A GYÓGYSZER MEGNEVEZÉSE
AGGRENOX 200 MG + 25 MG Keményen módosított felszabadító kapszula
02.0 MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL
Egy kapszula tartalmaz:
dipiridamol 200 mg
acetilszalicilsav 25 mg
Ismert hatású segédanyagok: egy kapszula 53 mg laktózt és 11,3 mg szacharózt tartalmaz
A segédanyagok teljes listáját lásd a 6.1 pontban
03.0 GYÓGYSZERFORMA
Módosított hatóanyag-leadású kemény kapszulák.
04.0 KLINIKAI INFORMÁCIÓK
04.1 Terápiás javallatok
Az AGGRENOX a stroke megelőzésére javallott azoknál a betegeknél, akiknél korábban átmeneti ischaemiás rohamok vagy trombózis miatti teljes ischaemiás stroke jelentkezett (másodlagos megelőzés).
04.2 Adagolás és alkalmazás
Az ajánlott adag egy kapszula naponta kétszer, általában egyszer reggel és egyszer este, lehetőleg étkezés közben.
A kapszulákat egészben, rágás nélkül kell lenyelni.
04.3 Ellenjavallatok
• Túlérzékenység a hatóanyagokkal, szalicilátokkal vagy bármely segédanyaggal szemben.
• Aktív gyomor- vagy nyombélfekélyben vagy véralvadási zavarban szenvedő betegek.
• Terhesség és szoptatás: Az AGGRENOX általában ellenjavallt a terhesség első és második trimeszterében, valamint a szoptatás alatt, ellenjavallt a harmadik trimeszterben (lásd 4.6 pont).
• A gyógyszer alkalmazása ellenjavallt gyermekeknél és tizenhat év alatti fiataloknál.
• Az acetilszalicilsav jelenléte miatt kerülni kell az AGGRENOX adását súlyos veseelégtelenségben (glomeruláris szűrési sebesség kevesebb, mint 10 ml / perc) vagy májban (lásd még 5.2 pont).
Ritka örökletes állapotok esetén, amelyek összeegyeztethetetlenek a gyógyszer segédanyagával, ugyanez ellenjavallt.
04.4 Különleges figyelmeztetések és a használathoz szükséges óvintézkedések
Vérzés
A vérzés kockázata miatt, mint más vérlemezke -gátló szerekhez hasonlóan, az AGGRENOX -ot óvatosan kell alkalmazni fokozott vérzési kockázatú betegeknél, őket gondosan figyelemmel kell kísérni a vérzés jelei, beleértve az okkult vérzést is (lásd 4.5 pont).
Azokat a betegeket, akik egyidejűleg olyan gyógyszereket szednek, amelyek növelhetik a vérzés kockázatát, mint például antikoagulánsok, vérlemezke -gátló szerek, szelektív szerotonin -visszavétel -gátlók (SSRI -k) vagy anagrelid, óvatosan kell kezelni (lásd 4.5 pont).
Szív- és érrendszeri patológiák
Többek között a dipiridamol értágító hatású. A dipiridamolt óvatosan kell alkalmazni súlyos koszorúér -betegségben szenvedő betegeknél, beleértve az instabil anginát vagy a közelmúltban bekövetkezett szívinfarktust, a kamrai kiáramlás elzáródását vagy a hemodinamikai instabilitást (pl. Pangásos szívelégtelenség).
Az AGGRENOX -ban jelen lévő acetilszalicilsav dózisát nem vizsgálták a miokardiális infarktus másodlagos megelőzésében.
Myasthenia gravis
Myasthenia gravisban szenvedő betegeknél a dipiridamol adagjának megváltoztatása esetén szükség lehet a kezelési rend módosítására (lásd 4.5 pont).
Epebetegségek
Kevés olyan esetet jelentettek, amikor a nem konjugált dipiridamolt különböző mennyiségben (a kő száraz tömegének akár 70% -áig) építették be az epekőbe. Ezek a betegek mind idősek voltak, emelkedő cholangitisben szenvedtek, és évek óta orális dipiridamollal kezelték őket. Ezeknél a betegeknél a dipiridamol nem bizonyította az epekő kiváltó okát. Lehetséges, hogy az epes konjugált dipiridamol bakteriális deglucuronidációja lehet az a mechanizmus, amely felelős a dipiridamol epekövekben való jelenlétéért.
Fejfájás vagy migrén
A fejfájást vagy migrént, amelyek különösen az AGGRENOX -kezelés kezdetén jelentkezhetnek, nem szabad acetilszalicilsav fájdalomcsillapító dózisokkal kezelni.
Túlérzékenység
Ezenkívül óvatosság ajánlott azoknál a betegeknél, akik túlérzékenyek az NSAID -okra.
Az acetilszalicilsavra vonatkozó figyelmeztetések
Az acetilszalicilsav jelenléte miatt az AGGRENOX-ot óvatosan kell alkalmazni asztmában, allergiás náthában, orrpolipokban, krónikus vagy visszatérő gyomor- vagy nyombélfájdalomban, vese- vagy májelégtelenségben (lásd 5.2 pont) vagy glükóz-6-foszfát hiányban szenvedő betegeknél. dehidrogenáz.
Gyermekek és serdülők
Lehetséges összefüggés van az acetilszalicilsav és a Reye -szindróma között, ha gyermekeknek adják be. Ezért az AGGRENOX nem alkalmazható lázas állapotú vagy lázas vagy anélküli vírusfertőzésben szenvedő gyermekeknél és serdülőknél a Reye -szindróma kockázata miatt. A Reye -szindróma nagyon ritka betegség, amely befolyásolja az agyat és a májat, és halálos lehet.
Idős államporgárok
A 70 év feletti emberek, különösen egyidejű terápia jelenlétében, csak orvosával folytatott konzultációt követően használhatják ezt a gyógyszert.
Stressz teszt intravénás dipiridamollal
A klinikai tapasztalatok azt sugallják, hogy az orális dipiridamollal kezelt betegeknek, akiknek intravénás dipiridamollal végzett gyógyszeres stresszteszten is részt kell venniük, 24 órával az intravénás dipiridamol-kezelés előtt le kell állítaniuk az orális dipiridamol-tartalmú gyógyszeres kezelést. intravénás dipiridamollal együtt ronthatja a teszt érzékenységét.
Az AGGRENOX egyes összetevőire vonatkozó figyelmeztetések
Egy kapszula 53 mg laktózt és 11,3 mg szacharózt tartalmaz, amelyek 106 mg laktózt és 22,6 mg szacharózt alkotnak a javasolt maximális napi adagban: ritka örökletes fruktóz- és / vagy galaktóz-intoleranciában, laktázhiányban vagy glükóz- galaktóz felszívódási zavar vagy szacharáz izomaltáz elégtelenség nem szedheti ezt a gyógyszert.
04.5 Kölcsönhatások más gyógyszerekkel és egyéb interakciók
Nem szteroid gyulladáscsökkentők (NSAID-ok) / Kortikoszteroidok / Alkohol
Az emésztőrendszeri mellékhatások fokozódnak, ha az acetilszalicilsavat NSAID -okkal, kortikoszteroidokkal vagy krónikus alkoholfogyasztással kombinálják.
Az ibuprofen egyidejű alkalmazása, de természetesen nem más NSAID -ok vagy paracetamolé, korlátozhatja az aszpirin jótékony kardiovaszkuláris hatásait fokozott kardiovaszkuláris kockázatú betegeknél.
A véralvadást befolyásoló anyagok
Ha a dipiridamolt más, a véralvadást befolyásoló anyagokkal, például véralvadásgátlókkal és vérlemezkékkel együtt alkalmazzák, figyelembe kell venni ezen gyógyszerek biztonságossági profilját.
Az acetilszalicilsavról kimutatták, hogy növeli a vérzés kockázatát, ha antikoagulánsokkal, vérlemezke -gátló gyógyszerekkel, szelektív szerotonin -visszavétel -gátlókkal (SSRI -k) vagy anagreliddel együtt adják.
A dipiridamol és az acetilszalicilsav társulása nem növeli a vérzés gyakoriságát.
Ha a dipiridamolt warfarinnal együtt adják, a vérzés nem gyakoribb vagy intenzívebb, mint önmagában a warfarin.
Antikonvulzív szerek
Kimutatták, hogy az acetilszalicilsav fokozza a valproinsav és a fenitoin hatását, növelve a mellékhatások kockázatát.
Adenozin
A dipiridamol növeli az adenozin vérszintjét és kardiovaszkuláris hatásait, ezért mérlegelni kell az adenozin adagjának módosítását.
Vérnyomáscsökkentők
A dipiridamol fokozhatja a vérnyomáscsökkentő gyógyszerek vérnyomáscsökkentő hatását.
Kolinészteráz inhibitorok
A dipiridamol ellensúlyozhatja a kolinészteráz inhibitor gyógyszerek antikolinészteráz hatását, és potenciálisan súlyosbíthatja a myasthenia gravis eseteit (lásd 4.4 pont).
Hypoglykaemics / Methotrexate
A hipoglikémiás gyógyszerek hatását és a metotrexát toxicitását fokozhatja az acetilszalicilsav egyidejű alkalmazása.
Spironolakton / Uricosuric szerek
Az acetilszalicilsav csökkentheti a spironolakton natriuretikus hatását, és gátolhatja az urikozúrikus gyógyszerek (például probenecid, szulfinpirazon) hatását.
A kísérleti adatok azt mutatják, hogy az ibuprofen gátolhatja az alacsony dózisú acetilszalicilsav vérlemezke-aggregációra gyakorolt hatását, ha a gyógyszereket egyidejűleg alkalmazzák. Azonban a korlátozott adatok és bizonytalanságok a klinikai helyzetben való alkalmazásukra vonatkozóan nem teszik lehetővé a következtetések levonását az ibuprofen; úgy tűnik, nincs klinikailag releváns hatása az ibuprofen időnkénti alkalmazásának (lásd 5.1 pont).
04.6 Terhesség és szoptatás
Terhesség
Bár a preklinikai vizsgálatok nem mutattak ki egészségügyi kockázatot (lásd 5.3 pont), nincs elegendő bizonyíték a dipiridamol és az alacsony dózisú acetilszalicilsav terhesség alatti biztonságosságára. Ezért az AGGRENOX -ot a terhesség első és második trimeszterében csak akkor szabad alkalmazni, ha az orvos elengedhetetlennek tartja a várható előnyök szempontjából a lehetséges kockázatokhoz képest.
Az AGGRENOX a terhesség harmadik trimeszterében is ellenjavallt.
Etetési idő
A dipiridamol és a szalicilátok kiválasztódnak az anyatejbe (lásd 5.2 és 5.3 pont).
Ezért szoptató nőknél az AGGRENOX -ot csak feltétlenül szükséges beadni.
Termékenység
Nem végeztek vizsgálatokat a gyógyszer emberi termékenységre gyakorolt hatásáról. A dipiridamollal vagy acetilszalicilsavval végzett preklinikai vizsgálatokban nem figyeltek meg termékenységi károsodást (lásd 5.3 pont).
04.7 Hatások a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre
A gyógyszer gépjárművezetéshez és gépek kezeléséhez szükséges képességekre gyakorolt hatását nem vizsgálták.
A betegeket azonban figyelmeztetni kell arra, hogy a klinikai vizsgálatok során olyan tüneteket jelentettek, mint a szédülés és a zavartság. Ezért óvatosságra van szükség, amikor gépjárművet vezet vagy gépeket kezel.
Ha a betegek ilyen tüneteket tapasztalnak, kerülniük kell a potenciálisan veszélyes tevékenységeket, például a gépjárművezetést vagy a gépek kezelését.
04.8 Nemkívánatos hatások
A biztonsági profil összefoglalása
Az AGGRENOX biztonságossági profiljának meghatározásához két nagyszabású vizsgálat (ESPS-2, PRoFESS) eredményeit, amelyekbe összesen 26 934 beteget vontak be, akik közül 11 831-et az AGGRENOX kezelési csoportba soroltak. Ezeket az adatokat integrálták az AGGRENOX forgalomba hozatal utáni széles körű tapasztalatába.
A leggyakrabban jelentett mellékhatások a fejfájás, szédülés és gyomor -bélrendszeri események, például diszpepszia, hasmenés, hányinger és hasi fájdalom. Az AGGRENOX alkalmazásával kapcsolatos legfontosabb súlyos mellékhatások a vérzéses események voltak.
Nemkívánatos hatások táblázat
A következő mellékhatásokat jelentették az AGGRENOX alkalmazása során az ESPS-2 és a PRoFESS vizsgálatokban, valamint a spontán jelentések eredményeként.
1 A dipiridamol önmagában ismert mellékhatásai
2 Az acetilszalicilsav monoterápia ismert mellékhatásai
A kiválasztott mellékhatások leírása
Az AGGRENOX alkalmazásával kapcsolatos legfontosabb súlyos mellékhatások a vérzéses események voltak. Az ESPS-2 és a PRoFESS vizsgálatokból származó adatokat vérzési események, köztük súlyos vérzések alapján értékelték. A vérzési eseményeket osztályozták. emésztőrendszeri vérzés:
Az ESPS-2 kontrollált vizsgálatban 1650 beteget kezeltek az AGGRENOX csoportban (100%) és 1649 beteget a placebo csoportban (100%). A kezelés átlagos időtartama 1,4 év volt. A vérzések teljes előfordulási gyakorisága 8,7% volt az AGGRENOX csoportban és 4,5% a placebo csoportban. A súlyos vérzések gyakorisága 1,6%, illetve 0,4% volt. Az intrakraniális vérzések gyakorisága 0,6%, illetve 0,4%, míg a gyomor -bélrendszeri vérzések gyakorisága 4,3%, illetve 2,6% volt.
A PRoFESS vizsgálatban 10 055 beteget kezeltek az AGGRENOX csoportban (100%). A kezelés átlagos időtartama 1,9 év volt. A vérzés teljes előfordulási gyakorisága 5,3%volt. A súlyos vérzések gyakorisága 3,3%. Az intrakraniális vérzések incidenciája 1,2%(beleértve az intraokuláris vérzést (0, 2%)), míg a gyomor -bélrendszeri vérzések gyakorisága 1,9%.
A feltételezett mellékhatások bejelentése
A gyógyszer engedélyezése után jelentkező feltételezett mellékhatások bejelentése fontos, mivel lehetővé teszi a gyógyszer előny / kockázat arányának folyamatos nyomon követését. Az egészségügyi szakembereket kérjük, hogy jelentsék be a feltételezett mellékhatásokat a nemzeti bejelentési rendszeren keresztül. "Cím www. agenziafarmaco.gov.it/it/responsabili.
04.9 Túladagolás
Tünetek
Tekintettel a dipiridamol és az acetilszalicilsav dózisarányára, a túladagolást a dipiridamol jelei és tünetei uralják.
A bejelentett esetek kis száma miatt a dipiridamol túladagolásával kapcsolatban kevés tapasztalat áll rendelkezésre. Olyan tünetek várhatók, mint a meleg érzés, kipirulás, izzadás, nyugtalanság, gyengeségérzés, szédülés és anginafájdalmak. Vérnyomásesés és tachycardia figyelhető meg.
Az acetilszalicilsav szerény akut túladagolásának jelei és tünetei a hiperventiláció, a zümmögés, az émelygés, a hányás, a látás és hallás zavara, szédülés és zavartság.
Súlyos mérgezés esetén delírium, remegés, dyspnoe, izzadás, vérzés, kiszáradás, a sav-bázis egyensúly és a vér elektrolit összetételének zavara, hipotermia és kóma figyelhető meg.
A szédülés és a fülcsengés a túladagolás tünete lehet, különösen idős betegeknél.
Terápia
Javasolt tüneti terápia. A xantin -származékok (pl .: aminofillin) beadása ellensúlyozhatja a dipiridamol túladagolásának hemodinamikai hatásait. Széles szöveti eloszlása és túlnyomó hepatikus eliminációja miatt a dipiridamol alig áll rendelkezésre. Gyorsított eltávolításra.
05.0 FARMAKOLÓGIAI TULAJDONSÁGOK
05.1 Farmakodinámiás tulajdonságok
Farmakoterápiás csoport: antitrombotikumok, vérlemezke -gátlók; ATC kód: B01AC.
Az acetilszalicilsav / dipiridamol kombináció antitrombotikus hatása a különféle biokémiai mechanizmusokon alapul.
L "acetilszalicilsav visszafordíthatatlanul inaktiválja a ciklo-oxigenáz enzimet a vérlemezkékben, ezáltal megakadályozza a tromboxán A2 termelését, amely a vérlemezke-aggregáció és az érszűkület erős induktora.
Az dipiridamol gátolja az adenozin felvételét eritrocitákban, vérlemezkékben és endoteliális sejtekben in vitro és in vivo; A gátlás maximális értéke megközelítőleg 80%, és a terápiás koncentrációban (0,5 - 2 mcg / ml) alkalmazott dózistól függ. Következésképpen megnő az adenozin helyi koncentrációja, amely a vérlemezkék A2 -receptorára hat, stimulálja a vérlemezke -adenil -ciklázt, és ezáltal növeli a vérlemezkékben a ciklikus adenozin -monofoszfát (AMPc) szintjét.
Ezért a vérlemezkék aggregációját különböző ingerek, például vérlemezke -aktiváló faktor (PAF), kollagén és adenozin -difoszfát (ADP) hatására gátolják. A csökkent vérlemezke -aggregáció csökkenti a vérlemezke -fogyasztást a normális szintre. Ezenkívül az adenozin értágító hatású, és ez az egyik mechanizmusok, amelyek révén a dipiridamol vazodilatációt okoz.
A stroke-os betegeknél kimutatták, hogy a dipiridamol csökkenti a vérlemezkékben jelen lévő felszíni protrombotikus fehérjék (PAR-1: trombinreceptor) sűrűségét, valamint csökkenti a c-reaktív fehérje (CRP) és a von Willebrand-faktor (vWF) szintjét.) . In vitro kutatások kimutatták, hogy a dipiridamol szelektíven gátolja a gyulladásos citokineket (MCP-1 és MMP-9), amelyek a vérlemezke-monocita kölcsönhatásból származnak.
Farmakodinamika
A dipiridamol gátolja a foszfodiészterázt (PDE) különböző szövetekben.
Míg az AMPc-PDE gátlása gyenge, a dipiridamol terápiás szintje gátolja a ciklikus guanozin-monofoszfát-PDE-t (GMPc-PDE), ezáltal növelve az "EDRF (endotéliumból származó relaxáló faktor," nitrogén-monoxid (NO) ") által termelt GMPc növekedését )).
A dipiridamol fokozza a szöveti plazminogén aktivátor felszabadulását a mikrovaszkuláris endotélsejtekből, és kimutatták, hogy dózisfüggő módon fokozza az endothelsejtek antitrombotikus tulajdonságait a trombusképződésre a szomszédos subendoteliális mátrixon. A dipiridamol az oxi- és peroxigyökök hatékony tisztítószere.
A dipiridamol stimulálja a prosztaciklin bioszintézisét és felszabadulását az endotélium által, és csökkenti a szubendoteliális struktúrák trombogenitását azáltal, hogy növeli a védőközvetítő 13-HODE (13-hidroxi-oktadekadieno-sav) koncentrációját.
Míg az acetilszalicilsav csak a vérlemezkék aggregációját gátolja, a dipiridamol a vérlemezkék aktivációját és tapadását is gátolja. Ezért az acetilszalicilsav és a dipiridamol antitrombotikus hatása additív.
Klinikai vizsgálatok
Az AGGRENOX-ot egy 24 hónapos, kettős vak, placebo-kontrollos vizsgálatban (European Stroke Prevention Study 2, ESPS2) tanulmányozták, amelyben 6602 betegnél jelentkezett ischaemiás stroke vagy átmeneti ischaemiás roham (TIA) három hónapon belül a beiratkozás előtt.
A betegeket a négy kezelési csoport egyikébe randomizálták: AGGRENOX (ASA / nyújtott hatóanyag-leadású dipiridamol) 25 mg / 200 mg; 200 mg nyújtott hatóanyag-leadású dipiridamol (ER-DP); 25 mg ASA önmagában vagy placebo. A betegek naponta kétszer kapszulát kaptak (reggel és este).
A hatékonyság értékelése magában foglalta a stroke (halálos vagy nem halálos) és a halál (bármilyen okból) halálának elemzését egy elvakult morbiditási és mortalitási csoportban. Az ESPS-2-ben lévő AGGRENOX 23,1% -kal csökkentette a stroke kockázatát az ASA 50 mg / nap-hoz képest (p = 0,006), és a stroke kockázatát 24,7% -kal csökkentette a felszabaduló dipiridamolhoz képest. Hosszabb 400 mg / nap önmagában (p = 0,002) ). Az AGGRENOX 37% -kal csökkentette a stroke kockázatát a placebóhoz képest (p
Az ESPS-2 vizsgálat eredményeit alátámasztja a European / Australasian Stroke Prevention in Reversible Ischaemia Trial (ESPRIT) vizsgálata, amely napi 400 mg dipiridamol kombinált kezelését vizsgálta (a betegek 83% -a hosszabbított dipiridamol) és 30-325 mg ASA naponta. Összesen 2739, artériás ischaemiás stroke -ban szenvedő beteget vontak be, 1376 -at az ASA önmagában, és 1363 -at az ASA plusz dipiridamol karba. A fő eredmény az összes érrendszeri halál, a nem halálos stroke, a nem halálos szívinfarktus vagy a súlyos vérzés szövődményeinek kombinációja volt. Az ASA plusz dipiridamol csoportba tartozó betegek 20% -os kockázatcsökkenést mutattak (p
A PRoFESS (PRevention Regimen For Effective to välttä Second Strokes) egy párhuzamos csoportú, randomizált, nemzetközi, kettős-vak, dupla-dummy, aktív-kontrollált és placebo-kontrollos vizsgálat, 2x2 faktoros felépítéssel, összehasonlítva az AGGRENOX-ot a klopidogréllel, és a telmizartánt a placebóval. a stroke megelőzésében azoknál a betegeknél, akik korábban átestek nem-kardioembóliás ischaemiás stroke-ban.
Összesen 20 332 beteget randomizáltak AGGRENOX (n = 10 181) vagy klopidogrél (n = 10 151) kezelésre. Az elsődleges végpont a stroke első megismétlődésének ideje volt.
Az elsődleges végpont előfordulási gyakorisága hasonló volt mindkét kezelési csoportban (9,0% az AGGRENOX és 8,8% a klopidogrél esetében; HR 1,01, 95% CI 0,92 - 1,11).Az AGGRENOX és a klopidogrél kezelési csoportok között nem találtak szignifikáns különbséget számos más, előre meghatározott végpont esetében, beleértve az ismétlődő stroke, a miokardiális infarktus vagy az érrendszeri halál okozta összetett végpontot (13,1% mindkét kezelési csoportban; HR 0,99, 95%) CI 0,92 - 1,07) és a visszatérő stroke vagy súlyos vérzéses esemény összetett végpontja (11,7% az AGGRENOX és 11,4% a klopidogrél esetében; HR 1,03, 95% CI 0,95 - 1,11).
A neurológiai funkcionális eredményeket 3 hónappal az ismétlődő stroke után a Modified Rankin-skála (mRS) alapján értékelték, és nem észleltek szignifikáns különbséget az mRS eloszlásban az AGGRENOX és a klopidogrél között (p = 0,3073 a Cochran-Armitage tesztből lineáris trend alapján).
A kísérleti adatok azt mutatják, hogy az ibuprofen gátolhatja az alacsony dózisú acetilszalicilsav vérlemezke-aggregációra gyakorolt hatását, ha a gyógyszereket egyidejűleg alkalmazzák. Egy vizsgálatban, egyetlen 400 mg-os ibuprofen adag beadását követően, 8 órán belül vagy 30 perccel azután acetilszalicilsav (81 mg) beadása esetén csökkent az acetilszalicilsav tromboxánképződésre és vérlemezke -aggregációra gyakorolt hatása. A korlátozott adatok és a klinikai helyzetben való alkalmazásukhoz kapcsolódó bizonytalanságok azonban nem teszik lehetővé végleges következtetések levonását az ibuprofen további alkalmazására vonatkozóan; úgy tűnik, nincs klinikailag releváns hatása az ibuprofen időnkénti alkalmazásának.
05.2 Farmakokinetikai tulajdonságok
Nincs szignifikáns kölcsönhatás a dipiridamol retardált pellet és az acetilszalicilsav között. Ezért az AGGRENOX farmakokinetikája összefügg a két komponens egyedi farmakokinetikájával.
Dipiridamol
(A legtöbb adat egészséges önkéntesekre vonatkozik).
Dózis - linearitás figyelhető meg a dipiridamollal a terápia során alkalmazott minden dózisban.
A dipiridamolt tartalmazó, módosított hatóanyag-leadású kapszulákat hosszú távú kezelésre fejlesztették ki. A dipiridamol pH-függő oldhatóságát, amely megakadályozza az oldódást az alsó gyomor-bél traktusban (ahol a nyújtott hatóanyag-leadású készítményeknek még nem kell felszabadítaniuk a hatóanyagot), borkősavval való társítással sikerült leküzdeni; a retard hatást diffúziós membránnal érjük el, amelyet a pelletre permetezünk.
Számos egyensúlyi állapotú kinetikai vizsgálat bizonyítja, hogy a módosított hatóanyag-leadású készítmény tulajdonságainak jellemzésére szolgáló minden megfelelő farmakokinetikai paraméter egyenértékű vagy némileg javult a módosított hatóanyagleadású dipiridamol kapszulák napi kétszeri adagolásával összehasonlítva a dipiridamollal naponta háromszor. A biohasznosulás valamivel magasabb, a csúcskoncentrációk hasonlóak, a downstream koncentrációk lényegesen magasabbak, és a csúcs / mélypont ingadozás kicsi.
Abszorpció
Az abszolút biohasznosulás körülbelül 70%. Mivel az első passzív hatás a beadott adag körülbelül 1/3 -át távolítja el, feltételezhető, hogy a dipiridamol felszívódása majdnem teljes az AGGRENOX beadása után.
A plazma csúcskoncentráció körülbelül 2-3 órával érhető el 400 mg AGGRENOX (200 mg naponta kétszer) beadása után. Az átlagos egyensúlyi csúcskoncentráció 1,98 mcg / ml (tartomány 1,01 - 3,99 mcg / ml), a legalacsonyabb koncentráció pedig 0,53 mcg / ml (0,18 - 1,01 mcg / ml).
Az ételnek nincs jelentős hatása a dipiridamol farmakokinetikájára az AGGRENOX -ban.
terjesztés
Magas lipofilitása miatt a log P 3,92 (n-oktanol / 0,1 n, NaOH), a dipiridamol sok szervben eloszlik. Állatokban a dipiridamol előnyösen a májban, majd a tüdőben, a vesében, a lépben és a szívben oszlik el.
Az intravénás adagolás során megfigyelt gyors eloszlási fázis nem látható orális adagolást követően.
A központi rekesz látszólagos eloszlási térfogata (Vc) körülbelül 5 l (hasonló a plazma térfogatához). A látszólagos eloszlási térfogat egyensúlyi állapotban körülbelül 100 l, és tükrözi a különböző rekeszek közötti eloszlást.
A gyógyszer nem lép át jelentős mértékben a vér -agy gáton.
A dipiridamol placentáris transzferje nagyon alacsony. Egy nőnél a plazmakoncentráció körülbelül tizenhetedike volt kimutatható az anyatejben.
A dipiridamol fehérjékhez való kötődése megközelítőleg 97-99%, és főként alfa -1 savas glikoprotein és albumin esetén fordul elő.
Biotranszformáció
A dipiridamol metabolizmusa a májban történik. A dipiridamol elsősorban glükuronsavval való konjugáció útján metabolizálódik, és főként monoglikuronidot és csak kis mennyiségű diglikuronidot képez. A plazmában a teljes mennyiség körülbelül 80% -a az eredeti vegyületből áll, és a teljes mennyiség 20% -a monoglikuronidból áll .
A dipiridamol glükuronidjainak farmakodinamikai aktivitása lényegesen alacsonyabb, mint a dipiridamolé.
Kiküszöbölés
A domináns felezési idő szájon át történő beadást követően körülbelül 40 perc, valamint az intravénás beadás után.
Az anyavegyület renális kiválasztása elhanyagolható (az ürülék epével, az enterohepatikus recirkuláció némi nyomával).
A teljes clearance megközelítőleg 250 ml / perc, az átlagos tartózkodási idő pedig körülbelül 11 óra (az átlagos tartózkodási idő kb. 6,4 óra és az átlagos felszívódási idő 4,6 óra).
Az intravénás adagoláshoz hasonlóan meghosszabbított, körülbelül 13 órás végső eliminációs felezési időt figyeltek meg.
Ez a végső eliminációs fázis viszonylag csekély jelentőséggel bír, mivel a teljes AUC kis részét képviseli, ezt bizonyítja az a tény, hogy az egyensúlyi állapot két napon belül, két módosított hatóanyag-leadású kapszula adagolásával érhető el.
Az ismételt adagolást követően nem volt jelentős gyógyszerfelhalmozódás.
Kinetika időseknél
Az idősek (> 65 év) plazmakoncentrációja (AUC -ként meghatározva) körülbelül 50% -kal magasabb volt a tablettákkal történő kezelés után, és körülbelül 30% -kal magasabb az AGGRENOX -kezelést követően, mint a fiatalabb alanyokban (
Hasonló plazmakoncentráció-növekedést idős betegeknél figyeltek meg a Persantin, módosított hatóanyag-leadású kapszulák, valamint az AGGRENOX ESPS-2 vizsgálatában.
Kinetika vesekárosodásban szenvedő betegeknél
Mivel a vesék kiválasztódása nagyon alacsony (5%), veseelégtelenség esetén nem várható változás a farmakokinetikában. Az ESPS-2 vizsgálatban olyan betegeknél, akiknél a kreatinin-clearance 15 ml / perc és> 100 ml / perc között volt, nem változik a dipiridamol vagy metabolikus glükuronidjának farmakokinetikája, ha az adatokat korkülönbséggel korrigálják.
Kinetika májkárosodásban szenvedő betegeknél
A májelégtelenségben szenvedő betegek nem mutatnak változást a dipiridamol plazmakoncentrációjában, hanem a glükuronidok növekedését (farmakodinamikailag inaktív). Javasolt a dipiridamol korlátozás nélküli adagolása, amennyiben nincs klinikai bizonyíték a májelégtelenségre.
Acetilszalicilsav
Abszorpció
Orális adagolás után az acetilszalicilsav gyorsan és teljesen felszívódik a gyomorban és a belekben. Az acetilszalicilsav adagjának körülbelül 30% -a előzetesen szisztematikusan hidrolizálódik szalicilsavvá.
A maximális plazmakoncentráció az AGGRENOX 50 mg acetilszalicilsav adagja után (25 mg naponta kétszer beadva) minden egyes adag után 30 perc elteltével érhető el, és a csúcskoncentráció egyensúlyi állapotban körülbelül 360 ng / ml. Acetilszalicilsav esetén. A szalicilsav plazmakoncentrációja 60-90 perc múlva érhető el, és körülbelül 1100 ng / ml.
Az élelmiszer nem gyakorol jelentős hatást az AGGRENOX -ban lévő acetilszalicilsav farmakodinamikájára.
terjesztés
Az acetilszalicilsav gyorsan szaliciláttá alakul, de a gyógyszer elsődleges formája a plazmában az orális beadást követő első 20 percben.
Az acetilszalicilsav plazmakoncentrációja gyorsan csökken, felezési ideje körülbelül 15 perc, fő metabolitja, a szalicilsav erősen kötődik a plazmafehérjékhez, és kötődése koncentrációfüggő (nem lineáris). Alacsony koncentrációban (központi idegrendszer, anyatej és magzati szövetek).
Biotranszformáció
Az acetilszalicilsavat a nem specifikus észterázok gyorsan metabolizálják szalicilsavvá.
A szalicilsav metabolizálódik szalicilsavsavvá, szalicil-fenol-glükuroniddá, acil-szalicilsav-glükuroniddá, és kisebb mértékben géniuszi-savsá és gentisurinsavvá. A fő metabolitok, a szalicil-kénsav és a szalicil-fenol-glükuronid képződése könnyen telíthető, és a Michaelis-t követi -Menten kinetika; a többi anyagcsereút elsőrendű folyamat.
Kiküszöbölés
Az acetilszalicilsav eliminációs felezési ideje 15-20 perc a plazmában; a fő metabolit, a szalicilsav eliminációs felezési ideje 2-3 óra kis dózisok esetén (pl. 325 mg), amely magasabb dózisok esetén 30 órára nőhet az anyagcsere nemlinearitása és a plazmafehérjékhez való kötődése miatt.
Az acetilszalicilsav több mint 90% -a metabolitok formájában eliminálódik a vesén keresztül.
A változatlan formában eliminált szalicilsav aránya a vizeletben növekszik az adag növelésével, és a teljes szalicilát renális clearance -e is nő a vizelet pH -értékének növekedésével.
Kinetika vesekárosodásban szenvedő betegeknél
Súlyos veseelégtelenségben (glomeruláris szűrési sebesség kevesebb, mint 10 ml / perc) szenvedő betegeknél kerülni kell az acetilszalicilsav adását.
Beszámoltak a teljes plazmakoncentráció és a szalicilsav nem kötődő frakciójának növekedéséről.
Kinetika májkárosodásban szenvedő betegeknél
Súlyos májelégtelenségben szenvedő betegeknél kerülni kell az acetilszalicilsav adását. A szalicilsav nem kötött frakciójának növekedéséről számoltak be.
05.3 A preklinikai biztonságossági adatok
A dipiridamol és az acetilszalicilsav kombináció orális beadását követő egyszeri dózisú toxicitási vizsgálatokban az akut toxicitást több gramm / kg rágcsálóknál és 900 mg / kg kutyáknál észlelték.
Ez megfelelt a keverékben lévő acetilszalicilsav mennyiségének. A dipiridamol mennyisége nem talált semmilyen további vagy szinergista hatást, függetlenül a tényleges aránytól (dipiridamol: acetilszalicilsav = 1: 0,125 vagy 1: 4 és 1: 6). A szív- és érrendszeri elégtelenséget halál okának tekintik.
Ismételt dózisú toxicitási vizsgálatokban dipiridamol: acetilszalicilsav 1: 4 és 1: 5 arányban, legfeljebb 6 hónapig, legfeljebb 400 mg / kg -ot adtak patkányoknak és kutyáknak. A patkányok tolerálták ezeket az adagokat, nyilvánvaló mérgezési jelek nélkül.
A 200 mg / ttkg feletti dózisok mérgezőek a kutyák számára, emésztőrendszeri elváltozásokat okozva, 320 mg / kg acetilszalicilsav részarány, valamint szívizom- és endokardiális rendellenességek, valamint 40 mg / kg dipiridamol által okozott vesegyulladás következtében. . Hasonló változásokat találtak az egyes komponenseknél is hasonló dózisokban. Ezért elmondható, hogy a kombináció nem mutatott semmilyen további vagy fokozott toxikus hatásra utaló jelet.
Teratogenitási vizsgálatokat végeztek patkányokon és nyulakon az anyai toxicitásig terjedő dózisokban, dipiridamol: acetilszalicilsav 1: 5,4 arányban. A maximális dózissal kezelt csoporttal párhuzamosan egy másik csoportot csak aszpirinnel kezeltek, a megfelelő dózisban. Másodlagosan az anyasági toxicitáshoz kapcsolódó nagy dózisok mellett (405 mg / kg patkányokban, 135 mg / kg nyulakban), magasabb felszívódási arányt értek el, patkányokban elérve a 100% -ot, és csökkentették az utódok súlyát. A rendellenességeket csak az acetilszalicilsavval kezelt csoportokban figyelték meg, de a dipiridamollal / acetilszalicilsavval kezelt csoportokban nem.
Termékenységi vizsgálatokat és perinatális időszakra vonatkozó vizsgálatokat csak az egyes komponensekkel végeztek. A termékenység károsodását nem találták. Mivel az acetilszalicilsav ismert hatásai előrehaladott terhességben, a dipiridamol és az acetilszalicilsav kombinációjával történő kezelés csak akkor javasolt, ha ez valós prioritás.
A kezelés ezzel a kombinációval különösen ellenjavallt a terhesség utolsó trimeszterében.
A mutagenitás alapos szűrése in vitro és in vivo vizsgálatokban nem mutatott jeleket a mutagenitás kockázatára.
A rákkeltő hatást patkányokban és egerekben vizsgálták 450 mg / kg maximális dózisban, ami 75 mg / kg dipiridamolnak és 375 mg / kg acetilszalicilsavnak felel meg. Nem mutattak rákkeltő hatást.
06.0 GYÓGYSZERÉSZETI INFORMÁCIÓK
06.1 Segédanyagok
Borkősav, povidon, metakrilsav-metil-metakrilát kopolimer (1: 2), talkum, arab gumi, hipromellóz-ftalát, hipromellóz, triacetin, dimetikon 350, sztearinsav / palmitinsav, laktóz-monohidrát, alumínium-sztearát, kolloid szilícium-dioxid, kukoricakeményítő cellulóz, szacharóz, E 171; kapszula (kemény): zselatin, E 171, E 172, tisztított víz.
06.2 Inkompatibilitás
Más gyógyszerekkel való összeférhetetlenség nem ismert.
06.3 Érvényességi idő
3 év.
06.4 Különleges tárolási előírások
Tárolja 30 ° C alatt, tartsa zárva az üveget a nedvességtől való védelem érdekében.
06.5 A közvetlen csomagolás jellege és a csomagolás tartalma
Átlátszatlan fehér polipropilén palack gyermekbiztos polietilénnel és polipropilén csavaros kupakkal.
06.6 Használati utasítás
Nincsenek speciális utasítások.
07.0 FORGALOMBA HOZATALI ENGEDÉLY
BOEHRINGER INGELHEIM ITALIA S.p.A.
Via Lorenzini, 8
20139 Milánó
08.0 A FORGALOMBA HOZATALI ENGEDÉLY SZÁMA
50 kapszula A.I.C. n. 033181037
60 kapszula A.I.C. n. 033181049
09.0 Az első forgalomba hozatali engedély kiadásának időpontja
01.10.2001/01.10.2006
10.0 A SZÖVEG FELÜLVIZSGÁLÁSÁNAK DÁTUMA
2015. július 14