Hatóanyagok: Bilasztin
ROBILAS 20 mg TABLETTA
Miért használják a Robilas -t? Mire való?
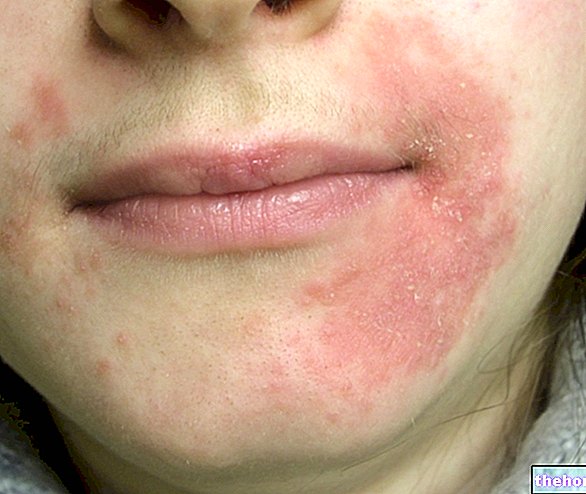
A ROBILAS tabletta bilasztin hatóanyagot tartalmaz, amely antihisztamin. A ROBILAS 20 mg tabletta a szénanátha (tüsszentés, viszketés, orrfolyás, orrdugulás, vörös és könnyes szem) és más allergiás nátha tüneteinek enyhítésére szolgál. Viszkető bőrkiütések (például csalánkiütés) kezelésére is alkalmazható.
Ellenjavallatok Mikor nem szabad Robilas -t használni
Ne szedje a ROBILAS 20 mg tablettát, ha:
ha allergiás (túlérzékeny) a bilasztinra vagy a ROBILAS 20 mg tabletta egyéb összetevőjére
Az alkalmazással kapcsolatos óvintézkedések Mit kell tudnia a Robilas szedése előtt
A ROBILAS 20 mg tabletta fokozott elővigyázatossággal alkalmazható
Ha mérsékelt vagy súlyos vesekárosodása van, és más gyógyszereket szed (lásd alább)
Nem alkalmazható 12 év alatti gyermekeknél
Ne lépje túl az ajánlott adagot. Ha a tünetek továbbra is fennállnak, forduljon orvosához.
Kölcsönhatások Mely gyógyszerek vagy élelmiszerek módosíthatják a Robilas hatását
Feltétlenül tájékoztassa kezelőorvosát vagy gyógyszerészét a jelenleg vagy nemrégiben szedett egyéb gyógyszereiről, beleértve a vény nélkül kapható készítményeket is. Különösen konzultáljon orvosával, ha az alábbi gyógyszerek bármelyikét szedi:
- Ketokonazol (gombaellenes gyógyszer)
- Eritromicin (antibiotikum)
- Diltiazem (angina kezelésére)
- Ciklosporin (az immunrendszer aktivitásának csökkentésére a transzplantátum kilökődésének elkerülése érdekében, vagy az autoimmun és allergiás betegségek, például pikkelysömör, atópiás dermatitis vagy reumatoid arthritis aktivitásának csökkentésére)
- Ritonavir (AIDS kezelésére)
- Rifampicin (antibiotikum)
A ROBILAS 20 mg tabletta egyidejű bevétele étellel és itallal
A tablettákat nem szabad étellel vagy grapefruitlével vagy más gyümölcslevekkel együtt bevenni, mivel ez csökkenti a bilasztin hatását. Ennek elkerülése érdekében tegye a következőket:
- vegye be a tablettát, és várjon egy órát, mielőtt bármilyen ételt vagy gyümölcslevet fogyaszt
- ha ételt vagy gyümölcslevet fogyasztott, várjon két órát a tabletta bevétele előtt
Figyelmeztetések Fontos tudni, hogy:
Terhesség és szoptatás
Forduljon orvosához, ha terhes, ha terhes lehet, vagy ha szoptat. Mielőtt bármilyen gyógyszert elkezdene szedni, kérjen tanácsot orvosától vagy gyógyszerészétől.
A készítmény hatásai a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre
A bilasztin gépjárművezetési képességre gyakorolt hatásának megállapítására végzett tanulmány kimutatta, hogy a 20 mg bilasztin dózisokkal történő kezelés nem befolyásolja a gépjárművezetéshez szükséges képességeket. Azonban nagyon ritkán néhány embernél tapasztaltak aluszékonyságot, ami befolyásolhatja a gépjárművezetéshez és gépek kezeléséhez szükséges képességeket.
Alkoholfogyasztás
A bilasztin az ajánlott adagban (20 mg) nem növeli az alkohol által okozott álmosságot.
Adagolás, az alkalmazás módja és ideje A Robilas használata: Adagolás
Felnőttek, beleértve az időseket és a 12 éves vagy idősebb serdülőket
- Vegyen be egy tablettát naponta.
- A tablettát éhgyomorra kell bevenni, például reggel, reggeli előtt. A bilasztin bevétele után 1 órán keresztül ne egyen.
- A tablettát egy pohár vízzel nyelje le.
- A bemetszésvonalat nem használják a tabletta egyenlő adagokra osztására. A tabletta törésére és megkönnyítésére használható.
A kezelés időtartamát illetően orvosa meghatározza, hogy milyen betegségben szenved, és eldönti, mennyi ideig kell szednie a ROBILAS 20 mg tablettát.
Túladagolás Mi a teendő, ha túl sok Robilas -t vett be?
Ha az előírtnál több ROBILAS 20 mg tablettát vett be
Ha Ön vagy valaki más túl sok ROBILAS 20 mg tablettát vett be, azonnal forduljon orvosához vagy gyógyszerészéhez.
Ha elfelejtette bevenni a ROBILAS 20 mg tablettát
Ne vegyen be kétszeres adagot a kihagyott adag pótlására.
Ha elfelejtett bevenni egy adagot, vegye be a lehető leghamarabb, majd térjen vissza a szokásos adagolási rendhez.
Ha bármilyen további kérdése van a ROBILAS 20 mg tabletta alkalmazásával kapcsolatban, kérdezze meg kezelőorvosát vagy gyógyszerészét.
Mellékhatások Mik a Robilas mellékhatásai?
Mint minden gyógyszer, így a ROBILAS 20 mg tabletta is okozhat mellékhatásokat, amelyek azonban nem mindenkinél jelentkeznek.
A lehetséges mellékhatások a következők:
Gyakori: 100 -ból 1-10 beteget érint
fejfájás
álmosság
Nem gyakori: 1000 -ből 1-10 beteget érint
- kóros elektrokardiográfiás nyom (EKG)
- vérvizsgálatok, amelyek a máj működésének megváltozását jelzik
- szédülés
- gyomorfájdalmak
- fáradtság
- fokozott étvágy
- szabálytalan szívverés
- súlygyarapodás
- hányinger (hányinger)
- szorongás
- szárazság vagy kellemetlen érzés az orrban
- hasfájás
- hasmenés
- gastritis (a gyomor falának gyulladása)
- szédülés (szédülés)
- gyengeség érzése
- szomjúság
- nehézlégzés (nehézlégzés)
- száraz száj
- emésztési zavar
- viszket
- orális herpesz
- láz
- tinnitus (csengés a fülben)
- elalvási nehézség
- vérvizsgálatok, amelyek a veseműködés megváltozását jelzik
- megnövekedett zsír a vérben
Ha bármely mellékhatás súlyossá válik, vagy ha a betegtájékoztatóban felsorolt mellékhatásokon kívül egyéb tünetet észlel, kérjük, értesítse orvosát vagy gyógyszerészét.
Lejárat és megőrzés
Gyermekektől elzárva tartandó!
A dobozon és a buborékcsomagoláson feltüntetett lejárati időn túl ne alkalmazza a ROBILAS 20 mg tablettát. A lejárati idő az adott hónap utolsó napjára vonatkozik.
Ez a gyógyszer nem igényel különleges tárolási körülményeket.
A gyógyszereket nem szabad a szennyvízzel vagy a háztartási hulladékkal együtt megsemmisíteni. Kérdezze meg gyógyszerészét, hogy mit tegyen a már nem használt gyógyszereivel. Ez elősegíti a környezet védelmét.
Mit tartalmaz a ROBILAS 20 mg tabletta?
- A készítmény hatóanyaga a bilasztin. 20 mg bilasztint tartalmaz tablettánként.
- Egyéb összetevők: mikrokristályos cellulóz, A típusú nátrium -keményítő -glikolát (burgonyából származó), vízmentes kolloid szilícium -dioxid, magnézium -sztearát.
Milyen a ROBILAS 20 mg tabletta külleme és mit tartalmaz a csomagolás:
A ROBILAS 20 mg tabletta fehér, ovális, mindkét oldalán domború és metszett.
A tablettákat 10, 20, 30, 40 vagy 50 tablettát tartalmazó buborékcsomagolásban szállítjuk.
Nem feltétlenül mindegyik kiszerelés kerül kereskedelmi forgalomba.
Forrás betegtájékoztató: AIFA (Olasz Gyógyszerügynökség). A tartalom 2016 januárjában jelent meg. A jelenlévő információk nem feltétlenül naprakészek.
A legfrissebb verzióhoz való hozzáféréshez ajánlatos az AIFA (Olasz Gyógyszerügynökség) webhelyét elérni. Jogi nyilatkozat és hasznos információk.
01.0 A GYÓGYSZER MEGNEVEZÉSE
ROBILAS 20 MG TABLETTA
02.0 MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL
20 mg bilasztint tartalmaz tablettánként.
A segédanyagok teljes listáját lásd a 6.1 pontban.
03.0 GYÓGYSZERFORMA
Tabletta.
Fehér, ovális, mindkét oldalán domború tabletta, bemetszéssel.
A tabletta bemetszése csak a törés megkönnyítésére szolgál, hogy könnyebben lenyelje a tablettát e Nem hogy egyenlő adagokra ossza.
04.0 KLINIKAI INFORMÁCIÓK
04.1 Terápiás javallatok
Az allergiás rhinoconjunctivitis (szezonális és évelő) és csalánkiütés tüneti kezelése.
04.2 Adagolás és alkalmazás
Az alkalmazás módja: szájon át történő alkalmazásra.
Felnőttek és serdülők (12 év felett)
20 mg (1 tabletta) naponta egyszer az allergiás rhinoconjunctivitis (SAR és PAR) és csalánkiütés tüneteinek enyhítésére.
A tablettát szájon át kell bevenni egy órával étkezés vagy gyümölcslé előtt vagy két órával azután. A napi adagot egyetlen adagban kell bevenni.
Idős államporgárok
Idős betegeknél nincs szükség az adag módosítására (lásd 5.1 és 5.2 pont). A 65 év feletti betegeknél a tapasztalat gyenge.
12 év alatti gyermekek
A bilasztin biztonságosságát és hatásosságát 12 év alatti gyermekeknél még nem igazolták.
Vesekárosodás
Vesekárosodásban szenvedő betegeknél nincs szükség az adag módosítására. (lásd 5.2 pont).
Májkárosodás
Nincs klinikai tapasztalat májkárosodásban szenvedő betegeknél. Mivel a bilasztin nem metabolizálódik, és a vese clearance a fő eliminációs útvonal, a májkárosodás várhatóan nem növeli a szisztémás expozíciót a biztonsági határon túl. Ezért májkárosodásban szenvedő betegeknél nincs szükség az adag módosítására (lásd 5.2 pont).
A kezelés időtartama
Allergiás nátha esetén a kezelést az allergéneknek való kitettség időszakára kell korlátozni. Szezonális allergiás nátha esetén a kezelést a tünetek eltűnése után le lehet állítani, és újbóli megjelenésük után folytatni kell. Az évelő allergiás nátha esetén a kezelést az allergénekkel való érintkezés idején is folytathatják a betegek. Urticaria esetén a kezelés időtartama a panaszok típusától, időtartamától és lefolyásától függ.
04.3 Ellenjavallatok
Túlérzékenység a bilasztin hatóanyaggal vagy bármely segédanyaggal szemben.
04.4 Különleges figyelmeztetések és a használathoz szükséges óvintézkedések
A bilasztin biztonságosságát és hatásosságát 12 év alatti gyermekeknél nem igazolták.
Mérsékelt vagy súlyos vesekárosodásban szenvedő betegeknél a bilasztin P-glikoprotein inhibitorokkal, például ketokonazollal, eritromicinnel, ciklosporinnal, ritonavirrel vagy diltiazemmel történő együttes alkalmazása növelheti a bilasztin plazmaszintjét, és ezáltal növelheti a káros hatások kockázatát. Ezért kerülni kell a bilasztin és a P-glikoprotein inhibitorok együttes alkalmazását közepesen súlyos vagy súlyos vesekárosodásban szenvedő betegeknél.
04.5 Kölcsönhatások más gyógyszerekkel és más interakciók
Kölcsönhatás az étellel
Az étel jelentősen csökkenti a bilasztin orális biohasznosulását 30%-kal.
Kölcsönhatás a grapefruitlével
A 20 mg bilasztin és a grapefruitlé egyidejű bevétele 30%-kal csökkenti a bilasztin biohasznosulását. Ez a hatás más gyümölcsleveknél is előfordulhat. A biológiai hozzáférhetőség csökkenésének mértéke a termelőktől és a gyümölcsöktől függően eltérő lehet. Ennek az interakciónak a mechanizmusa " gátolja az "OATP1A2, felvételi transzporter, amelynek szubsztrátja a bilasztin (lásd 5.2 pont). Az OATP1A2 szubsztrátjai vagy gátlói, például a ritonavir vagy a rifampicin, hasonló módon csökkenthetik a bilasztin plazmakoncentrációját.
Kölcsönhatás ketokonazollal vagy eritromicinnel
A bilasztin és a ketokonazol vagy az eritromicin egyidejű bevitele kétszeresére növelte a bilasztin AUC-értékét, és kétszeresére emelte a Cmax értékét. Ezeket a változásokat a bélkiáramlás transzportereivel való kölcsönhatás magyarázhatja, mivel a bilasztin a P-gp szubsztrátja, és nem metabolizálódik (lásd 5.2 pont). Úgy tűnik, hogy ezek a változások nem befolyásolják a bilasztin és a ketokonazol, vagy az eritromicin biztonsági profilját. illetve más gyógyszerek, amelyek a P-gp szubsztrátjai vagy gátlói, mint például a ciklosporin, hasonlóképpen növelhetik a bilasztin plazmakoncentrációját.
Kölcsönhatás diltiazemmel
A 20 mg bilasztin és a 60 mg diltiazem egyidejű bevétele 50%-kal növelte a bilasztin Cmax értékét. Ez a hatás a bélkiáramlás transzportereivel való kölcsönhatással magyarázható (lásd 5.2 pont), és úgy tűnik, hogy nem befolyásolja a bilasztin biztonsági profilját.
Kölcsönhatás az alkohollal
Az alkohol és a 20 mg bilasztin egyidejű bevétele után a pszichomotoros teljesítmény hasonló volt, mint az alkohol és a placebo bevétele után.
Kölcsönhatás lorazepámmal
A 20 mg bilasztin és a 3 mg lorazepám 8 napon keresztül történő együttes alkalmazása nem erősítette a lorazepám központi idegrendszeri nyugtató hatását.
04.6 Terhesség és szoptatás
Termékenység
Nincsenek klinikai adatok, vagy azok száma korlátozott. Patkányokon végzett vizsgálat nem mutatott semmilyen káros hatást a termékenységre (lásd 5.3 pont).
Terhesség
A bilasztin terhes nőkön történő alkalmazására vonatkozó adatok nem állnak rendelkezésre, vagy csak korlátozott számban állnak rendelkezésre.
Az állatkísérletek nem utalnak közvetlen vagy közvetett káros hatások jelenlétére a reprodukciós toxicitás, a szülés vagy a születés utáni fejlődés tekintetében (lásd 5.3 pont). Elővigyázatosságból célszerű kerülni a Robilas használatát terhesség alatt.
Etetési idő
Nem ismert, hogy a bilasztin kiválasztódik -e az anyatejbe. A bilasztin anyatejbe történő kiválasztódását állatokon nem vizsgálták. El kell dönteni, hogy folytatják / abbahagyják a szoptatást, vagy folytatják / abbahagyják a Robilas -kezelést, figyelembe véve a szoptatás előnyét a gyermekre és a bilasztin -kezelés előnyeit. az anyának.
04.7 Hatások a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre
A bilasztin gépjárművezetési képességre gyakorolt hatásának értékelésére végzett tanulmány kimutatta, hogy a 20 mg -os kezelés nem befolyásolja a gépjárművezetéshez szükséges képességeket. Figyelmeztetni kell azonban a betegeket, hogy egyes embereknél nagyon ritkán jelentkezett aluszékonyság, ami befolyásolhatja a gépjárművezetéshez és gépek kezeléséhez szükséges képességeket.
04.8 Nemkívánatos hatások
A klinikai vizsgálatokban 20 mg bilasztinnal kezelt, allergiás rhinoconjunctivitisben vagy krónikus idiopátiás csalánkiütésben szenvedő betegeknél előforduló mellékhatások száma hasonló volt a placebóval kezelt betegekhez (12,7%, szemben a 12,8% -kal).
A II. És III. Fázisú klinikai vizsgálatok során 20 mg bilasztint kapó betegek leggyakrabban jelentett mellékhatásai a fejfájás, aluszékonyság, szédülés és fáradtság voltak. Ezek a mellékhatások hasonló gyakorisággal fordultak elő placebóval kezelt betegeknél.
Az alábbi táblázat tartalmazza azokat a nemkívánatos eseményeket, amelyek legalább a bilasztinnal kapcsolatosak és a klinikai fejlődés során 20 mg bilasztinnal kezelt betegek több mint 0,1% -ánál jelentettek.
A frekvenciákat a következőképpen osztják ki:
• nagyon gyakori (≥1 / 10)
• gyakori (≥1 / 100 -
• nem gyakori (≥1 / 1000 -
• ritka (≥1 / 10 000 -
• nagyon ritka (
• nem ismert (a gyakoriság a rendelkezésre álló adatokból nem becsülhető meg)
Ritka, nagyon ritka és ismeretlen gyakoriságú táblázat nem szerepelt.
04.9 Túladagolás
Az akut túladagolással kapcsolatos információk a bilasztin kifejlesztése során végzett klinikai vizsgálatok során gyűjtött tapasztalatokra korlátozódnak. Miután a bilasztint a terápiás dózis (220 mg (egyszeri adag) vagy 200 mg / nap 7 napon keresztül) nagyobb dózisaiban (220 mg (egyszeri adag) vagy 200 mg / nap 7 napon át) magasabb dózisokban adták be egészséges önkénteseknek, a kezelés során előforduló mellékhatások gyakorisága kétszer nagyobb volt, mint placebo. A leggyakrabban jelentett mellékhatások szédülés, fejfájás és hányinger voltak. Súlyos mellékhatásokról és jelentős QTc -megnyúlásról nem számoltak be.
A többszörös bilasztin (100 mg x 4 nap) dózisnak a kamrai repolarizációra gyakorolt hatásának kritikus értékelése "alapos QT / QTc keresztvizsgálat" segítségével, 30 egészséges önkéntes bevonásával nem mutatott ki jelentős QTc-megnyúlást.
Túladagolás esetén tüneti és támogató kezelés javasolt.
A bilasztinnak nincs ismert ellenszere.
05.0 FARMAKOLÓGIAI TULAJDONSÁGOK
05.1 Farmakodinámiás tulajdonságok
Farmakoterápiás csoport: antihisztaminok szisztémás használatra, egyéb antihisztaminok szisztémás alkalmazásra
ATC kód: RO6AX29.
A bilasztin egy hosszú hatású, nem nyugtató hisztaminerg antagonista, amely szelektív perifériás H1-receptor antagonista affinitással rendelkezik, és nincs affinitása a muszkarin receptorokhoz.
A bilasztin egyszeri adag beadását követően 24 órán keresztül gátolta a hisztamin által kiváltott bőrkiütéseket.
A felnőtt és serdülőkorú (szezonális és évelő) rhinoconjunctivitisben szenvedő felnőtt és serdülő betegeknél végzett klinikai vizsgálatok során a 20 mg bilasztin, amelyet naponta egyszer 14-28 napig adtak, hatékonyan enyhítette a tüneteket, például a tüsszentést, az orr kellemetlen érzését, az orrviszketést, az orrdugulást, viszkető szemek, könnyes szemek és vörös szemek A bilasztin 24 órán keresztül hatékonyan szabályozta a tüneteket.
Két klinikai vizsgálatban, amelyeket krónikus idiopátiás csalánkiütésben szenvedő betegeknél végeztek, a 20 mg bilasztin, naponta egyszer, 28 napon keresztül, hatékonyan enyhítette a viszketés intenzitását és a csalánkiütések számát és méretét, valamint a csalánkiütés okozta rendellenességeket. a betegek állapota és életminősége javult.
A bilasztinnal végzett klinikai vizsgálatok során nem figyelték meg a QTc-intervallum klinikailag releváns meghosszabbodását vagy bármely más szív- és érrendszeri hatást, még napi 200 mg-os dózisok (a klinikai dózis tízszerese) esetén sem, 7 napon keresztül 9 alanyban, vagy még akkor sem, ha P-gp inhibitorok, például ketokonazol (24 alany) és eritromicin (24 alany) Ezenkívül alapos QT-vizsgálatot végeztek 30 önkéntesen.
Az ajánlott napi egyszeri 20 mg -os dózisban végzett kontrollos klinikai vizsgálatokban a bilasztin központi idegrendszeri biztonsági profilja hasonló volt a placebóhoz, és az aluszékonyság előfordulási gyakorisága nem különbözött statisztikailag a placebótól. A napi 40 mg -os dilasztin nem befolyásolta a pszichomotoros teljesítményt klinikai vizsgálatok során, és nem befolyásolta a vezetési képességet a szokásos vezetési vizsgán.
A II. És III. Fázisú vizsgálatokba bevont idős betegeknél (≥ 65 évesek) nem volt különbség a hatásosságban vagy a biztonságban a fiatalabb betegekhez képest.
05.2 Farmakokinetikai tulajdonságok
Abszorpció
A bilasztin szájon át történő alkalmazás után gyorsan felszívódik, és körülbelül 1,3 óra alatt éri el a maximális plazmakoncentrációt. Felhalmozódási jelenséget nem figyeltek meg. A bilasztin átlagos biohasznosulása szájon át történő beadás után 61%.
terjesztés
Oktatás in vitro És in vivo kimutatta, hogy a bilasztin a Pgp szubsztrátja (lásd 4.5 pont, A ketokonazollal, az eritromicinnel és a diltiazemmel való kölcsönhatás) és az OATP (lásd 4.5 pont A kölcsönhatás a grapefruitlével). Úgy tűnik, hogy a bilasztin nem a BCRP transzporter vagy az OCT2, OAT1 és OAT3 vese transzporterek szubsztrátja. Tanulmányok alapján in vitro, a bilasztin várhatóan nem gátolja a következő transzportereket a szisztémás keringésben: P-gp, MRP2, BCRP, BSEP, OATP1B1, OATP1B3, OATP2B1, OAT1, OAT3, OCT1, OCT2 és NTCP, mivel csak mérsékelt gátlást észleltek a P- gp, OATP2B1 és OCT1, becsült IC50 ≥ 300 mcM, jóval magasabb, mint a számított klinikai plazma Cmax, ezért ezek az interakciók nem lesznek klinikailag relevánsak. Ezen eredmények alapján azonban nem zárható ki a bilasztin gátló hatása a bélnyálkahártyában jelen lévő transzporterekre, például a P-gp-re.
Terápiás dózisokban a bilasztin 84-90% -ban kötődik a plazmafehérjékhez.
Biotranszformáció
A bilasztin a vizsgálatok során nem indukálta vagy gátolta a CYP450 izoenzimek aktivitását in vitro.
Kiküszöbölés
Egy egészséges önkénteseken végzett tömegegyensúly-vizsgálatban, egyetlen 20 mg-os 14C-bilasztin adag beadását követően, a beadott adag közel 95%-a a vizeletből (28,3%) és a székletből (66,5%) maradt változatlan bilasztin formájában, így megerősítve, hogy a bilasztin nem metabolizálódik szignifikánsan az emberekben Az egészséges önkéntesek számított átlagos eliminációs felezési ideje 14,5 óra.
Linearitás
A bilasztin lineáris farmakokinetikát mutat a vizsgált dózistartományban (5-220 mg), alacsony egyének közötti variabilitással.
Vesekárosodásban szenvedő betegek
Egy vesekárosodásban szenvedő alanyokban végzett vizsgálatban az átlagos (SD) AUC0-∞ 737,4 (± 260,8) ngxh / ml-ről emelkedett károsodás nélkül (GFR:> 80 ml / perc / 1,73 m2) 967,4 (± 140,2) ngxh / ml enyhén károsodott személyeknél (GFR: 50-80 ml / perc / 1,73 m2), 1384,2 (± 263,23) ngxh / ml mérsékelt károsodásban (GFR: 30-2) és 1708,5 (± 699,0) ngxh / ml súlyosan károsodott alanyokban (GFR: 2). A bilasztin átlagos (SD) felezési ideje 9,3 óra (± 2,8) volt károsodás nélkül, 15,1 óra (± 7,7) enyhe károsodásban szenvedő betegeknél, 10,5 óra (± 2.3) közepesen károsodott alanyoknál és 18,4 óra (± 11,4) súlyos károsodásban szenvedő betegeknél. A bilasztin vizelettel történő kiválasztása lényegében teljes volt 48-72 óra elteltével minden alanynál. Ezeknek a farmakokinetikai változásoknak várhatóan nincs klinikailag jelentős hatása a bilasztin biztonságosságára, mivel a vesekárosodásban szenvedő betegek plazma bilasztinszintje még mindig a biztonságos tartományban van bilasztinból.
Májkárosodásban szenvedő betegek
Nincsenek farmakokinetikai adatok májkárosodásban szenvedő betegekről. A bilasztin nem metabolizálódik emberben. Mivel a vesekárosodási vizsgálat eredményei azt mutatják, hogy a vesén keresztül történő elimináció járul hozzá főként az eliminációhoz, az epével történő kiválasztás várhatóan csak csekély mértékben vesz részt a bilasztin eliminációjában. A májfunkció megváltozása várhatóan nem gyakorol klinikailag jelentős hatást a bilasztin farmakokinetikájára.
Idős betegek
A 65 év feletti alanyokról csak korlátozott mennyiségű adat áll rendelkezésre. Idősek és fiatalok között nem figyeltek meg statisztikailag szignifikáns különbségeket a bilasztin farmakokinetikájában.
05.3 A preklinikai biztonságossági adatok
A bilasztinnal kapcsolatos, nem klinikai adatok a hagyományos farmakológiai biztonságossági, ismételt dózistoxicitási, genotoxicitási és karcinogén potenciális vizsgálatok alapján nem mutatnak különleges veszélyt az emberre.
A reprodukciós toxicitási vizsgálatokban a bilasztin magzatra gyakorolt hatását (a beültetés előtti és utáni veszteség patkányokban, valamint a koponyacsontok, a szegycsont és a végtagok hiányos csontosodása nyulakban) csak anyai toxikus dózisok esetén figyelték meg. A megfigyelt mellékhatásmentes szint (NOAEL) expozíciós szintje az ajánlott terápiás dózisnál kellően meghaladja (> 30-szor) az emberi expozíciót.
Patkányokon végzett termékenységi vizsgálatban az orálisan 1000 mg / kg / nap dózisban adott bilasztin nem volt hatással a hím és nőstény reproduktív szervekre. A párzási, termékenységi és terhességi mutatókat nem érintette.
Amint azt egy patkányokon végzett eloszlási vizsgálat mutatja, a gyógyszerkoncentráció autoradiográfiás meghatározásával, a bilasztin nem halmozódik fel a központi idegrendszerben.
06.0 GYÓGYSZERÉSZETI INFORMÁCIÓK
06.1 Segédanyagok
Mikrokristályos cellulóz
Nátrium -keményítő -glikolát (A típus) (burgonyából származik)
Vízmentes kolloid szilícium -dioxid
Magnézium-sztearát
06.2 Inkompatibilitás
Nem releváns.
06.3 Érvényességi idő
5 év.
06.4 Különleges tárolási előírások
Ez a gyógyszer nem igényel különleges tárolási körülményeket.
06.5 A közvetlen csomagolás jellege és a csomag tartalma
A gyógyszert egy buborékcsomagolásba csomagolják, amely két részből áll: laminált, orientált poliamidból (a laminátum külső oldala), alumíniumból és PVC -ből (a laminátum belső oldala)
Alumíniumlemez: az alumíniumlemezt hőzáró lakkal (PVC-PVAC kopolimer és butil-metakrilát gyanták) hővel lezárják a laminátumra a formázás és a tablettákkal való feltöltés után.
Minden buborékcsomagolás 10 tablettát tartalmaz. A hólyagokat kartondobozokba csomagolják.
10, 20, 30, 40 vagy 50 tablettát tartalmazó csomagolás.
Nem feltétlenül mindegyik kiszerelés kerül kereskedelmi forgalomba.
06.6 Használati utasítás
Nincsenek speciális utasítások.
A fel nem használt gyógyszert és a gyógyszerből származó hulladékot a helyi előírásoknak megfelelően kell megsemmisíteni.
07.0 FORGALOMBA HOZATALI ENGEDÉLY
Menarini International Operations Luxembourg S.A.
1, Avenue de la Gare, L -1611 - Luxemburg
Kereskedő eladó:
A. Menarini Industrie Farmaceutiche Riunite s.r.l.
Via Sette Santi, 3 - Firenze
08.0 A FORGALOMBA HOZATALI ENGEDÉLY SZÁMA
Robilas 20 mg tabletta:
AIC n. 041045016 / M - 10 tabletta
AIC n. 041045028 / M - 20 tabletta
AIC n. 041045030 / M - 30 tabletta
AIC n. 041045042 / M - 40 tabletta
AIC n. 041045055 / M - 50 tabletta
09.0 Az első forgalomba hozatali engedély kiadásának időpontja
Az első engedélyezés időpontja: 2012. április 3
10.0 A SZÖVEG FELÜLVIZSGÁLÁSÁNAK DÁTUMA
2012. április
























.jpg)

