Hatóanyagok: Enalapril (enalapril -maleát)
Innovace 5 mg, 20 mg tabletta
Miért alkalmazzák az Innovace -t? Mire való?
Az Innovace hatóanyaga az enalapril -maleát. Ez a hatóanyag az ACE -gátlók (angiotenzin -konvertáló enzim inhibitorok) nevű gyógyszerek csoportjába tartozik.
Az Innovace alkalmazható:
- magas vérnyomás (hipertónia) kezelésére
- szívelégtelenség (szívműködés gyengülése) kezelésére. Csökkentheti a kórházi kezelés szükségességét, és segíthet néhány betegnek tovább élni
- A jelek a következők: légszomj, fáradtság könnyű fizikai tevékenység, például gyaloglás után, vagy a bokák és lábak duzzanata.
Ez a gyógyszer úgy működik, hogy tágítja az ereit. Ez csökkenti a vérnyomását. A gyógyszer általában egy órán belül hatni kezd, és a hatás legalább 24 órán át tart. Néhány embernek több hetes kezelésre van szüksége, mielőtt a vérnyomás legjobb hatása látható lenne.
Ellenjavallatok Amikor az Innovace -ot nem szabad alkalmazni
Ne szedje az Innovace -t
- ha allergiás az enalapril -maleátra vagy a gyógyszer egyéb összetevőjére
- ha korábban allergiás reakciója volt az ACE -gátlónak nevezett, ehhez a gyógyszerhez hasonló típusú gyógyszerrel szemben
- - ha korábban az arc, az ajkak, a száj, a nyelv vagy a torok duzzanata volt, amely nyelési és légzési nehézséget okozott (angioödéma), ismeretlen vagy örökletes jellegű
- ha cukorbeteg vagy vesefunkciója van, és aliszkiren tartalmú vérnyomáscsökkentő gyógyszerrel kezelik
- ha több mint 3 hónapos terhes (a terhesség korai szakaszában is célszerű elkerülni az Innovace alkalmazását - lásd a terhességre vonatkozó részt).
Ne szedje ezt a gyógyszert, ha a fenti problémák bármelyike fennáll Önnél. Ha nem biztos benne, beszéljen kezelőorvosával vagy gyógyszerészével, mielőtt elkezdi szedni ezt a gyógyszert.
Az alkalmazással kapcsolatos óvintézkedések Mit kell tudnia az Innovace szedése előtt
Az Innovace szedése előtt beszéljen kezelőorvosával vagy gyógyszerészével:
- ha szívproblémája van - ha olyan állapota van, amely az agy ereit érinti
- - ha vérproblémái vannak, például alacsony vagy hiányzik a fehérvérsejtek száma (neutropenia / agranulocitózis), alacsony a vérlemezkeszám (trombocitopénia) vagy alacsony a vörösvértestek száma (vérszegénység)
- ha májbetegsége van
- ha veseproblémája van (beleértve a veseátültetést is). Ez a vér káliumszintjének növekedéséhez vezethet, ami súlyos lehet. Előfordulhat, hogy kezelőorvosának módosítania kell az Innovace adagját, vagy ellenőriznie kell a vér káliumszintjét.
- ha dialízisben részesül
- ha nemrégiben túlzott hányása vagy súlyos hasmenése volt
- ha alacsony sótartalmú étrendet követ, kálium-kiegészítőket, káliummegtakarító szereket vagy káliumtartalmú sópótlókat szed
- ha Ön 70 évesnél idősebb
- ha cukorbeteg. Szükséges alaposan ellenőrizni a vércukorszint csökkenését, különösen a kezelés első hónapjában. A vér káliumszintje is magasabb lehet
- ha valaha allergiás reakciója volt az arc, az ajkak, a nyelv vagy a torok duzzanatával, nyelési vagy légzési nehézséggel. Tudnia kell, hogy a fekete bőrű betegeknél nagyobb a kockázata az ilyen típusú ACE -gátló reakcióknak
- - ha alacsony a vérnyomása (ezt akkor veszi észre, ha ájul vagy szédül, különösen felálláskor)
- ha kollagén vaszkuláris betegségben (pl. lupus erythematosus, reumatoid artritisz vagy szkleroderma) szenved, az immunrendszert elnyomó kezelés alatt áll, az allopurinolt vagy a prokainamidot vagy ezek kombinációit szed
- ha az alábbi, magas vérnyomás kezelésére szolgáló gyógyszerek bármelyikét szedi:
- angiotenzin II receptor antagonista (AIIRA) (más néven szartánok - például valzartán, telmizartán, irbezartán stb.), különösen, ha cukorbetegséggel kapcsolatos vesebetegsége van
- aliszkiren.
Kezelőorvosa rendszeres időközönként ellenőrizheti a veseműködését, a vérnyomását és az elektrolitok (pl. Kálium) mennyiségét a vérében.
Tájékoztassa kezelőorvosát, ha úgy gondolja, hogy terhes (vagy fennáll a terhesség lehetősége). Ez a gyógyszer nem ajánlott a terhesség korai szakaszában, és nem szedhető, ha több mint 3 hónapos terhes, mivel ebben a szakaszban súlyos károkat okozhat a babának (lásd terhesség szakasz).
Tudnia kell, hogy ez a gyógyszer kevésbé hatékonyan csökkenti a vérnyomást fekete bőrű betegeknél, mint nem fekete betegeknél.
Ha nem biztos abban, hogy a fentiek bármelyike vonatkozik -e Önre, beszéljen kezelőorvosával vagy gyógyszerészével, mielőtt elkezdi szedni ezt a gyógyszert.
Ha eljárás előtt áll
Ha az alábbi eljárások bármelyike előtt áll, közölje orvosával, hogy Innovace -ot szed:
- bármilyen típusú műtét vagy érzéstelenítés (még a fogorvosnál is)
- kezelés, amely eltávolítja a koleszterint a vérből "LDL aferezis" néven
- deszenzibilizáló kezelés a méhek vagy darázs csípések allergiájának hatásainak csökkentésére.
Ha a fentiek bármelyike vonatkozik Önre, beszéljen orvosával vagy fogorvosával az eljárás előtt.
Kölcsönhatások Mely gyógyszerek vagy ételek módosíthatják az Innovace hatását
Feltétlenül tájékoztassa kezelőorvosát vagy gyógyszerészét a jelenleg vagy nemrégiben szedett, valamint szedni tervezett egyéb gyógyszereiről. Növényi gyógyszereket tartalmaz. Ez azért van, mert az Innovace befolyásolhatja egyes gyógyszerek hatását, míg néhány más gyógyszer szintén befolyásolhatja az Innovace hatását. Előfordulhat, hogy orvosának módosítania kell az adagot, és / vagy más óvintézkedéseket kell tennie.
Különösen tájékoztassa kezelőorvosát vagy gyógyszerészét, ha az alábbi gyógyszerek bármelyikét szedi:
- angiotenzin II receptor antagonista (AIIRA) vagy aliszkiren (lásd még a „Ne szedje az Innovace -t” és a „Figyelmeztetések és óvintézkedések” című információkat)
- egyéb vérnyomáscsökkentő gyógyszerek, például béta -blokkolók vagy vízhajtók - káliumtartalmú gyógyszerek (beleértve az étrendi sóhelyettesítőket)
- cukorbetegség elleni gyógyszerek (beleértve az orális antidiabetikumokat és az inzulint)
- lítium (bizonyos típusú depresszió kezelésére használt gyógyszer)
- depresszió elleni gyógyszerek, amelyeket "triciklusos antidepresszánsoknak" neveznek - pszichés problémák kezelésére használt gyógyszerek "antipszichotikumok"
- néhány köhögés- és megfázás elleni gyógyszer, valamint testsúlycsökkentő gyógyszer, amely úgynevezett "szimpatomimetikus szert" tartalmaz
- bizonyos fájdalom- vagy ízületi gyulladáscsökkentő gyógyszerek, beleértve az aranysó terápiát-nem szteroid gyulladáscsökkentő gyógyszerek, beleértve a COX-2 inhibitorokat (gyulladást csökkentő gyógyszerek, amelyek a fájdalom enyhítésére használhatók)
- aszpirin (acetilszalicilsav)
- a vérrögök feloldására használt gyógyszerek (trombolitikumok) - alkohol
Ha nem biztos abban, hogy a fentiek bármelyike vonatkozik -e Önre, beszéljen kezelőorvosával vagy gyógyszerészével az Innovace szedése előtt.
Az Innovace egyidejű bevétele étellel és itallal
Az Innovace étellel vagy anélkül is bevehető. A legtöbb ember az Innovace -t egy pohár vízzel veszi be
Figyelmeztetések Fontos tudni, hogy:
Terhesség és szoptatás
Terhesség
Ha Ön terhes vagy szoptat, illetve ha fennáll Önnél a terhesség lehetősége vagy gyermeket szeretne, a gyógyszer alkalmazása előtt beszéljen kezelőorvosával. Kezelőorvosa általában azt tanácsolja, hogy hagyja abba az Innovace szedését, mielőtt teherbe esne, vagy amint megtudja, hogy terhes, és azt fogja javasolni, hogy az Innovace helyett más gyógyszert vegyen be. Ez a gyógyszer nem ajánlott a terhesség korai szakaszában, és nem szedhető ha több mint három hónapos terhes, mivel a terhesség harmadik hónapja után szedve súlyosan károsíthatja a babát.
Etetési idő
Tájékoztassa kezelőorvosát, ha szoptat, vagy ha szoptatnia kell. Nem ajánlott szoptatni a csecsemőket (a születés utáni első hetekben), különösen a koraszülötteknél, miközben ezt a gyógyszert alkalmazza. Idősebb gyermekek esetében kezelőorvosa tájékoztatni fogja Önt a gyógyszer szoptatás alatti szedésének kockázatairól és előnyeiről, összehasonlítva más kezelésekkel.
A készítmény hatásai a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre
A gyógyszer szedése közben szédülést vagy álmosságot tapasztalhat. Ha ez megtörténik, ne vezessen gépjárművet, és ne használjon semmilyen eszközt vagy gépet.
Az Innovace laktózt tartalmaz
Az Innovace laktózt tartalmaz, amely egyfajta cukor. Ha kezelőorvosa korábban már figyelmeztette Önt, hogy bizonyos cukrokra érzékeny, keresse fel orvosát, mielőtt elkezdi szedni ezt a gyógyszert.
Adagolás, az alkalmazás módja és ideje Az Innovace alkalmazása: Adagolás
Ezt a gyógyszert mindig az orvos vagy a gyógyszerész által elmondottaknak megfelelően szedje. Ha kétségei vannak, forduljon orvosához vagy gyógyszerészéhez.
- Nagyon fontos, hogy mindaddig folytassa a gyógyszer szedését, amíg orvosa előírja.
- Ne vegyen be több tablettát az előírtnál.
Magas vérnyomás
- A szokásos kezdő adag 5-20 mg naponta egyszer.
- Néhány betegnek alacsonyabb dózissal kell elkezdenie a kezelést.
- A szokásos fenntartó adag 20 mg naponta egyszer.
- A maximális fenntartó adag 40 mg naponta egyszer.
Szív elégtelenség
- A szokásos kezdő adag 2,5 mg naponta egyszer.
- Kezelőorvosa fokozatosan növeli az adagot, amíg el nem éri az Önnek megfelelő adagot.
- A szokásos fenntartó adag napi 20 mg, egy vagy két adagban bevéve.
- A maximális fenntartó adag napi 40 mg, két adagra osztva.
Vesebetegségben szenvedő betegek
A gyógyszer adagja a vesék működésétől függően változik:
- mérsékelt veseproblémák - 5-10 mg naponta
- súlyos veseproblémák - 2,5 mg naponta
- ha dialízisben részesül - 2,5 mg naponta. Azon napokon, amikor nem dialízis, az adag a vérnyomásnak megfelelően változtatható.
Idős betegek
Az adagot orvosa határozza meg, és a vesék működésének függvénye.
Alkalmazása gyermekeknél
Az Innovace magas vérnyomásban szenvedő gyermekeknél történő alkalmazásával kapcsolatos tapasztalatok korlátozottak. Ha a gyermek le tudja nyelni a tablettákat, az adag a gyermek súlyától és vérnyomásától függ. A szokásos kezdő adagok:
- súlya 20 kg és 50 kg között - 2,5 mg naponta
- 50 kg feletti súly - 5 mg naponta.
Az adag a gyermek szükségleteinek megfelelően módosítható:
- napi 20 mg maximális adag alkalmazható 20 és 50 kg közötti testtömegű gyermekeknél
- napi 40 mg -os maximális adag alkalmazható 50 kg -nál nagyobb testtömegű gyermekeknél.
Ez a gyógyszer nem javasolt csecsemőknek (az élet első heteiben) és veseproblémás gyermekeknek.
Túladagolás Mi a teendő, ha túl sok Innovace -t vett be?
Ha az előírtnál több Innovace -t vett be
Ha az előírtnál több Innovace -t vett be, azonnal tájékoztassa kezelőorvosát, vagy azonnal menjen kórházba. Vigye magával a gyógyszercsomagot. A következő hatások fordulhatnak elő: szédülés vagy szédülés. Ennek oka a hirtelen vagy túlzott vérnyomásesés.
Ha elfelejtette bevenni az Innovace -t
- Ha elfelejtett bevenni egy tablettát, hagyja ki az elfelejtett adagot.
- A következő adagot a szokásos módon vegye be.
- Ne vegyen be kétszeres adagot a kihagyott adag pótlására.
Ha idő előtt abbahagyja az Innovace szedését
Ne hagyja abba a gyógyszer szedését, hacsak orvosa ezt nem mondja. Ha bármilyen további kérdése van a gyógyszer alkalmazásával kapcsolatban, kérdezze meg kezelőorvosát vagy gyógyszerészét.
Mellékhatások Melyek az Innovace mellékhatásai?
Mint minden gyógyszer, így ez a gyógyszer is okozhat mellékhatásokat, amelyek azonban nem mindenkinél jelentkeznek. A következő mellékhatások jelentkezhetnek ezzel a gyógyszerrel:
Hagyja abba az Innovace szedését, és azonnal forduljon orvoshoz, ha az alábbiak bármelyikét észleli:
- az arc, az ajkak, a nyelv vagy a torok duzzanata, ami légzési vagy nyelési nehézséget okozhat
- a kezek, lábak vagy bokák duzzanata
- kiütések kialakulása kiemelkedő vörös dudorokkal (csalánkiütés).
Tudnia kell, hogy a fekete bőrű betegeknél nagyobb a kockázata az ilyen típusú reakciók kialakulásának. Ha ezen tünetek bármelyikét észleli, hagyja abba az Innovace szedését, és azonnal forduljon orvosához.
A gyógyszer szedésének megkezdésekor elájulhat vagy szédülhet. Ha ez megtörténik, hasznos lehet a fekvés. Ezt az alacsony vérnyomás okozza. A gyógyszer szedésének folytatásakor javulnia kell. Ha aggódik, forduljon orvosához.
Egyéb mellékhatások:
Nagyon gyakori (10 beteg közül több mint 1 beteget érinthet)
- szédülés, gyengeség vagy rossz közérzet
- homályos látás
- köhögés
Gyakori (10 beteg közül legfeljebb 1 beteget érinthet)
- - zavartság az alacsony vérnyomás, a szívritmus megváltozása, a gyors szívverés, az angina pectoris vagy a mellkasi fájdalom miatt
- fejfájás, depresszió, ájulás (ájulás)
- megváltozott ízérzék
- légszomj
- hasmenés, hasi fájdalom
- fáradtság (fáradtság)
- kiütés, allergiás reakciók az arc, az ajkak, a nyelv vagy a torok duzzanatával, légzési vagy nyelési nehézségekkel
- magas káliumszint a vérben, megnövekedett kreatininszint a vérben (általában mindkettő laboratóriumi vizsgálatban található meg
Nem gyakori (100 beteg közül legfeljebb 1 beteget érinthet)
- vörösség
- hirtelen vérnyomásesés
- gyors vagy szabálytalan szívverés (szívdobogás)
- szívroham (valószínűleg a nagyon alacsony vérnyomás miatt néhány magas kockázatú betegnél, beleértve azokat is, akiknek szív- vagy agyi keringési problémái vannak)
- stroke (valószínűleg a nagyon alacsony vérnyomás miatt a magas kockázatú betegeknél)
- vérszegénység (beleértve az aplasztikus és hemolitikus anémiát)
- zavartság, álmatlanság vagy álmosság, idegesség
- bizsergés vagy zsibbadás érzése
- szédülés (szédülés)
- csengés a fülben (tinnitus)
- orrfolyás, torokfájás vagy rekedtség - asztma, amely mellkasi szorítással jár
- lelassult élelmiszer -áthaladás a bélben (ileus), hasnyálmirigy -gyulladás
- hányinger, hányás, nehéz emésztés, székrekedés, étvágytalanság
- gyomorpanaszok (gyomorirritáció), szájszárazság, fekély
- izomgörcsök
- károsodott vesefunkció, veseelégtelenség
- fokozott izzadás
- viszketés vagy csalánkiütés
- hajhullás
- általános rossz közérzet, magas testhőmérséklet (láz)
- impotencia
- magas fehérjetartalom a vizeletben (laboratóriumi vizsgálattal mérve)
- alacsony vércukorszint vagy nátrium, magas vér karbamid (mindezt vérvizsgálattal mérik)
Ritka (1000 -ből legfeljebb 1 beteget érinthet)
- "Raynaud -jelenség", amelyben a kéz és a láb nagyon hideg és fehér lesz az alacsony véráramlás miatt
- a vér értékének változása, például a fehérvérsejtek és a vörösvértestek számának csökkenése, a hemoglobinszint csökkenése, a vérlemezkék számának csökkenése
- csontvelő depresszió
- a nyak, a hónalj vagy az ágyék mirigyeinek duzzanata
- autoimmun betegség
- furcsa álmok vagy alvászavarok
- folyadék vagy más anyagok felhalmozódása a tüdőben (röntgensugarak bizonyítják)
- az orr gyulladása
- tüdőgyulladás, ami légzési nehézséget okoz (tüdőgyulladás)
- az arc, az íny, a nyelv, az ajkak, a torok gyulladása
- a vizelet mennyiségének csökkenése
- célszerű kiütés (erythema multiforme)
- "Stevens-Johnson-szindróma" és "toxikus epidermális nekrolízis" (súlyos bőrbetegségek, amelyekben bőrpír és hámlás, hólyagos vagy kitett fekélyek), exfoliatív dermatitis / erythroderma (súlyos bőrkiütés a bőrfelület hámlásával vagy hámlásával), pemphigus ( kis, folyadékkal töltött hólyagok a bőrön)
- - máj- vagy epehólyag -problémák, például csökkent májfunkció, májgyulladás, sárgaság (a bőr vagy a szemek sárgulása), magas májenzim- vagy bilirubinszint (vérvizsgálattal mérve)
- megnagyobbodott mellek férfiaknál (gynecomastia)
Nagyon ritka (10 000 -ből legfeljebb 1 beteget érinthet)
- duzzanat a belekben (bél angioödéma)
Nem ismert (a gyakoriság a rendelkezésre álló adatokból nem becsülhető meg)
- az antidiuretikus hormon túlzott termelése, folyadékvisszatartást okozva, ami gyengeséget, fáradtságot vagy zavartságot okoz
- Tünetkomplexet jelentettek, amely az alábbiak egy részét vagy mindegyikét tartalmazhatja: láz, erek gyulladása (szerositis / vasculitis), izomfájdalom (myalgia / myositis), ízületi fájdalom (arthralgia / arthritis). Kiütés, fényérzékenység vagy más bőrkiütés léphet fel.
Mellékhatások bejelentése
Ha Önnél bármilyen mellékhatás jelentkezik, tájékoztassa erről kezelőorvosát vagy gyógyszerészét. Ez a betegtájékoztatóban fel nem sorolt bármilyen lehetséges mellékhatásra is vonatkozik. A mellékhatásokat közvetlenül a hatóság részére is bejelentheti az V. függelékben található elérhetőségeken keresztül. A mellékhatások bejelentésével Ön is hozzájárulhat ahhoz, hogy minél több információ álljon rendelkezésre a gyógyszer biztonságosságáról.
Lejárat és megőrzés
A gyógyszer gyermekektől elzárva tartandó!
A buborékcsomagoláson és a dobozon feltüntetett lejárati idő (EXP) után ne alkalmazza ezt a gyógyszert. A lejárati idő az adott hónap utolsó napjára vonatkozik.
Legfeljebb 25 ° C -on tárolandó.
A nedvességtől való védelem érdekében az eredeti csomagolásban tárolandó. Semmilyen gyógyszert ne dobjon a szennyvízbe vagy a háztartási hulladékba. Kérdezze meg gyógyszerészét, hogy mit tegyen a már nem használt gyógyszereivel. Ez segít a környezet védelmében.
Mit tartalmaz az Innovace?
- A készítmény hatóanyaga az enalapril -maleát (5 mg vagy 20 mg).
- Egyéb összetevők: laktóz -monohidrát, nátrium -hidrogén -karbonát, kukoricakeményítő, előzselatinizált kukoricakeményítő, magnézium -sztearát. A 20 mg -os tabletta vörös vas -oxidot (E172) és sárga vas -oxidot (E172) is tartalmaz.
Milyen az Innovace külleme és mit tartalmaz a csomagolás?
Az Innovace a következő kiszerelésben kapható:
Az ENAPREN 5 mg 2, 14, 20, 28, 28 x 1, 30, 49 x 1, 50, 60, 98 vagy 100 tablettát tartalmazó alumínium buborékcsomagolásban.
Az ENAPREN 20 mg 10, 14, 20, 28, 28 x 1, 30, 49 x 1, 50, 56, 60, 84, 90, 98, 100 vagy 500 tablettát tartalmazó alumínium buborékcsomagolásban. Nem feltétlenül mindegyik kiszerelés kerül kereskedelmi forgalomba.
Forrás betegtájékoztató: AIFA (Olasz Gyógyszerügynökség). A tartalom 2016 januárjában jelent meg. A jelenlévő információk nem feltétlenül naprakészek.
A legfrissebb verzióhoz való hozzáféréshez ajánlatos az AIFA (Olasz Gyógyszerügynökség) webhelyét elérni. Jogi nyilatkozat és hasznos információk.
01.0 A GYÓGYSZER MEGNEVEZÉSE
ENAPREN TABLETTA
02.0 MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL
Innovace 5 mg.
Minden tabletta 5 mg enalapril -maleátot tartalmaz.
Segédanyag: minden tabletta 196 mg laktóz -monohidrátot tartalmaz.
Innovace 20 mg.
20 mg enalapril -maleát tablettánként.
Segédanyag: minden tabletta 147 mg laktóz -monohidrátot tartalmaz.
Ismert hatású segédanyag (ok):
A segédanyagok teljes listáját lásd a 6.1 pontban.
03.0 GYÓGYSZERFORMA
Tabletta.
5 mg
fehér, kerek alakú, egyik oldalán törésnyom *, a másikon 712 jelzéssel.
20 mg
őszibarack színű, kerek alakú, egyik oldalán negyed törésnyom *, a másikon 714-es felirat.
* A törésjel csak a törés megkönnyítésére szolgál, hogy megkönnyítse a szájon át történő beadást, és nem a tablettát egyenlő adagokra osztja.
04.0 KLINIKAI INFORMÁCIÓK
04.1 Terápiás javallatok
• A magas vérnyomás kezelése.
• Tüneti szívelégtelenség kezelése.
• Tüneti szívelégtelenség megelőzése tünetmentes bal kamrai diszfunkcióban szenvedő betegeknél (kilökődési frakció ≤35%).
(Lásd 5.1 pont)
04.2 Adagolás és alkalmazás
Adagolás
Az élelmiszer nem zavarja az Innovace tabletta felszívódását.
Az adagot hozzá kell igazítani a betegprofilhoz (lásd 4.4 pont) és a vérnyomás -választ.
Gyermekpopuláció
Gyermekkori hipertóniás betegek klinikai vizsgálatai során az Innovace alkalmazásával kapcsolatos tapasztalatok korlátozottak (lásd 4.4, 5.1 és 5.2 pont).
Magas vérnyomás
A kezdő adag 5 mg és legfeljebb 20 mg, a magas vérnyomás mértékétől és a beteg állapotától függően (lásd alább). Az Innovace -t naponta egyszer adják be. Enyhe magas vérnyomás esetén az ajánlott kezdő adag 5-10 mg. Az intenzíven aktivált renin-angiotenzin-aldoszteron rendszerben szenvedő betegeknél (pl. Renovascularis hipertóniában, sóhiányban és / vagy hipovolemiában, dekompenzációban vagy súlyos hipertóniában szenvedő betegeknél) túlzott mértékű Az ilyen betegeknél a kezdő adag 5 mg vagy annál alacsonyabb, és a kezelés megkezdését szoros orvosi felügyelet mellett kell elvégezni.
A nagy dózisú diuretikumokkal való korábbi kezelés hypovolaemiát és hipotenzió kockázatát eredményezheti az enalapril -kezelés megkezdésekor. Az ilyen betegeknél a kezdő adag 5 mg vagy annál kevesebb. Ha lehetséges, a diuretikum-kezelést 2-3 nappal fel kell függeszteni az Innovace-kezelés megkezdése előtt. A veseműködést és a szérum káliumszintet ellenőrizni kell.
A szokásos fenntartó adag 20 mg / nap. A maximális fenntartó adag 40 mg / nap.
Szívelégtelenség / tünetmentes bal kamrai diszfunkció
A tüneti szívelégtelenség kezelésében az Innovace-t diuretikumokkal és adott esetben digitalisokkal vagy béta-blokkolókkal együtt alkalmazzák. Az Innovace kezdő adagja tüneti szívelégtelenségben vagy tünetmentes bal kamrai diszfunkcióban szenvedő betegeknél 2,5 mg, és szoros orvosi felügyelet mellett kell beadni a vérnyomásra gyakorolt kezdeti hatás meghatározásához. Tüneti járvány utáni hipotenzió hiányában. A kezelés megkezdése szívelégtelenség esetén az Innovace alkalmazásával vagy annak sikeres kezelése után az adagot fokozatosan kell növelni, a beteg tolerálhatósága alapján, a szokásos 20 mg -os fenntartó adagra, egyszeri adagként vagy 2 adagra osztva. 2-4 hetes időszak A maximális adag 40 mg, két részre osztva.
1. táblázat: Az Innovace javasolt adagolási titrálása
szívelégtelenségben / tünetmentes bal kamrai diszfunkcióban szenvedő betegeknél
* Megfelelő óvintézkedéseket kell követni azoknál a betegeknél, akik diuretikumokat kapnak, és vesekárosodásban szenvedő betegeknél (lásd 4.4 pont).
A vérnyomást és a vesefunkciót gondosan ellenőrizni kell az Innovace -kezelés megkezdése előtt és után is (lásd 4.4 pont), mivel hipotenzióról és (ritkábban) későbbi veseelégtelenségről számoltak be. Diuretikumokkal kezelt betegeknél az adagot lehetőség szerint csökkenteni kell Az Innovace -kezelés kezdete után a hipotenzió megjelenése nem jelenti azt, hogy a hypotonia visszatér az Innovace krónikus terápia során, és nem zárja ki a gyógyszer további alkalmazását.
Adagolás veseelégtelenségben
Általában meg kell hosszabbítani az enalapril adagolása közötti időközöket és / vagy csökkenteni kell az adagot.
2. táblázat: Adagolás veseelégtelenségben
* lásd 4.4 pont. Az enalaprilát dializálható. Azokon a napokon, amikor a betegek nem dialízis alatt vannak, az adagolást a vérnyomás -válasznak megfelelően kell beállítani.
Alkalmazása időseknél
Az adagnak összhangban kell lennie az idős beteg vesefunkciójával (lásd 4.4 pont).
Gyermekgyógyászati felhasználás
Azoknál a betegeknél, akik képesek lenyelni a tablettákat, az adagot a beteg profiljának és a vérnyomás -válasznak megfelelően kell beállítani. Az ajánlott kezdő adag 2,5 mg a 20 és 20 év közötti betegeknél
Az Innovace nem javasolt újszülötteknél és gyermekgyógyászati betegeknél, akiknek glomeruláris szűrési aránya 2, mivel nincs adat.
Az alkalmazás módja
Szájon át történő alkalmazás.
04.3 Ellenjavallatok
• Túlérzékenység a hatóanyaggal vagy a 6.1 pontban felsorolt bármely segédanyaggal vagy más ACE -gátlókkal szemben.
• ACE -gátló kezeléssel összefüggő angioödéma.
• Örökletes vagy idiopátiás angioödéma.
• A terhesség második és harmadik trimeszterében (lásd 4.4 és 4.6 pont).
• Az Innovace és aliszkiren tartalmú készítmények egyidejű alkalmazása ellenjavallt cukorbetegségben vagy vesekárosodásban (GFR 2) szenvedő betegeknél (lásd 4.5 és 5.1 pont).
04.4 Különleges figyelmeztetések és a használathoz szükséges óvintézkedések
Tüneti hipotónia
Szövődményes magas vérnyomásban szenvedő betegeknél ritkán jelentettek tüneti hipotenziót. Az Innovace-t kapó hipertóniás betegeknél a tüneti hipotenzió nagyobb valószínűséggel fordul elő, ha a beteg hipovolémiás, például diuretikumokkal kezelt betegek, alacsony nátriumtartalmú étrendben szenvedők, hemodializált betegek, hasmenéses vagy hányós betegek (lásd 4.5 és 4.8 pont). Tüneti hipotóniát figyeltek meg szívelégtelenségben szenvedő betegeknél, társult veseelégtelenséggel vagy anélkül. Ez nagyobb valószínűséggel fordul elő azoknál a betegeknél, akiknél súlyosabb fokú szívelégtelenség áll fenn, amint ezt nagy dózisok alkalmazása is tükrözi. Hurok diuretikumok, vesefunkció. Ezeknél a betegeknél a terápiát orvosi felügyelet mellett kell elkezdeni, és a betegeket szorosan figyelemmel kell kísérni, amikor az Innovace és / vagy a diuretikum adagját módosítják.
Hasonló megfontolások alkalmazhatók az iszkémiás szívbetegségben szenvedő vagy "cerebrovascularis betegségben szenvedő betegeknél is, akiknél a túlzott vérnyomásesés miokardiális infarktushoz vagy cerebrovaszkuláris balesethez vezethet.
Ha hipotenzió lép fel, a beteget hanyatt kell helyezni, és szükség esetén intravénás sóoldatos infúziót kell kapni. Az átmeneti vérnyomáscsökkentő válasz nem ellenjavallata a további adagoknak, amelyeket általában nehézség nélkül lehet beadni, amint a vérnyomás a térfogatnövekedés után emelkedett.
Az Innovace -kezelés a normál vagy alacsony vérnyomású szívelégtelenségben szenvedő betegek egy részénél tovább csökkentheti a vérnyomást. Ez a hatás várható, és általában nem szükséges felfüggeszteni a kezelést. Ha a hipotenzió tüneti jellegűvé válik, szükség van az adag csökkentésére és / vagy a diuretikum és / vagy az Innovace abbahagyására.
Aorta- vagy mitrális billentyű szűkület / hipertrófiás kardiomiopátia
Mint minden értágító, az ACE -gátlókat óvatosan kell alkalmazni olyan betegeknél, akiknél elzáródott a billentyű és a bal kamra, és el kell kerülni kardiogén sokk és jelentős hemodinamikai elzáródás esetén.
Károsodott vesefunkció
Vesekárosodás (kreatinin -clearance) esetén
Veseelégtelenségről számoltak be az enalaprillel kapcsolatban, és főleg súlyos szívelégtelenségben és mögöttes vesebetegségben szenvedő betegeknél fordult elő, beleértve a veseartéria -szűkületet is. Ha ezt időben felismerik és megfelelően kezelik, az enalapril -kezeléshez társuló veseelégtelenség általában visszafordítható.
Néhány magas vérnyomásban szenvedő betegnél, akiknek nincs nyilvánvaló, már meglévő vesebetegsége, a vér karbamid- és kreatininszintje emelkedett, amikor az enalaprilt diuretikummal együtt alkalmazták. Szükség lehet az enalapril adagjának csökkentésére és / vagy a diuretikum abbahagyására. Ez a körülmény megkérdőjelezi az alapvető veseartéria szűkületének lehetőségét (lásd 4.4 pont)Renovaszkuláris hipertónia).
Renovaszkuláris hipertónia
Azoknál a betegeknél, akiknél kétoldali veseartéria -szűkület vagy egyetlen működő vese artériás szűkülete van, ACE -gátlókkal kezeltek, fokozott a hipotenzió és a veseelégtelenség kockázata. A vesefunkció elvesztése csak kis szérum kreatinin -változások esetén is előfordulhat. Ezeknél a betegeknél a terápiát szoros orvosi felügyelet mellett kell elkezdeni, kis dózisokkal, gondos titrálással és a vesefunkció ellenőrzésével.
Veseátültetés
Nincs klinikai tapasztalat az Innovace alkalmazásáról olyan betegeknél, akik nemrégiben veseátültetésen estek át. Ezért az Innovace -kezelés nem ajánlott.
Májelégtelenség
Ritkán az ACE -gátlókat olyan szindrómával hozták összefüggésbe, amely kolesztatikus sárgasággal vagy májgyulladással kezdődik, és fulmináns májelhaláshoz és (néha) halálhoz vezet. Ennek a szindrómának a mechanizmusa nem ismert. Az ACE-gátlót szedő betegeknek, akik sárgaságot vagy májenzim-emelkedést észlelnek, abba kell hagyniuk az ACE-gátlót, és megfelelő orvosi ellenőrzésen kell részt venniük.
Neutropenia / agranulocytosis
Az ACE -gátlókkal kezelt betegeknél neutropeniát / agranulocitózist, thrombocytopeniát és anaemiát jelentettek. Normális és szövődményes vesefunkciójú betegeknél a neutropenia ritkán fordul elő. Az enalaprilt rendkívül óvatosan kell alkalmazni érrendszeri kollagénbetegségben, immunszuppresszív terápiában, allopurinol- vagy prokainamid-kezelésben vagy e szövődmények kombinációjában szenvedő betegeknél, különösen akkor, ha már fennáll a vesekárosodás. Ezen betegek egy részénél súlyos fertőzések alakultak ki, amelyek bizonyos esetekben nem reagáltak az intenzív antibiotikum -terápiára. Ha ezeknél a betegeknél enalaprilt alkalmaznak, ajánlatos a leukociták időszakos monitorozása, és utasítani kell a betegeket, hogy jelentsék a fertőzés jeleit.
Túlérzékenység / angioneurotikus ödéma
Az arc, a végtagok, az ajkak, a nyelv, a nyelőcső és / vagy a gége angioneurotikus ödémáját jelentették angiotenzin -konvertáló enzim inhibitorokkal, köztük az Enaprennel kezelt betegeknél. Ez a kezelés során bármikor előfordulhat. Ilyen esetekben az Innovace -t haladéktalanul abba kell hagyni, és megfelelő monitorozást kell végezni a tünetek teljes visszafejlődésének biztosítása érdekében, mielőtt a beteg kiürülne. Még azokban az esetekben is, amikor az ödéma csak a nyelvre korlátozódik, légzési zavar nélkül, a betegeknek hosszú távú megfigyelésre lehet szükségük, mivel az antihisztaminok és a kortizonok kezelése nem elegendő.
Nagyon ritkán számoltak be halálesetekről a gégeödéma vagy a nyelv ödémával járó angioödéma miatt. Légúti elzáródás valószínűsíthető azoknál a betegeknél, akiknek érintett nyelve, nyelőcsöve vagy gége van, különösen akkor, ha pozitív légúti műtétet végeztek. Valószínűsíthető légúti elzáródás, megfelelő terápia, például 1: 1000 epinefrin szubkután (0,3-0,5 ml) haladéktalanul be kell adni és / vagy fenn kell tartani a szabad légutakat.
Az ACE-gátlót kapó fekete bőrű betegeknél gyakrabban fordult elő angioödéma, mint a nem fekete betegeknél.
Azoknál a betegeknél, akiknek anamnézisében az angioödéma nem kapcsolódik az ACE -gátló kezeléshez, fokozott az angioödéma kockázata az ACE -gátló kezelés alatt (lásd még a 4.3 pontot).
Anafilaktoid reakciók a himlőre való deszenzibilizáció során
Ritkán, az ACE-gátló kezelésben részesülő betegek életveszélyes anafilaktoid reakciókról számoltak be a szaruhártya-méreggel való deszenzibilizáció során. Ezek a reakciók elkerülhetők voltak az ACE -gátló kezelés ideiglenes leállításával minden deszenzibilizálás előtt.
Anafilaktoid reakciók az LDL aferezis során
Ritkán életveszélyes anafilaktoid reakciók alakultak ki az ACE-gátló kezelésben részesülő betegek egy részénél, akik alacsony sűrűségű lipoprotein (LDL) aferezisben részesültek dextrán-szulfáttal. Ezeket a reakciókat el lehetett kerülni az ACE -gátló kezelés ideiglenes abbahagyásával minden aferezis előtt.
Hemodialízisben részesülő betegek
Anafilaktoid reakciókat jelentettek magas fluxusú membránokkal (pl. AN 69) dializált betegeknél, akiket egyidejűleg ACE -gátlóval kezeltek. Az ilyen betegeknél meg kell fontolni más típusú dialízis membrán vagy más vérnyomáscsökkentő gyógyszerek alkalmazását.
Hipoglikémia
Az orális antidiabetikumokkal vagy az ACE -gátlóval induló inzulinnal kezelt cukorbetegeknek azt kell tanácsolniuk, hogy fokozott figyelemmel kísérjék a hipoglikémiát, különösen az egyidejű alkalmazás első hónapjában (lásd 4.5 pont).
Köhögés
Köhögést jelentettek az ACE-gátlók alkalmazása során. A köhögés általában nem termékeny, tartós és a kezelés abbahagyásakor megszűnik. Az ACE-gátló okozta köhögést figyelembe kell venni a köhögés differenciáldiagnosztikájában.
Műtét / érzéstelenítés
Azoknál a betegeknél, akik nagy műtéten esnek át, vagy altatást végeznek hipotenziót okozó szerekkel, az enalapril blokkolja az angiotenzin II képződését a kompenzáló renin -felszabadulás miatt, és az ilyen esetekben fellépő hipotenziót a megnövekedett vértérfogat korrigálja.
Hiperkalémia
Néhány ACE -gátlóval, beleértve az enalaprilt, kezelt betegnél a szérum káliumszint emelkedését figyelték meg. A hyperkalaemia kialakulásának kockázati tényezői közé tartozik a veseelégtelenség, a veseműködés romlása, életkor (> 70 év), diabetes mellitus, előforduló események, különösen a kiszáradás, akut szívelégtelenség, metabolikus acidózis és diuretikumok egyidejű alkalmazása. , eplerenon, triamteren vagy amilorid), kálium-kiegészítők vagy káliumtartalmú sóhelyettesítők; vagy más, a szérum káliumszint emelkedésével járó gyógyszerek (pl. heparin) egyidejű alkalmazása. Különösen vesekárosodásban szenvedő betegeknél a káliummegtakarító vízhajtók, kálium-kiegészítők vagy káliumtartalmú sópótlók alkalmazása a szérum káliumszintjének jelentős növekedéséhez vezethet . A hyperkalaemia súlyos, néha halálos ritmuszavarokat okozhat.
Lítium
A lítium és az enalapril kombinációja általában nem javasolt (lásd 4.5 pont).
A renin-angiotenzin-aldoszteron rendszer (RAAS) kettős blokádja
Bizonyíték van arra, hogy az ACE -gátlók, angiotenzin II -receptor blokkolók vagy aliszkiren együttes alkalmazása növeli a hipotenzió, a hyperkalaemia és a csökkent vesefunkció (beleértve az akut veseelégtelenséget) kockázatát. Ezért nem ajánlott a RAAS kettős blokkolása ACE -gátlók, angiotenzin II -receptor -blokkolók vagy aliszkiren együttes használatával (lásd 4.5 és 5.1 pont).
Ha a kettős blokk terápiát feltétlenül szükségesnek ítélik, ezt csak szakember felügyelete mellett és a veseműködés, az elektrolitok és a vérnyomás szoros és gyakori ellenőrzésével szabad elvégezni.
Az ACE -gátlókat és az angiotenzin II -receptor -antagonistákat nem szabad egyidejűleg alkalmazni diabéteszes nephropathiában szenvedő betegeknél.
Laktóz
Az Innovace laktózt tartalmaz, ezért azok a betegek, akik ritka, örökletes galaktóz intoleranciában, laktázhiányban vagy glükóz-galaktóz felszívódási zavarban szenvednek, nem szedhetik ezt a gyógyszert.
Az Innovace kevesebb mint 200 mg laktózt tartalmaz tablettánként.
Gyermekpopuláció
Korlátozott tapasztalat áll rendelkezésre a hatékonyságot és biztonságosságot illetően 6 évesnél idősebb hipertóniás gyermekeknél, de a többi javallatról nincs tapasztalat. Korlátozott farmakokinetikai adatok állnak rendelkezésre 2 hónaposnál idősebb gyermekeknél (lásd még 4.2, 5.1 és 5.2 pont). Az Innovace gyermekeknek nem javallott más javallatokra, mint a magas vérnyomás.
Az Innovace nem javasolt glomeruláris szűrési sebességű újszülötteknél és gyermekgyógyászati betegeknél
Terhesség
Terhesség alatt nem szabad ACE -gátló kezelést elkezdeni. Hacsak nem tartják elengedhetetlennek a folytatólagos ACE -gátló kezelést, a terhességet tervező betegeket alternatív vérnyomáscsökkentő terápiára kell váltani, amelynek biztonsági profilja a terhesség alatt történő alkalmazásra vonatkozik. Ha a terhesség létrejött. Terhesség, az ACE -gátló kezelést azonnal le kell állítani, és ha szükség esetén alternatív terápiát kell elkezdeni (lásd 4.3 és 4.6 pont).
Etnikai különbségek
Más angiotenzin-konvertáló enzim-gátlókhoz hasonlóan, úgy tűnik, az enalapril kevésbé hatékonyan csökkenti a vérnyomást feketéknél, mint a nem feketéknél, valószínűleg a vér alacsony reninszintjének magas előfordulása miatt.
04.5 Kölcsönhatások más gyógyszerekkel és más interakciók
A renin-angiotenzin-aldoszteron rendszer (RAAS) kettős blokádja
A klinikai vizsgálatok adatai azt mutatták, hogy a renin-angiotenzin-aldoszteron rendszer (RAAS) kettős blokádja az ACE-gátlók, az angiotenzin II-receptor blokkolók vagy az aliszkiren együttes alkalmazásával nagyobb számú gyakorisággal jár együtt a nemkívánatos eseményekkel, például hipotóniával, hiperkalémiával és csökkent vesefunkció (beleértve az akut veseelégtelenséget is) a RAAS -rendszeren ható egyetlen szer alkalmazásával összehasonlítva (lásd 4.3, 4.4 és 5.1 pont).
Kálium-megtakarító vízhajtók és kálium-kiegészítők
Az ACE -gátlók csökkentik a vizelethajtó által kiváltott káliumveszteséget. A kálium-megtakarító vízhajtók (pl. Spironolakton, eplerenon, triamteren és amilorid), kálium-kiegészítők vagy káliumtartalmú sópótlók a szérum káliumszintjének jelentős növekedéséhez vezethetnek. Ha az egyidejű alkalmazást a kimutatott hypokalaemia miatt indokolt, óvatosan és a szérum káliumszint gyakori ellenőrzésével kell alkalmazni (lásd 4.4 pont).
Diuretikumok (tiazidok vagy hurok diuretikumok)
A korábbi, nagy dózisú diuretikumokkal végzett kezelés az enalapril -kezelés megkezdésekor térfogatkimerülést és hipotenzió kockázatát okozhatja (lásd 4.4 pont). A vérnyomáscsökkentő hatások csökkenthetők a diuretikumok abbahagyásával, a vértérfogat növelésével vagy sók szedésével, vagy alacsony dózisú enalapril -kezelés megkezdésével.
Más vérnyomáscsökkentő szerek
Ezeknek a gyógyszereknek az egyidejű alkalmazása fokozhatja az enalapril vérnyomáscsökkentő hatását. Egyidejű alkalmazás nitroglicerinnel és más nitrátokkal vagy más értágító szerekkel tovább csökkentheti a vérnyomást.
Lítium
A lítium és az ACE -gátlók egyidejű alkalmazása során visszafordítható szérum -lítium -koncentráció -emelkedésről és lítium -toxicitási epizódokról számoltak be. A tiazid -diuretikumok egyidejű alkalmazása tovább növelheti a lítiumszintet és növelheti a lítiumtoxicitás kockázatát ACE -gátlókkal. Az enalapril és lítium együttes alkalmazása nem ajánlott, de ha a kombináció szükséges, gondosan ellenőrizni kell a szérum lítiumszintjét (lásd. 4.4).
Triciklusos antidepresszánsok / Antipszichotikumok / Anesztetikumok / Kábítószerek
Egyes érzéstelenítő gyógyszerek, triciklusos antidepresszánsok és antipszichotikumok ACE -gátlókkal történő egyidejű alkalmazása a vérnyomás további csökkenését eredményezheti (lásd 4.4 pont).
Nem szteroid gyulladáscsökkentők (NSAID-ok), beleértve a szelektív ciklooxigenáz-2 (COX-2) inhibitorokat.
A nem szteroid gyulladáscsökkentők (NSAID-ok), beleértve a szelektív ciklooxigenáz-2 inhibitorokat (COX-2 inhibitorok), csökkenthetik a diuretikumok és más vérnyomáscsökkentők hatását. Ezért az angiotenzin II receptor antagonisták vagy az ACE-gátlók vérnyomáscsökkentő hatását gyengítheti NSAID-ok, beleértve a szelektív COX-2-gátlókat.
Az NSAID-ok (beleértve a COX-2 inhibitorokat) és az angiotenzin II receptor antagonisták vagy ACE-gátlók egyidejű alkalmazása additív hatással van a szérum káliumszint növekedésére, és a veseműködés romlásához vezethet. Ezek a hatások általában visszafordíthatók. Akut veseelégtelenség ritkán fordulhat elő, különösen olyan betegeknél, akiknek károsodott a veseműködése (például idősek, vagy vesekárosodott betegek, beleértve a diuretikummal kezelt betegeket is). Ezért a kombinációt óvatosan kell alkalmazni vesekárosodásban szenvedő betegeknél A betegeknek megfelelően hidratáltnak kell lenniük, és meg kell fontolni a vesefunkció monitorozását az egyidejű kezelés megkezdése után, majd ezt követően.
Auroterápia
Nitritoid reakciókat (amelyek tünetei közé tartozik az arc kipirulása, hányinger, hányás és hypotensio) ritkán jelentettek azoknál a betegeknél, akik ACE -gátlók, köztük a l -enalapril egyidejű alkalmazásakor injekciós aranysót (nátrium -aurotiomalát) kaptak.
Szimpatomimetikumok
A szimpatomimetikumok csökkenthetik az ACE -gátlók vérnyomáscsökkentő hatását.
Antidiabetikumok
Epidemiológiai vizsgálatok azt sugallták, hogy az ACE -gátlók és a cukorbetegség elleni gyógyszerek (inzulinok, orális hipoglikémiás szerek) egyidejű alkalmazása fokozhatja a vércukorszint -csökkentő hatást, és hipoglikémia kockázatát okozhatja. Ez a hatás nagyobb valószínűséggel jelentkezik az első hetekben kombinált kezelésben és vesekárosodásban szenvedő betegeknél (lásd 4.4 és 4.8 pont).
Alkohol
Az alkohol fokozza az ACE -gátlók vérnyomáscsökkentő hatását.
Acetilszalicilsav, trombolitikumok és béta-blokkolók
Az enalapril biztonságosan adható egyidejűleg acetilszalicilsavval (kardiológiai adagokban), trombolitikumokkal és béta-blokkolókkal.
Gyermekpopuláció
Interakciós vizsgálatokat csak felnőtteknél végeztek.
04.6 Terhesség és szoptatás
Terhesség
ACE -gátlók:
Az ACE -gátlók alkalmazása nem ajánlott a terhesség első trimeszterében (lásd 4.4 pont). Az ACE -gátlók alkalmazása ellenjavallt a terhesség második és harmadik trimeszterében (lásd 4.3 és 4.4 pont).
A terhesség első trimeszterében az ACE -gátlókkal végzett expozíciót követő teratogenitás kockázatára vonatkozó epidemiológiai bizonyítékok nem meggyőzőek; a kockázat kismértékű növekedése azonban nem zárható ki. Kivéve, ha az ACE -gátló kezelés folytatását elengedhetetlennek tartják, a terhességet tervező betegeket alternatív vérnyomáscsökkentő terápiára kell váltani, amelynek biztonságossági profilja terhesség alatt alkalmazható.
A terhesség diagnosztizálásakor az ACE -gátló kezelést azonnal le kell állítani, és szükség esetén alternatív terápiát kell kezdeni.
A terhesség második és harmadik trimeszterében az ACE -gátló kezelésnek való kitettségről ismert, hogy emberben fetotoxicitást (csökkent vesefunkció, oligohidramnion, koponyacsontosodási retardáció) és újszülöttkori toxicitást (veseelégtelenség, hypotensio, hyperkalaemia) okoz (lásd 5.3 pont). oligohidramnózis esetei voltak, amelyek feltehetően a magzati vesefunkció csökkenésére utalnak, és amelyek végtagösszehúzódásokat, koponya -arc deformációkat és pulmonális hypoplasia kialakulását okozhatják.
Ha a terhesség második trimeszterétől az ACE -gátlók expozíciója történt, ajánlott a veseműködés és a koponya ultrahangvizsgálata.
Azokat az újszülötteket, akiknek anyja ACE -gátlót szedett, gondosan ellenőrizni kell a hypotensio szempontjából (lásd 4.3 és 4.4 pont).
Etetési idő
Korlátozott farmakokinetikai adatok azt mutatják, hogy az anyatejben nagyon alacsony a koncentráció (lásd 5.2 pont). Bár ezek a koncentrációk klinikailag irrelevánsnak tűnnek, az Innovace szoptatás alatti alkalmazása koraszülött csecsemőknél és a szülés utáni első hetekben nem javasolt a kardiovaszkuláris és veseelégtelenség hipotetikus kockázata, valamint a kevés klinikai tapasztalat miatt. Idősebb csecsemők esetében az Innovace szoptatás alatti alkalmazása megfontolandó, ha ez a kezelés szükséges az anyának, de ebben az esetben a csecsemőt figyelemmel kell kísérni a lehetséges káros hatások miatt.
04.7 Hatások a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre
Gépjárművezetés vagy gépek kezelése során figyelembe kell venni, hogy időnként szédülésről és fáradtságról számoltak be.
04.8 Nemkívánatos hatások
A klinikai vizsgálatokban és a forgalomba hozatalt követően az alábbi mellékhatásokról számoltak be az enalapril esetében:
3. táblázat. Az Innovace mellékhatásai
* Az incidencia aránya összehasonlítható volt a klinikai vizsgálatokban a placebo és az aktív kontrollcsoportokban jelentettekkel.
A feltételezett mellékhatások bejelentése
A gyógyszer engedélyezése után jelentkező feltételezett mellékhatások bejelentése fontos, mivel lehetővé teszi a gyógyszer előny / kockázat arányának folyamatos nyomon követését. Az egészségügyi szakembereket kérjük, hogy jelentsék be a feltételezett mellékhatásokat a nemzeti bejelentési rendszeren keresztül. "Cím: www .agenziafarmaco.gov.it/it/Responsabili.
04.9 Túladagolás
Korlátozott mennyiségű adat áll rendelkezésre az emberek túladagolásáról. A legszembetűnőbb megnyilvánulások a kifejezett hypotensio, amely körülbelül hat órával a tabletták bevétele után kezdődik, a renin-angiotenzin rendszer blokádjával és a kábultsággal együtt. Az ACE -gátlók túladagolásával kapcsolatos tünetek közé tartozhatnak a keringési sokk, az elektrolit -zavarok, a veseelégtelenség, a hiperventiláció, a tachycardia, a szívdobogásérzés, a bradycardia, a szédülés, a szorongás és a köhögés. 300 mg és 440 mg enalapril bevitele után az enalaprilat szérumszintje 100, illetve 200 -szor magasabb volt, mint a terápiás adagok után jellemzően megfigyelt értékek.
A túladagolás ajánlott kezelése sóoldat intravénás infúziója. Hipotenzió esetén a beteget hanyatt kell helyezni. Ha rendelkezésre áll, megfontolandó az angiotenzin II -vel és / vagy katecholaminokkal való kezelés. A lenyelés nemrég történt, tegyen intézkedéseket az enalapril -maleát megszüntetésére (pl. hányás, gyomormosás, adszorbensek és nátrium -szulfát beadása). Az enaprilat hemodialízissel eltávolítható az általános keringésből (lásd 4.4 pont). A terápia-refrakter bradycardia esetén pacemaker-kezelés javasolt. Az élettani jeleket, a szérum elektrolitokat és a kreatinin-koncentrációt folyamatosan ellenőrizni kell.
05.0 FARMAKOLÓGIAI TULAJDONSÁGOK
05.1 Farmakodinámiás tulajdonságok
Farmakoterápiás csoport: Angiotenzin -konvertáló enzim inhibitorok.
ATC kód: C09A A02.
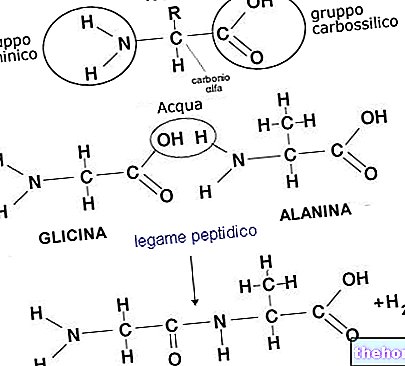
Az Innovace (enalapril-maleát) az enalapril maleát-sója, amely két aminosav, az L-alanin és az L-prolin származéka. Az angiotenzin-konvertáló enzim (ACE) egy peptidil-dipeptidáz, amely katalizálja az angiotenzin-I átalakítását nyomáshatású anyaggá. , angiotenzin II. Felszívódás után az enalapril enalaprilatává hidrolizálódik, ami gátolja az ACE -t. Az ACE gátlása a plazma angiotenzin II szintjének csökkenését eredményezi, ami a plazma renin aktivitásának növekedéséhez vezet (a renin felszabadulásával kapcsolatos negatív visszajelzések eltávolítása miatt) és csökken az aldoszteron szekrécióban.
Az ACE azonos a kinináz II -vel, így az Enapren gátolhatja a bradikinin, egy erős értágító peptid lebontását is. Ennek a hatásnak az Enapren terápiás hatásaira gyakorolt szerepe még tisztázatlan.
A cselekvés mechanizmusa
Bár úgy tűnik, hogy az Innovace csökkenti a vérnyomást, főként a renin-angiotenzin-aldoszteron rendszer elnyomása, az Innovace alacsony renin-tartalmú magas vérnyomásban szenvedő betegeknél is hatékony.
Farmakodinámiás hatások
Az Innovace hipertóniás betegeknek történő alkalmazása a fekvő- és állóvérnyomás csökkenését eredményezi anélkül, hogy jelentősen megemelkedne a pulzusszám.
A tünetekkel járó poszturális hipotenzió ritka. Néhány betegnél több hetes kezelésre lehet szükség az optimális vérnyomáscsökkentés eléréséhez.
A konvertáló enzimaktivitás hatékony gátlása rendszerint 2-4 órával kezdődik az egyszeri enalapril -adag orális beadása után.A vérnyomáscsökkentő aktivitás általában egy óra elteltével észlelhető, és a maximális aktivitás 4-6 órán belül érhető el. A hatás időtartama dózisfüggő, azonban az ajánlott adag mellett a hemodinamikai és vérnyomáscsökkentő hatások legalább 24 órán át fennmaradnak.
Az esszenciális hipertóniában szenvedő betegeknél végzett hemodinamikai vizsgálatokban a vérnyomáscsökkenés a perifériás artériás ellenállás csökkenésével járt együtt, megnövekedett szívteljesítménnyel és a szívfrekvencia nem vagy csak minimális változásával. Az Innovace beadása után megnőtt a vese véráramlása; a glomeruláris szűrési sebesség változatlannak tűnt. Nem volt nyoma víz- vagy nátrium -visszatartásnak. Azonban azoknál a betegeknél, akiknél a kezelés előtt alacsony volt a glomeruláris szűrési arány, ez általában növekedést mutatott.
Az enalapril beadását követően rövid távú klinikai vizsgálatokban cukorbeteg és nem cukorbeteg vesebetegeknél az albuminuria, a vizelet IgG kiválasztásának és a teljes proteinuria csökkenését figyelték meg.
Ha tiazid diuretikumot adnak együtt az Innovace-val, a vérnyomáscsökkentő hatás legalább additív.
Azoknál a szívelégtelenségben szenvedő betegeknél, akiket digitáliszokkal és diuretikumokkal kezeltek, az Innovace tablettával vagy injekcióval történő kezelés összefüggésben állt a perifériás ellenállás és a vérnyomás csökkenésével. A szívteljesítmény növekedett, míg a pulzusszám csökkent (általában szívelégtelenségben szenvedő betegeknél). A tüdő kapilláris éknyomása is csökkent. A New York Heart Association kritériumai szerint mért edzéstolerancia és szívelégtelenség súlyossága javult. Ezek a hatások a krónikus terápia során is fennálltak.
Enyhe vagy közepesen súlyos szívelégtelenségben szenvedő betegeknél az enalapril lelassította a szív tágulásának / megnagyobbodásának és a szívelégtelenségnek a progresszióját, amit a bal kamra szisztolés és végdiasztolés térfogatának csökkenése és a kilökődési frakció javulása is bizonyít.
A renin-angiotenzin-aldoszteron rendszer (RAAS) kettős blokádja
Két nagy, randomizált, kontrollált vizsgálatban (ONTARGET (ONgoing Telmisartan Alone and with Ramipril Global Endpoint Trial) és VA Nephron-D (The Veterans Affairs Nephropathy in Diabetes)) vizsgálták az ACE-gátló és a antagonista kombinációjának alkalmazását. angiotenzin II receptor.
Az ONTARGET vizsgálatot olyan betegeknél végezték, akiknek kórtörténetében kardiovaszkuláris vagy cerebrovaszkuláris betegség, vagy 2 -es típusú cukorbetegség áll fenn, amelyek szervi károsodással járnak. A VA NEPHRON-D egy 2-es típusú diabetes mellitusban és diabéteszes nephropathiában szenvedő betegeknél végzett vizsgálat.
Ezek a vizsgálatok nem mutattak szignifikáns jótékony hatást a vese- és / vagy kardiovaszkuláris kimenetelekre és a mortalitásra, miközben megnövekedett hyperkalaemia, akut vesekárosodás és / vagy hipotenzió kockázatát figyelték meg a monoterápiához képest.
Ezek az eredmények más ACE -gátlók és angiotenzin II receptor antagonisták esetében is relevánsak, tekintettel hasonló farmakodinámiás tulajdonságaikra.
Ezért az ACE -gátlókat és az angiotenzin II -receptor -antagonistákat nem szabad egyidejűleg alkalmazni diabéteszes nephropathiában szenvedő betegeknél.
Az ALTITUDE (aliszkiren -próba 2 -es típusú cukorbetegségben, szív- és érrendszeri és vesebetegség -végpontokat alkalmazva) egy tanulmány volt, amelynek célja annak igazolása volt, hogy előnyös az aliszkiren hozzáadása az ACE -gátló vagy angiotenzin -II -antagonista standard terápiájához cukorbetegségben szenvedő betegeknél. 2 -es típusú és krónikus vesebetegségben szenvedő betegeknél , szív- és érrendszeri betegség, vagy mindkettő. A vizsgálatot korán befejezték a nemkívánatos események megnövekedett kockázata miatt. A szív- és érrendszeri halál és a stroke számszerűen gyakoribb volt az aliszkiren csoportban, mint a placebo csoportban, valamint a nemkívánatos események és a súlyos mellékhatások (hyperkalaemia) hipotenziót és veseműködési zavarokat) gyakrabban jelentettek az aliszkiren csoportban, mint a placebo csoportban.
Klinikai hatékonyság és biztonság
Egy multicentrikus, randomizált, kettős vak, placebo-kontrollos vizsgálat (SOLVD Prevention Study) a bal kamra diszfunkciójában (LVEF) szenvedő populációt vizsgálta
Egy multicentrikus, randomizált, kettős-vak, placebo-kontrollos vizsgálatban (SOLVD kezelési tanulmány) a szisztolés diszfunkció miatt pangásos szívelégtelenségben szenvedő populációt vizsgálták (miokardiális infarktus kilökődési frakció 23% (95% CI, 11-34%; 20% instabil pangina) pectoris (95% CI, 9-29%; p
Gyermekpopuláció
Korlátozott tapasztalat áll rendelkezésre 6 évesnél idősebb, magas vérnyomásban szenvedő gyermekgyógyászati betegeknél. Egy klinikai vizsgálatban 110, 6–16 éves, magas vérnyomásban szenvedő, 20 kg -nál nagyobb testtömegű és 30 ml / perc / 1,73 m2 glomeruláris szűrési sebességű gyermekgyógyászati beteg bevonásával végeztek klinikai vizsgálatot. testtömegű betegeknek
05.2 Farmakokinetikai tulajdonságok
Abszorpció
Az orális enalapril gyorsan felszívódik; az enalapril csúcskoncentrációja az alkalmazás után egy órán belül alakul ki. A vizelettel kiválasztott mennyiség alapján az enalapril felszívódásának sebessége az Innovace tablettákból megközelítőleg 60%. Az orális Innovace felszívódását nem befolyásolja az élelmiszer jelenléte a gyomor -bél traktusban.
A felszívódást követően az orális enalapril gyorsan és nagyrészt hidrolizálódik enalapriláttá, amely erős angiotenzin -konvertáló enzim inhibitor. Az enalaprilát maximális szérumkoncentrációja körülbelül 4 órával az enalapril orális adagja után következik be. Az enalaprilát hatékony felhalmozási felezési ideje többszöri szájon át történő enalapril-adag után 11 óra .. Normális vesefunkciójú egyéneknél a szérum enalaprilát-koncentráció egyensúlyi állapotában 4 nap után érhető el.
terjesztés
Terápiás szempontból releváns koncentrációtartományon belül a humán plazmafehérjékhez kötött enalaprilát nem haladja meg a 60%-ot.
Biotranszformáció
Az enalapriláttá történő átalakítás kivételével nincs bizonyíték az enalapril jelentős metabolizmusára.
Kiküszöbölés
Az enaprilat lényegében a vesén keresztül ürül ki.A vizeletben található fő vegyületek az enalaprilat, amely az adag 40% -át teszi ki, és a változatlan enalapril (körülbelül 20%).
Vesekárosodás
Az enalapril és az enalaprilat expozíciója megnőtt veseelégtelenségben szenvedő betegeknél. Enyhe vagy közepes fokú veseelégtelenségben (kreatinin-clearance 40-60 ml / perc) szenvedő betegeknél az enalaprilát egyensúlyi stádiumú AUC-értéke kétszer olyan magas volt, mint a normális betegeknél. a vesefunkció napi 5 mg beadása után. A betegeknél
súlyos vesekárosodás (kreatinin -clearance
Gyermekek és serdülők
Többszörös dózisú farmakokinetikai vizsgálatot végeztek 40 férfi és nő hipertóniás gyermekbetegségben 2 hónapos és ≤16 év közötti, napi 0,07-0,14 mg / kg enalapril -maleát szájon át történő beadását követően. Az enalaprilát farmakokinetikájában gyermekeknél nem volt jelentős különbség a felnőttek korábbi adataihoz képest. Az adatok azt mutatják, hogy az életkor előrehaladtával az AUC (a testtömegre normalizált dózis) emelkedik; azonban nem figyelhető meg az AUC növekedése, ha az adatokat testfelület szerint normalizálják. Egyensúlyi állapotban az enalaprilát átlagos felhalmozási felezési ideje 14 óra volt.
Etetési idő
Öt szülés utáni nő egyszeri 20 mg -os orális adagja után az enalapril átlagos csúcsszintje a tejben 1,7 mcg / l (0,54-5,9 mcg / l) volt 4-6 órával az adag beadása után. Az enalaprilát átlagos csúcsértéke 1,7 mcg / l (1,2-2,3 mcg / l); a csúcsok a 24 órás időszakban különböző időpontokban jelentkeztek. A tejcsúcsokból származó adatok felhasználásával a kizárólag szoptatott csecsemők becsült maximális bevitele az anyai súlyhoz igazított adag körülbelül 0,16% -a lenne.
Egy nő, aki 11 hónapon keresztül naponta 10 mg szájon át szedett enalaprilt vett be, az enalapril tej csúcsszintje 2 mcg / l volt 4 órával az adag beadása után, és az enalaprilát csúcsértéke 0,75 mcg / l körülbelül 9 órával később. A tejben mért enalapril és enalaprilat teljes mennyisége a 24 órás időszakban 1,44 mcg / l, illetve 0,63 mcg / l volt.
Az enalaprilat szintje a tejben nem volt mérhető (
05.3 A preklinikai biztonságossági adatok
A hagyományos farmakológiai biztonságossági, ismételt dózistoxicitási, genotoxicitási és karcinogén potenciális vizsgálatok alapján a nem klinikai biztonságossági adatok nem mutatnak különleges veszélyt az emberekre. Egy olyan vizsgálatban, amelyben a gyógyszert nőstény patkányoknak adták a párzás előtt a terhességig, megnőtt a szoptató utódok halálozási aránya. A vegyületről kimutatták, hogy átjut a placenta gáton, és kiválasztódik az anyatejbe. Az angiotenzin -konvertáló enzim -gátlók, mint osztály, foetotoxikusnak bizonyultak (magzati károsodást és / vagy halált okozva), amikor a második vagy a harmadik trimeszterben alkalmazzák.
06.0 GYÓGYSZERÉSZETI INFORMÁCIÓK
06.1 Segédanyagok
Nátrium -hidrogén -karbonát
Kukoricakeményítő
Előzselatinizált kukoricakeményítő
Magnézium-sztearát
Laktóz -monohidrát
Vörös vas -oxid (E172) - csak 20 mg -os tabletták
Sárga vas -oxid (E172) - csak 20 mg -os tabletták
06.2 Inkompatibilitás
Nem releváns.
06.3 Érvényességi idő
2 év.
06.4 Különleges tárolási előírások
Legfeljebb 25 ° C -on tárolandó. A nedvességtől való védelem érdekében az eredeti csomagolásban tárolandó.
06.5 A közvetlen csomagolás jellege és a csomag tartalma
Az Innovace 5 mg tabletta 2, 14, 20, 28, 28 x 1, 30, 49 x 1, 50, 60, 98 vagy 100 tablettát tartalmazó alumínium buborékcsomagolásban kapható.
Az Innovace 20 mg tabletta 10, 14, 20, 28, 28 x 1, 30, 49 x 1, 50, 56, 60, 84, 90, 98, 100 vagy 500 tablettát tartalmazó alumínium buborékcsomagolásban kapható.
Nem feltétlenül mindegyik kiszerelés kerül kereskedelmi forgalomba.
06.6 Használati utasítás
Nincsenek speciális utasítások.
07.0 FORGALOMBA HOZATALI ENGEDÉLY
MERCK SHARP & DOHME LIMITED
Hertford Road, Hoddesdon
Hertfordshire, Nagy -Britannia
08.0 A FORGALOMBA HOZATALI ENGEDÉLY SZÁMA
28 tabletta 5 mg 025682042
14 tabletta 20 mg 025682028
28 tabletta 20 mg 025682079
09.0 Az első forgalomba hozatali engedély kiadásának időpontja
Az első engedélyezés dátuma:
Innovace 5 mg tabletta: 1987. április 27
Innovace 20 mg tabletta: 1985. március 12
Az utolsó megújítás dátuma: 2010. november 17
10.0 A SZÖVEG FELÜLVIZSGÁLÁSÁNAK DÁTUMA
2015. június