Hatóanyagok: diklofenak (diklofenák -nátrium)
AKIS 25, 50,75 mg / ml oldatos injekció
Indikációk Miért használják az Akis -t? Mire való?
Az AKIS hatóanyaga diklofenák -nátrium. Az AKIS a nem szteroid gyulladáscsökkentők (NSAID-ok) osztályába tartozik. Egyéb NSAID -ok közé tartozik az aszpirin és az ibuprofen.
Ezek a gyógyszerek csökkentik a fájdalmat és a gyulladást.
Az AKIS -t olyan állapotok tüneti kezelésére használják, mint:
- Ízületi gyulladás vagy hátfájás
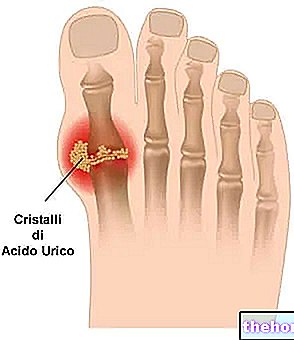
- Köszvényes támadások
- Vesekő okozta fájdalom
- Sebek, törések vagy traumák okozta fájdalom
- A műtétek utáni fájdalom kezelésére is használják
Ellenjavallatok Amikor az Akis -t nem szabad használni
Ne alkalmazza az Akis -t:
- Ha allergiás a diklofenakra, az aszpirinre, az ibuprofenre vagy más NSAID -okra
- Ha allergiás a gyógyszer (6. pontban felsorolt) egyéb összetevőjére
- -ha a nem szteroid gyulladáscsökkentők (NSAID-ok) bevétele után kórtörténetében emésztőrendszeri vérzés szerepel
- - ha két vagy több különálló gyomor- (gyomor-) vagy peptikus (nyombél) fekélye vagy emésztőrendszeri vérzése volt (beleértve a hányást vagy bélmozgást, vagy fekete kátrányos székletet)
- - ha súlyos májelégtelensége van vagy volt
- Ha súlyos szívelégtelenségben szenved vagy szenvedett
- Ha nyilvánvaló szívbetegsége és / vagy agyi érbetegsége van, pl. Szívrohama, agyvérzése, mini-stroke-ja (TIA) vagy "szív- vagy agyi erek elzáródása vagy műtét az ilyen akadályok megszüntetése vagy elkerülése érdekében"
- - ha vérkeringési problémái vannak vagy szenvedtek (perifériás artériás betegség)
- - ha súlyos veseelégtelensége van vagy volt
- Ha asztmája, csalánkiütése vagy akut rhinitis (allergia) van, amelyet NSAID vagy aszpirin alkalmazása okoz
- Ha véralvadási problémái vannak, vagy vérhígítót (például warfarint) használ
- Ha elmúlt a terhesség hatodik hónapja
- Ha Ön 18 évesnél fiatalabb.
Az alkalmazással kapcsolatos óvintézkedések Mit kell tudnia az Akis szedése előtt?
Vigyázzon Akisra
A diklofenak szedése előtt győződjön meg arról, hogy orvosa tudja
- Ha dohányzik
- Ha cukorbeteg
- Ha angina, vérrögök, magas vérnyomás, emelkedett koleszterinszint vagy emelkedett trigliceridszint van.
A nemkívánatos hatások minimálisra csökkenthetők a legalacsonyabb hatásos dózis és a szükséges legrövidebb időtartam használatával.
Az Akis alkalmazása előtt beszéljen kezelőorvosával:
- - ha valaha is nyelőcső-, gyomor- vagy nyombélfekélye vagy gyomor -bélrendszeri vérzése volt, amelynek tünetei közé tartozhat a vér hányás vagy bélmozgás során, vagy fekete kátrányos széklet
- Ha bélbetegsége van, beleértve a fekélyes vastagbélgyulladást és a Crohn -betegséget
- Ha vese- vagy májbetegsége van vagy volt
- - ha vérszegénységben vagy vérzésben szenved vagy szenved
- Ha asztmájában, krónikus obstruktív tüdőbetegségében (COPD), orrpolipokban vagy allergiás náthában szenved vagy szenvedett.
- Ha lupusban (szisztémás lupus erythematosus vagy SLE) vagy hasonló betegségekben szenved
- Ha terhességet tervez, mivel az Akis zavarhatja a fogamzást.
Kölcsönhatások Mely gyógyszerek vagy élelmiszerek változtathatják meg az Akis hatását
Feltétlenül tájékoztassa kezelőorvosát vagy gyógyszerészét a jelenleg vagy nemrégiben szedett, valamint szedni tervezett egyéb gyógyszereiről, beleértve a vény nélkül kapható készítményeket is (például vény nélkül kapható vagy szabadidős gyógyszereket). Egyes gyógyszerek zavarhatják a kezelést.
Tájékoztassa kezelőorvosát, ha az alábbi gyógyszerek bármelyikét szedi:
- Más NSAID-ok vagy ciklo-oxigenáz-2 inhibitorok, például aszpirin vagy ibuprofen (fájdalomcsillapítók)
- Antidiabetikus
- Antikoagulánsok (vérhígítók, például warfarin vagy heparin)
- Véralvadásgátlók (vérrögképződés megelőzésére)
- Diuretikumok (vizeletáramlást fokozó gyógyszerek)
- Lítium (bizonyos típusú depresszió kezelésére szolgáló gyógyszer)
- Fenitoin (epilepszia kezelésére használt gyógyszer)
- Szívglikozidok (pl. Digoxin; szívproblémák kezelésére szolgáló gyógyszer)
- Metotrexát (bizonyos típusú gyulladások és rákok kezelésére szolgáló gyógyszer)
- Ciklosporin és takrolimusz (bizonyos típusú gyulladások és immunszuppresszánsok esetén szervátültetés után)
- Kinolon antibiotikumok (bizonyos fertőzések kezelésére használt gyógyszerek)
- Szteroidok (gyulladáscsökkentő és immunrendszeri problémák kezelésére szolgáló gyógyszerek)
- Kolesztipol (koleszterinszint csökkentő gyógyszer)
- Kolesztiramin (máj- és Crohn -betegség kezelésére használt gyógyszer)
- Szulfinpirazon (köszvény kezelésére használt gyógyszer)
- Vorikonazol (gombás fertőzések kezelésére használt gyógyszer)
- Pemetrexed (kemoterápiás gyógyszer a rák bizonyos formáira)
- Deferasirox (gyakori vérátömlesztéses betegeknél használt gyógyszer)
- Mifepriszton - gyógyszer, amely a terhességmegszakítás kiváltására szolgál)
- Szívelégtelenség vagy magas vérnyomás kezelésére szolgáló gyógyszerek, például béta -blokkolók vagy ACE -gátlók
- Anksiolitikumok vagy antidepresszánsok, amelyeket szelektív szerotonin -visszavétel -gátlóknak (SSRI -k) neveznek
- Zidovudin (humán immunhiányos vírus (HIV) fertőzés kezelésére).
Figyelmeztetések Fontos tudni, hogy:
- Az olyan gyógyszerek, mint az AKIS, kismértékben fokozott szívroham (miokardiális infarktus) vagy stroke kockázatával járhatnak. A kockázat nagy dózisokkal és hosszan tartó kezeléssel nő. Ne lépje túl az ajánlott adagot vagy a megállapított kezelés időtartamát.
- Az AKIS gyulladáscsökkentő gyógyszer, így csökkentheti a fertőzés tüneteit, például a fejfájást vagy a lázat. Ha rosszul érzi magát, és kivizsgálásra szorul, ne felejtse el elmondani orvosának, hogy AKIS-t használ.
- Az idős betegek hajlamosabbak az AKIS mellékhatásaira: figyelmeztesse orvosát, ha bármilyen szokatlan tünetet észlel.
Terhesség és szoptatás
Mielőtt bármilyen gyógyszert elkezdene szedni, kérjen tanácsot orvosától vagy gyógyszerészétől.
- Az AKIS megnehezítheti a fogamzást. Tájékoztassa kezelőorvosát, ha nehézségei vannak a teherbe eséssel.
- Ha terhes, úgy gondolja, hogy terhes, vagy gyermeket tervez, kérjen tanácsot orvosától, aki eldönti, hogy az AKIS -t alkalmazza -e.
- Az AKIS -t nem szabad a terhesség hatodik hónapja után alkalmazni, mivel károsíthatja a magzat keringését vagy veséjét, és késleltetheti vagy meghosszabbíthatja a szülést
- Ha szoptat, kérjen tanácsot orvosától, aki eldönti, hogy az AKIS-t használja-e.
A készítmény hatásai a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre
Az AKIS szédülést, álmosságot vagy homályos látást okozhat. Kerülje a gépjárművezetést és a gépek kezelését, ha ezeket a panaszokat tapasztalja.
Adagolás, az alkalmazás módja és ideje Az Akis alkalmazása: Adagolás
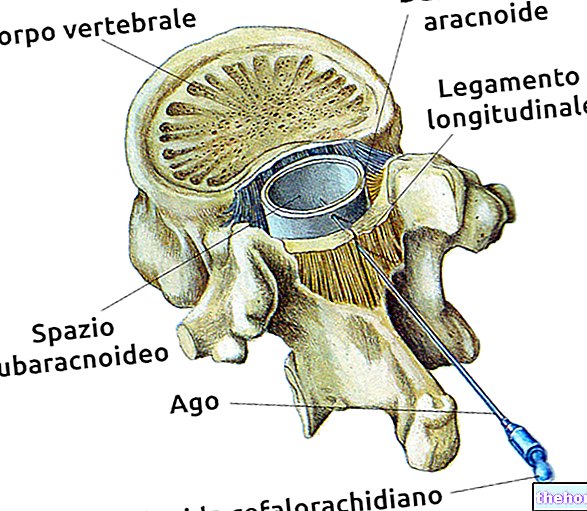
Kezelőorvosa fogja eldönteni, hogy mikor és hogyan kell alkalmazni az AKIS oldatos injekciót.Ön intramuszkuláris injekciót kap (izomba, általában a fenékbe) vagy „szubkután injekciót (a bőr alá, általában a fenékbe vagy a combba). Az AKIS -t nem szabad intravénásan (i.v.) adni.
Felnőttek: az ajánlott kezdő adag 25-75 mg, a fájdalom súlyosságától függően. Ha az erős fájdalom továbbra is fennáll, orvosa dönthet úgy, hogy 6 óra elteltével beadja Önnek a második injekciót. A maximális napi adag 150 mg. Az AKIS egy vagy két napig adható.
Idős betegek: kezelőorvosa a felnőtteknél ajánlottnál alacsonyabb adagot határozhat meg, ha Ön idős.
Gyermekek: Ne használja gyermekeknél (18 év alatt).
Az injekciót orvos, nővér vagy gyógyszerész készíti elő, nővér vagy orvos adja be az injekciót. Az injekciót nem szabad két egymást követő alkalommal ugyanazon a helyen beadni.
Túladagolás Mi a teendő, ha túl sok Akis -t vett be?
Ha az előírtnál több AKIS -t vett be, a következő tüneteket tapasztalhatja: hányinger, hányás, gyomorfájdalom, gyomor -bélrendszeri vérzés, ritkán hasmenés, szédülés, fülzúgás (zümmögés, zihálás, csengés, csengés vagy egyéb tartós csengés a fülben), és néha görcsök (roham vagy roham). Súlyos esetekben vese- vagy májkárosodás (a tünetek közé tartozik a vizelési nehézség vagy a fokozott vizelés, izomgörcsök, fáradtság, a kezek, a lábak és az arc duzzanata, hányinger vagy hányás, a bőr sárgulása (sárgaság). Azonnal tájékoztassa kezelőorvosát. Vagy nővér, ha úgy gondolja, hogy az előírtnál több AKIS -t kapott.
Mellékhatások Mik az Akis mellékhatásai?
Mint minden gyógyszer, így az AKIS is okozhat mellékhatásokat, amelyek azonban nem mindenkinél jelentkeznek.
Azonnal tájékoztassa kezelőorvosát, ha az alábbi tüneteket tapasztalja:
- Súlyos allergiás reakciók, többek között: az arc, a torok vagy a nyelv duzzanata, légzési nehézség, zihálás, nátha és bőrkiütés
- Gyomorégés vagy fájdalom, emésztési problémák, szél, hányinger vagy hányás
- A gyomor -bélrendszeri vérzés bármely tünete, például vér jelenléte a bélmozgás során, a széklet fekete elszíneződése, vér a hányásban
- Súlyos kiütés, viszketés, csalánkiütés, véraláfutás, fájdalom a vörös területeken, hólyagos vagy hámló bőr, óriás nyálkahártya (duzzadt bőr viszketéssel és égéssel). Ezek az állapotok hatással lehetnek az ajkakra, a szemre, az orrra és a nemi szervekre is
- A bőr sárgasága (sárgaság) vagy a szem szklerája
- Tartós torokgyulladás vagy láz
- Szokatlan változások a termelt vizelet mennyiségében és / vagy megjelenésében
- Szokatlan hajlam véraláfutásokra vagy gyakori torokgyulladásra és fertőzésekre.
Nagyon gyakori mellékhatások (10 beteg közül legfeljebb 1 -et érinthet)
- Fájdalom, bőrpír vagy keménység az injekció beadásának helyén
Gyakori mellékhatások (valószínűleg 100 beteg közül 1-10 beteget érint)
- Hányinger
Nem gyakori mellékhatások (1000 -ből 1 és 100 betegből 1 -et jelentettek)
- Szédülés és fejfájás
- Hasmenés, hányás és székrekedés
- A gyomornyálkahártya gyulladása fájdalommal, hányással és étvágytalansággal
- Májproblémák
- Bőrkiütés, viszketés
Egyéb mellékhatások
Az NSAID -okkal kezelt betegek a mellékhatások alábbi listájáról számoltak be.
Szív-, mell- és vér- és nyirokrendszeri betegségek
- Az olyan gyógyszerek, mint az AKIS, mérsékelten fokozott szívroham (miokardiális infarktus) vagy stroke kockázatával járhatnak
- Hipertónia, szívroham, szívdobogásérzés, mellkasi fájdalom és a törzs, a kezek és a lábak duzzanata
- Asztma, dyspnoe
- Vérbetegségek, például vérszegénység (csökkent vörösvérsejtszám). A tünetek közé tartozik a fáradtság, fejfájás, szédülés és sápadtság.
Emésztőrendszeri betegségek
- Gyomorfekély, szájfekély, nyelvfertőzés, vastagbél rendellenességek (beleértve a bélgyulladást és a Crohn -betegség súlyosbodását)
- A hasnyálmirigy és a gyomornyálkahártya gyulladása (tünetek, beleértve a súlyos gyomorfájdalmat, amely a hátra vagy a vállra is kiterjedhet).
Idegrendszeri betegségek
- Bizsergés vagy zsibbadás, bizsergés a kezekben, lábakban vagy végtagokban, remegés, homályos látás vagy diplopia, halláscsökkenés vagy problémák, tinnitus (csengés a fülben), álmosság, fáradtság
- Hallucinációk (olyan dolgok látása vagy hallása, amelyek nincsenek ott), depresszió, tájékozódási zavar, alvászavarok, ingerlékenység, szorongás, memóriazavar és görcsök (roham vagy roham)
- Az agyhártya gyulladása. A tünetek közé tartozik a nyak merevsége, fejfájás, hányinger, hányás, láz vagy tájékozódási zavar és extrém fényérzékenység. Máj- és vesebetegségek
- Májelégtelenség. A tünetek közé tartozik a hányinger, étvágytalanság, általános rossz közérzet, esetenként sárgaság
- Veseelégtelenség vagy problémák. A tünetek közé tartozik a hematuria, a habos vizelet, a kezek, a lábak és a törzs duzzanata.
A bőr és a bőr alatti szövet betegségei
- Súlyos bőrkiütések, például Stevens-Johnson szindróma és más bőrbetegségek, amelyek a napsugárzás hatására súlyosbodhatnak
- Hajhullás
Ha bármely mellékhatás súlyossá válik, vagy ha a betegtájékoztatóban felsorolt mellékhatásokon kívül egyéb tünetet észlel, kérjük, értesítse orvosát vagy gyógyszerészét.
A mellékhatásokat közvetlenül a hatóság részére is bejelentheti a "www.agenziafarmaco.gov.it/it/responsabili" címen. A mellékhatások bejelentésével Ön is hozzájárulhat ahhoz, hogy minél több információ álljon rendelkezésre a gyógyszer biztonságosságáról
Lejárat és megőrzés
- A gyógyszer gyermekektől elzárva tartandó!
- Az injekciós üvegen feltüntetett lejárati idő (Felhasználható :) után ne alkalmazza ezt a gyógyszert (A lejárati idő az adott hónap utolsó napjára vonatkozik)
- 25 ° C alatt tárolandó. Hűtőszekrényben nem fagyasztható. Az eredeti csomagolásban tárolandó, hogy a gyógyszert fénytől védje
- A gyógyszert felbontás után azonnal fel kell használni: a maradék oldatot meg kell semmisíteni
- Ne használja ezt a gyógyszert, ha zavarosságot vagy részecskéket észlel.
A helyes adag beadása után orvosa vagy a nővér kidobja a maradék oldatot a fecskendővel, tűkkel és tartályokkal együtt.
Semmilyen gyógyszert ne dobjon a szennyvízbe vagy a háztartási hulladékba. Kérdezze meg gyógyszerészét, hogy mit tegyen a már nem használt gyógyszereivel. Ez elősegíti a környezet védelmét.
Határidő "> Egyéb információ
Mit tartalmaz az AKIS?
A készítmény hatóanyaga: diklofenák -nátrium.
Minden 1 ml -es injekciós üveg tartalmaz:
- 25 mg diklofenák -nátrium vagy
- 50 mg diklofenak -nátrium vagy
- 75 mg diklofenák -nátrium
Egyéb összetevők: hidroxi -propil -béta -ciklodextrin, poliszorbát 20, injekcióhoz való víz.
Az AKIS megjelenésének leírása és a csomag tartalma
Ez a gyógyszer tiszta vagy enyhén borostyánsárga színű oldatos injekció, tiszta üvegtartályban (ampullában).
Ezt a gyógyszert steril adagolási készlettel szállítjuk, amely a következőket tartalmazza:
- 2 ml -es fecskendő
- szürke színű szubkután injekciózásra alkalmas tű (27 -es méretű)
- zöld színű intramuszkuláris injekciós tű (21 -es méretű)
1 ampulla csomag 1 adagolási készlettel, 3 ampulla 3 adagolási készlettel és 5 ampulla 5 adagolási készlettel.
Ez a gyógyszer előretöltött fecskendőben is kapható.
Nem feltétlenül mindegyik kiszerelés kerül kereskedelmi forgalomba.
Forrás betegtájékoztató: AIFA (Olasz Gyógyszerügynökség). A tartalom 2016 januárjában jelent meg. A jelenlévő információk nem feltétlenül naprakészek.
A legfrissebb verzióhoz való hozzáféréshez ajánlatos az AIFA (Olasz Gyógyszerügynökség) webhelyét elérni. Jogi nyilatkozat és hasznos információk.
01.0 A GYÓGYSZER MEGNEVEZÉSE -
AKIS INJEKCIÓS MEGOLDÁS
02.0 MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL -
A készítmény hatóanyaga: diklofenák -nátrium
Minden 1 ml -es injekciós üveg tartalmaz:
25 mg diklofenák -nátrium
50 mg diklofenak -nátrium
75 mg diklofenák -nátrium
A segédanyagok teljes listáját lásd a 6.1 pontban.
03.0 GYÓGYSZERFORMA -
Injektálható oldat
Világos vagy enyhén borostyánsárga színű átlátszó oldat
04.0 KLINIKAI INFORMÁCIÓK -
04.1 Terápiás javallatok -
Az AKIS oldatos injekció akut fájdalmas epizódok, például vesekólika, osteoarthritis és rheumatoid arthritis súlyosbodása, akut hátfájás, akut köszvényes rohamok, akut trauma és törések, műtét utáni fájdalom esetén javasolt (lásd 4.3 és 4.4 pont).
Az AKIS felnőtteknél javallt. Alkalmazása gyermekeknél nem ajánlott.
04.2 Adagolás és alkalmazás
A nemkívánatos hatások minimalizálhatók, ha a tünetek leküzdéséhez szükséges legrövidebb ideig a legalacsonyabb hatásos dózist adják be (lásd 4.4 pont).
Adagolás
Felnőttek
Az AKIS oldatos injekció intramuszkulárisan vagy szubkután adható be. Az AKIS csak rövid kezelésekre javallott, és két napnál tovább nem használható.
Enyhe vagy mérsékelt fájdalom esetén elegendő a legalacsonyabb dózis alkalmazása. Súlyos fájdalom, például vesekólika esetén 75 mg -os adag szükséges lehet. Kivételesen és súlyos esetekben a második 75 mg -os adag mg hat óra elteltével A maximális napi adag (24 óra) nem haladhatja meg a 150 mg -ot.
Ha egynél több injekcióra van szükség (legfeljebb napi 150 mg -ig), ajánlatos megváltoztatni az alkalmazás helyét a következő injekciókhoz.
Szükség esetén az AKIS injekciót más diklofenak készítményekkel együtt is lehet alkalmazni, legfeljebb 150 mg napi adagig.
Különleges populációk
Idős államporgárok
Az időseknél fokozott a nemkívánatos hatások kockázata (lásd 4.4 és 5.2 pont). Ha nem szteroid gyulladáscsökkentő kezelésre van szükség, akkor a lehető legrövidebb kezelési időtartamra a legalacsonyabb hatásos dózist kell alkalmazni.Az NSAID alkalmazása során a beteget rendszeresen ellenőrizni kell a gasztrointesztinális vérzés szempontjából. Az AKIS oldatos injekció maximális ajánlott napi adagja 150 mg.
Vesebetegségben szenvedő betegek
A hidroxipropil -betaciklodextrint (HPβCD), az AKIS oldatos injekció segédanyagát, elsősorban glomeruláris szűréssel eliminálják. Ezért a súlyos veseproblémákkal (30 ml / perc alatti kreatinin clearance) szenvedő betegeket nem szabad AKIS injekcióval kezelni (lásd 4.4 pont) és 5.2) A nem súlyos vesebetegségben szenvedő betegeket a legalacsonyabb hatásos dózissal kell kezelni.
Gyermekpopuláció
Az AKIS oldatos injekció biztonságosságát és hatásosságát 0 és 18 év közötti gyermekeknél még nem igazolták.
Az alkalmazás módja
Az AKIS oldatos injekciót csak egészségügyi személyzet adhatja be. Intramuszkulárisan vagy szubkután, tiszta, egészséges szövetben adható.
A fix dózis eléréséhez kettő helyett egyetlen injekciót kell alkalmazni. Például egyetlen 75 mg -os injekciót kell alkalmazni, nem pedig egy 25 mg -os és egy 50 mg -os injekciót, vagy egy 50 mg -os injekciót, nem pedig két 25 mg -os injekciót.
Intramuszkuláris
Az intramuszkuláris beadáshoz kövesse az alábbi utasításokat, hogy elkerülje az ideg vagy más szövet károsodását az injekció beadásának helyén. Az injekciót mélyen a fenék felső-külső negyedébe kell beadni. Ha napi két injekcióra van szükség, ajánlatos a második injekció beadási oldalát váltani. A készítményt lassan kell beadni, hogy minimális legyen a helyi szövetkárosodás.
Bőr alatti
Az injekciót a bőr alatti szövetben kell elvégezni, lehetőleg a fenék felső részén vagy a comb felső részén. A tűt teljesen a hüvelykujj és a mutatóujj közötti bőrredő vastagságába kell behelyezni. Győződjön meg arról, hogy nem hatol be az erekbe. A készítményt lassan és állandó sebességgel kell beadni.
Az AKIS -t nem szabad intravénásan injektálni (i.v.).
A használati és kezelési utasításokat lásd a 6.6 pontban.
04.3 Ellenjavallatok -
• Ismert túlérzékenység a hatóanyaggal vagy bármely segédanyaggal szemben.
• Aktív gyomor- vagy bélfekély, vérzés vagy perforáció
• A nem-szteroid gyulladáscsökkentők (NSAID-ok) bevétele után előfordult gyomor-bélrendszeri vérzés vagy perforáció
• Aktív vagy korábban ismétlődő peptikus fekély / vérzés (két vagy több különálló bizonyított fekély vagy vérzés epizód)
• A terhesség utolsó trimeszterében (lásd 4.6 pont).
• Súlyos májelégtelenség, súlyos veseelégtelenség vagy súlyos szívelégtelenség (lásd 4.4 pont)
• Más nem-szteroid gyulladásgátlókhoz (NSAID-okhoz) hasonlóan a diklofenak is ellenjavallt azoknál a betegeknél, akik asztmás rohamot, csalánkiütést vagy akut rhinitist tapasztaltak acetilszalicilsav vagy más NSAID-ok bevétele után
• Problémák hemosztázissal vagy folyamatban lévő véralvadásgátló kezeléssel (csak intramuszkuláris adagolás esetén)
• Nyilvánvaló pangásos szívelégtelenség (NYHA II-IV. Osztály), ischaemiás szívbetegség, perifériás artériás betegség és / vagy agyi érbetegség.
04.4 Különleges figyelmeztetések és a használattal kapcsolatos óvintézkedések -
Tábornok
A nemkívánatos hatások minimálisra csökkenthetők, ha a tünetek ellenőrzéséhez szükséges legrövidebb ideig a legalacsonyabb hatásos dózist adják be (lásd a 4.2. Pontot és az alábbi szakaszokat a gasztrointesztinális és kardiovaszkuláris kockázatokról).
Kerülni kell a diklofenak más szisztémás NSAID-okkal, beleértve a szelektív ciklooxigenáz-2 inhibitorokat, egyidejű alkalmazását, mivel nincs bizonyíték a szinergikus előnyökre és a lehetséges additív mellékhatásokra.
Általános orvosi szempontból óvatosság szükséges az időseknél. Különösen törékeny idős betegeknél vagy alacsony testtömegű betegeknél a legalacsonyabb hatásos dózis alkalmazása javasolt.
Más nem szteroid gyulladáscsökkentőkhöz hasonlóan ritka esetekben allergiás reakciók, beleértve az anafilaxiás / anafilaktoid reakciókat is előfordulhatnak anélkül, hogy előzetesen diklofenakot tennének ki.
A többi NSAID -hoz hasonlóan a diklofenak farmakodinamikai tulajdonságai miatt elfedheti a fertőzések jeleit és tüneteit.
Az intramuszkuláris injekcióra vonatkozó utasításokat szigorúan be kell tartani, hogy elkerüljék az injekció beadásának helyén fellépő nemkívánatos eseményeket, amelyek izomgyengeséget, izombénulást, hypoesthesiát és az injekció beadásának helyének nekrózisát okozhatják.
Emésztőrendszeri hatások
Az összes nem szteroid gyulladásgátlóval, beleértve a diklofenakot, végzett kezelés során jelentést tettek, és bármikor megjelenhetnek, figyelmeztető tünetekkel vagy anélkül, vagy anamnézisben súlyos gyomor -bélrendszeri események, gyomor -bélrendszeri vérzés, fekély vagy perforáció, amelyek halálosak lehetnek.
Általában súlyosabb következményekkel járnak az időseknél. Ha diklofenak -kezelésben részesülő betegeknél gyomor -bélrendszeri vérzés vagy fekély jelentkezik, a gyógyszer szedését abba kell hagyni.
Mint minden NSAID -hoz, beleértve a diklofenakot is, szigorú orvosi felügyelet kötelező, és különösen óvatosnak kell lenni, amikor diklofenakot írnak fel olyan betegeknek, akiknek gyomor -bélrendszeri (GI) rendellenességeire utaló tüneteik vannak, vagy akiknek kórtörténetében gyomor- vagy bélfekélyre, vérzésre vagy perforációra utalnak (lásd. 4.8). A gasztrointesztinális vérzés kockázata nagyobb az NSAID -ok nagyobb dózisával és azoknál a betegeknél, akiknek kórtörténetében fekély volt, különösen, ha vérzéssel vagy perforációval bonyolult. Az időseknél gyakrabban fordulnak elő mellékhatások, különösen a gyomor -bélrendszeri vérzés és perforáció, amelyek halálosak lehetnek.
A gasztrointesztinális toxicitás kockázatának csökkentése érdekében azoknál a betegeknél, akiknek kórtörténetében fekély volt, különösen ha vérzéssel vagy perforációval bonyolult, valamint időseknél, a kezelést a legalacsonyabb hatásos dózissal kell elkezdeni és folytatni.
A védőszerek (protonpumpa -gátlók vagy misoprosztol) egyidejű alkalmazását meg kell fontolni ezeknél a betegeknél, valamint azoknál a betegeknél, akik alacsony dózisú acetilszalicilsavat (ASA / aszpirin) vagy más olyan gyógyszereket, amelyek valószínűleg növelik az emésztőrendszeri kockázat.
Azoknak a betegeknek, akiknek kórtörténetében gasztrointesztinális toxicitás áll fenn, különösen az időseknek, jelenteniük kell a szokatlan gasztrointesztinális tüneteket (különösen a gyomor -bélrendszeri vérzést). Óvatosság ajánlott azoknál a betegeknél, akik egyidejűleg szednek gyógyszereket, amelyek növelhetik a fekély vagy vérzés kockázatát, például szisztémás kortikoszteroidokat, antikoagulánsokat, vérlemezke -gátlókat vagy szelektív szerotonin -visszavétel -gátlókat (lásd 4.5 pont). Szoros orvosi felügyelet és óvatosság szükséges a fekélyes vastagbélgyulladásban vagy Crohn -betegségben szenvedő betegeknél is, mivel ezek az állapotok súlyosbodhatnak (lásd 4.8 pont).
Májhatások
Szoros orvosi felügyelet szükséges, amikor a Diclofenac -ot májelégtelenségben szenvedő betegeknek írják fel, mivel állapotuk súlyosbodhat.
Más NSAID -okhoz hasonlóan a diklofenak is növelheti egy vagy több májenzim értékét. Hosszú diklofenak -kezelés alatt a májfunkció rendszeres ellenőrzése elővigyázatosságból indokolt. Ha a májfunkciós paraméterek tartósan megváltoznak vagy rosszabbodnak, ha a májbetegség klinikai tünetei vagy következetes tünetei alakulnak ki, vagy ha más megnyilvánulások (pl. Eozinofília, kiütés) jelentkeznek, a diklofenak -kezelést abba kell hagyni. A "hepatitis diklofenak alkalmazásával" prodromális tünetek nélkül is előfordulhat.
Különös óvatossággal kell eljárni a diklofenak máj porfíriában szenvedő betegeknél, mivel ez rohamot válthat ki.
Vesehatások
Mivel folyadékvisszatartásról és ödémáról számoltak be az NSAID -kezeléssel, beleértve a diklofenakot is, fokozott óvatosság szükséges szív- vagy veseelégtelenség, magas vérnyomás, idősek, valamint olyan betegeknél, akik egyidejűleg diuretikumokat vagy olyan gyógyszereket kapnak, amelyek jelentősen befolyásolhatják a vesét. és azoknál a betegeknél, akiknél bármilyen ok miatt (pl. nagy műtét előtt vagy után) jelentős extracelluláris térfogat -csökkenés tapasztalható (lásd 4.3 pont). Ilyen esetekben a vesefunkció ellenőrzése ajánlott elővigyázatosságból a Diclofenac alkalmazása során. A terápia abbahagyását általában a kezelés előtti állapotokhoz való visszatérés követi.
A HPβCD komponens elsősorban a vesékben glomeruláris szűréssel eliminálódik.
Ezért súlyos veseproblémákkal (30 ml / perc alatti kreatinin clearance) szenvedő betegeket nem szabad AKIS injekcióval kezelni. A nem súlyos vesebetegségben szenvedő betegeket a legalacsonyabb hatásos dózissal kell kezelni.
Bőrhatások
Súlyos bőrreakciókat, amelyek közül néhány halálos, beleértve az exfoliatív dermatitist, a Stevens-Johnson-szindrómát és a toxikus epidermális nekrolízist, nagyon ritkán jelentettek az NSAID-ok alkalmazásával összefüggésben (lásd 4.8 pont). A kezelés korai szakaszában a betegek nagyobb a kockázata: a reakció a legtöbb esetben a kezelés első hónapjában jelentkezik. Az AKIS -t abba kell hagyni, amikor bőrkiütés, nyálkahártya -elváltozás vagy egyéb túlérzékenységi tünet jelentkezik.
Kardiovaszkuláris és cerebrovaszkuláris hatások
Megfelelő megfigyelésre és oktatásra van szükség azoknál a betegeknél, akiknek kórtörténetében enyhe vagy közepes magas vérnyomás és / vagy pangásos szívelégtelenség áll fenn, mivel a NSAID -kezeléssel kapcsolatban folyadékvisszatartást és ödémát jelentettek.
A klinikai vizsgálatok és az epidemiológiai adatok azt sugallják, hogy a diklofenak alkalmazása (különösen nagy dózisban, 150 mg / nap és hosszú távú kezelések esetén) az artériás trombózisos események (pl. Miokardiális infarktus) vagy stroke kockázatának mérsékelt megnövekedésével járhat.
Azokat a betegeket, akiknél jelentős kardiovaszkuláris események kockázati tényezői vannak (pl. Magas vérnyomás, hiperlipidémia, cukorbetegség, dohányzás), csak alapos mérlegelés után lehet diklofenákkal kezelni.
Mivel a diklofenak kardiovaszkuláris kockázata az adaggal és az expozíció időtartamával együtt növekedhet, a lehető legrövidebb időtartamot és a legalacsonyabb hatékony napi dózist kell alkalmazni.
Hematológiai hatások
Hosszú diklofenak -kezelés alatt, mint más NSAID -okhoz, a vérkép ellenőrzése javasolt.
A többi nem szteroid gyulladáscsökkentőhöz hasonlóan a diklofenak is átmenetileg gátolhatja a vérlemezkék aggregációját.
A vízvisszatartás vagy az eritropoézisre gyakorolt hatások következtében vérszegénység alakulhat ki.
Következésképpen a hemoglobin és a hematokrit szintjét ellenőrizni kell az anaemia tünetei szempontjából.
Cukorbetegeknél vagy káliummegtakarító gyógyszerek mellett hiperkalémia is előfordulhat (lásd 4.5 pont).
Meglévő asztma
Az asztmás, szezonális allergiás nátha, az orrnyálkahártya duzzanata (pl. Orrpolipok), krónikus obstruktív tüdőbetegség vagy krónikus légúti fertőzések (különösen, ha az allergiás náthához hasonló tünetekhez kötődnek) betegeknél gyakoribbak, mint más betegeknél nem szteroid gyulladáscsökkentőkre adott reakciók, például asztma exacerbációk (ún. fájdalomcsillapító intolerancia / fájdalomcsillapító asztma), Quincke-ödéma vagy csalánkiütés, ezért ezeknél a betegeknél különleges elővigyázatosság ajánlott (a sürgősségi ellátásra való felkészülés).
Ez vonatkozik azokra a betegekre is, akik allergiásak más anyagokra, pl. bőrreakciókkal, viszketéssel vagy csalánkiütéssel.
SLE és vegyes kötőszöveti betegségek
Szisztémás lupus erythematosus (SLE) és vegyes kötőszöveti betegségekben szenvedő betegeknél fokozott az aszeptikus meningitis kockázata (lásd 4.8 pont).
Adminisztráció
Az injekciókat az aszepszis és az antiszepszis szigorú szabályai szerint kell végrehajtani.
A kezelés időtartama
Az AKIS -t nem szabad 2 napnál tovább alkalmazni. 2 napos terápia után mérlegelni kell a nem szteroid gyulladáscsökkentőkre való áttérés szükségességét, és ha ilyen gyógyszerekkel való hosszú távú kezelésre van szükség, a betegeket monitorozni kell a vese- és májműködési zavarok vagy a vérsejtek rendellenességei szempontjából. Ezek különösen fontosak a idős.
04.5 Kölcsönhatások más gyógyszerekkel és egyéb interakciók -
A következő kölcsönhatások közé tartoznak azok, amelyeket a diklofenak gyomornedv-ellenálló tablettákkal és / vagy a diklofenak más gyógyszerformáival észleltek.
Lítium: Az NSAID -ok növelhetik a lítium plazmakoncentrációját a csökkent lítium -kiválasztás miatt. Ha egyidejű alkalmazás szükséges, a diklofenak -kezelés kezdetén, a korrekció során és a végén ajánlott a szérum lítiumszintjének monitorozása.
Digoxin: egyidejű alkalmazás esetén a diklofenak növelheti a digoxin plazmakoncentrációját. A szérum digoxin szintjének monitorozása javasolt.
Diuretikumok, ACE-gátlók és angiotenzin-II-antagonisták : Az NSAID -ok csökkenthetik a diuretikumok és más vérnyomáscsökkentők (pl. Béta -blokkolók vagy angiotenzin -konvertáló enzim (ACE) inhibitorok) vérnyomáscsökkentő hatását. egy ACE-gátló vagy angiotenzin-II-antagonista, valamint a ciklo-oxigenázt gátló szerek a veseműködés további károsodását okozhatják, beleértve az akut veseelégtelenséget, amely általában reverzibilis. Ezért a kombinációt óvatosan kell alkalmazni, különösen időseknél. A betegeket megfelelően hidratálni kell, és mérlegelni kell a vesefunkció ellenőrzését az egyidejű kezelés megkezdése után és ezt követően rendszeresen (lásd 4.4 pont). lásd 4.4 pont)
Más NSAID -ok, kortikoszteroidok és acetilszalicilsav : diklofenak és más szisztémás nem szteroid gyulladásgátlók, kortikoszteroidok vagy acetilszalicilsav nem ajánlott, mivel növelheti a gyomor -bélrendszeri mellékhatások gyakoriságát (lásd 4.4 pont).
Antikoagulánsok és heparin (idősek vagy terápiás adagokban): Óvatosság ajánlott, mivel az egyidejű alkalmazás növelheti a vérzés kockázatát a vérlemezkék aggregációjának gátlásával vagy a gyomor -bélrendszer nyálkahártyájának károsodásával (lásd 4.4 pont). Az NSAID -ok fokozhatják az antikoagulánsok, például a warfarin és a heparin hatását. A heparin nem ajánlott időseknek vagy terápiás dózisoknak történő adagolásra. Ha az egyidejű alkalmazást nem lehet elkerülni, akkor a nemzetközi normalizált arány (INR) alapos monitorozása szükséges.
Bár a klinikai vizsgálatok adatai nem utalnak arra, hogy "a diklofenák befolyásolná az antikoagulánsok hatását", jelentettek jelentést a vérzés kockázatáról azoknál a betegeknél, akik diklofenakot kaptak antikoagulánsokkal együtt. Ezért ezeknek a betegeknek a gondos megfigyelés javasolt.
Trombolitikumok és vérlemezke -gátló szerek: Óvatosság ajánlott, mivel az NSAID-okkal való együttes alkalmazás növelheti a vérzés kockázatát a vérlemezkék működésének gátlása és a gastroduodonalis nyálkahártya károsodása miatt.
Szelektív szerotonin -visszavétel gátlók (SSRI -k): a szisztémás NSAID-ok, köztük a diklofenak és az SSRI együttes alkalmazása növelheti a gyomor-bélrendszeri vérzés kockázatát (lásd 4.4 pont).
Antidiabetikumok: a klinikai vizsgálatok kimutatták, hogy a diklofenak együtt adható orális antidiabetikumokkal anélkül, hogy befolyásolná azok klinikai hatását. Mindazonáltal mind a hipo-, mind a hiperglikémiás hatások elszigetelt eseteiről számoltak be, és szükség van a kezelés alatt alkalmazott antidiabetikumok adagjának módosítására. diklofenak Emiatt az egyidejű kezelés esetén elővigyázatosságból ajánlott a vércukorszint monitorozása.
Metotrexát: A diklofenák gátolhatja a metotrexát renális tubuláris felszabadulását azáltal, hogy növeli annak szintjét. Óvatosan kell eljárni, ha a nem szteroid gyulladáscsökkentőket, beleértve a diklofenakot, kevesebb, mint 24 órával a metotrexát -kezelés előtt vagy után adják be, mivel a metotrexát vérkoncentrációja és ennek következtében az anyag toxicitása fokozódhat. Az egyidejű kezelés első heteiben heti vérvizsgálat javasolt. Károsodott vesefunkciójú betegeknél és időseknél a megfigyelést el kell hosszabbítani.
Pemetrexed normál vesefunkciójú betegeknél, CLcr> 80 ml / perc: a pemetrexed fokozott toxicitási kockázata a csökkent elimináció miatt. Javasolt a veseműködés biológiai ellenőrzése.
Kalcineurin inhibitorok (ciklosporin, takrolimusz): a vese prosztaglandinokra gyakorolt hatásuk miatt az NSAID -ok fokozhatják a kalcineurin -inhibitorok nephrotoxicitását. Az egyidejű kezelés során javasolt a veseműködés ellenőrzése, különösen időseknél.
Deferasirox: az NSAID -ok és a deferazirox együttes alkalmazása növelheti a gasztrointesztinális toxicitás kockázatát.Ezek a gyógyszerek kombinációja gondos klinikai megfigyelést igényel.
Kinolon antibakteriális szerek: Különösen görcsrohamokról számoltak be, valószínűleg a kinolonok és az NSAID -ok egyidejű alkalmazása miatt.
Fenitoin: Ha a fenitoint diklofenakkal együtt alkalmazzák, az anyag fokozott expozíciója miatt a fenitoin plazmakoncentrációjának monitorozása ajánlott.
Kolesztipol és kolesztiramin: Ezek a szerek késleltethetik vagy csökkenthetik a diklofenák felszívódását, ezért ajánlott a diklofenakot legalább egy órával a kolesztipol / kolesztiramin beadása előtt vagy 4-6 órával beadni.
Erős CYP2C9 inhibitorok: Óvatosan kell eljárni, ha diklofenakot erős CYP2C9 inhibitorokkal (pl. Szulfinpirazon és vorikonazol) kombinálva írnak fel, ami az anyagcsere gátlása miatt jelentősen megnövelheti a plazma csúcskoncentrációt és a diklofenak -expozíciót.
Mifepristone: A mifespriszton beadása után 8-12 napig nem szabad NSAID-okat adni, mivel csökkenthetik a mifepriszton hatását.
Zidovudin: megnövekedett hematológiai toxicitás kockázata NSAID -k egyidejű alkalmazása esetén. Bizonyíték van a haemarthrosis és a hematómák fokozott kockázatára szeropozitív hemofíliás betegeknél, akik egyidejűleg kezelik a zidovudint és az ibuprofent.
Bár nagyrészt fehérjékhez kötődik, az AKIS nem zavarja a következők kötődését: szalicilátok, tolbutamid, prednizolon.
04.6 Terhesség és szoptatás -
Terhesség
A prosztaglandin -szintézis gátlása hátrányosan befolyásolhatja a terhességet és / vagy az embrió / magzat fejlődését. Az epidemiológiai vizsgálatok eredményei arra utalnak, hogy a terhesség korai szakaszában a prosztaglandin -szintézis -gátló alkalmazása után megnövekedett a spontán vetélés, a szívfejlődési rendellenességek és a gastroschisis kockázata. A szívhibák abszolút kockázata kevesebb, mint 1% -ról körülbelül 1,5% -ra nőtt.
Úgy vélték, hogy a kockázat az adag és a kezelés időtartama alatt nő. Állatokban kimutatták, hogy a prosztaglandin-szintézis inhibitorok beadása fokozott veszteséget okoz a beültetés előtt és után, valamint az embrió-magzati halálozást.
Ezenkívül a különböző rendellenességek, köztük a kardiovaszkuláris rendellenességek gyakoribb előfordulásáról számoltak be azokban az állatokban, akik prosztaglandin -szintézis -gátlókat kaptak az organogenetikai időszakban. A terhesség első és második trimeszterében a diklofenakot csak szigorúan szükséges esetekben szabad alkalmazni. Ha a diklofenakot olyan nő használja, aki teherbe akar esni, vagy a terhesség első és második trimeszterében, az adagot a lehető legalacsonyabb szinten kell tartani, és a kezelés időtartamát a lehető legrövidebbnek kell tartani.
A terhesség harmadik trimeszterében minden prosztaglandin -szintézis -gátló a következőket teheti ki a magzatnak:
- kardiopulmonális toxicitás (az artériás csatorna idő előtti bezárásával és pulmonális hipertóniával);
- veseelégtelenség, amely oligo-hidroamnionokkal veseelégtelenségig fejlődhet;
az anya és az újszülött a terhesség végén:
- a vérzési idő meghosszabbodása és vérlemezke -gátló hatás, amely még nagyon alacsony dózisok esetén is előfordulhat;
- a méhösszehúzódások gátlása, ami késleltetett vagy elhúzódó szüléshez vezet.
Következésképpen a diklofenak ellenjavallt a terhesség harmadik trimeszterében
Etetési idő
A többi NSAID -hoz hasonlóan a diklofenak kis mennyiségben bejut az anyatejbe. Ezért a diklofenakot nem szabad szoptatás alatt alkalmazni, hogy elkerüljék a csecsemő nemkívánatos hatásait.
Termékenység
A többi nem szteroid gyulladáscsökkentőhöz hasonlóan a diklofenak alkalmazása is károsíthatja a nők termékenységét, és nem ajánlott a teherbe esni vágyó nők számára.
04.7 Hatások a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre -
Azoknak a betegeknek, akik látási zavarokat, szédülést, szédülést, aluszékonyságot vagy más központi idegrendszeri rendellenességeket tapasztaltak a diklofenak alkalmazása során, tartózkodniuk kell azoktól a járművektől vagy gépektől, amelyek éberséget igényelnek.
04.8 Nemkívánatos hatások -
Klinikai vizsgálatok
Az AKIS -szel végzett klinikai vizsgálatok során megfigyelt leggyakoribb nemkívánatos hatások a gasztrointesztinális jellegűek vagy az injekció beadásának helyén fellépő reakciók, amelyek általában enyhék és átmeneti jellegűek.
A klinikai vizsgálatok eredményei azt sugallják, hogy a diklofenak oldatos injekció alkalmazása összefüggésben van az injekció beadásának helyén fellépő reakciókkal, például fájdalommal és hematómával. Az injekció beadásának helyén fellépő mellékhatások gyakorisága lényegesen alacsonyabb volt 25 és 50 mg -os dózisokkal szemben, szemben a 75 mg -mal. Hányinger, hányás, hasmenés és székrekedést is jelentettek a diklofenak beadása után.
Az alább felsorolt mellékhatások a MedDRA szervrendszeri osztályok (SOC) szerinti besorolása és a megfigyelési gyakoriság szerint, a következő egyezmény szerint: nagyon gyakori (> 1/10); gyakori (≥ 1/100,
A legmegfelelőbb MedDRA kifejezést használták egy adott reakció leírására, azonban a fel nem sorolt szinonimákat és kapcsolódó feltételeket a vártnak kell tekinteni.
Osztályhatások
A mellékhatások (1. táblázat) a gyakoriság szerint vannak felsorolva, először a leggyakoribbak, a következő konvenció szerint: nagyon gyakori (> 1/10); gyakori (≥ 1/100,
A következő mellékhatások közé tartoznak azok, amelyeket rövid vagy hosszú távú alkalmazás esetén jelentettek.
Asztal 1
A klinikai vizsgálatok és az epidemiológiai adatok következetesen arra utalnak, hogy a diklofenak alkalmazásával összefüggésben fokozott az artériás trombózisos események (például miokardiális infarktus vagy stroke) kockázata, különösen nagy dózisok (150 mg / nap) és hosszú távú kezelés esetén (lásd 4.3 pont). és 4.4 pontban az ellenjavallatokra és a különleges figyelmeztetésekre és az alkalmazással kapcsolatos óvintézkedésekre).
A feltételezett mellékhatások bejelentése
A gyógyszer engedélyezése után jelentkező feltételezett mellékhatások bejelentése fontos, mivel lehetővé teszi a gyógyszer előny / kockázat arányának folyamatos nyomon követését. Az egészségügyi szakembereket kérjük, hogy jelentsék be a feltételezett mellékhatásokat a nemzeti bejelentési rendszeren keresztül. "Address" www .agenziafarmaco.gov.it/it/Responsabili ".
04.9 Túladagolás -
Tünetek
A diklofenak túladagolásából adódóan nincs tipikus klinikai kép. A túladagolás olyan tüneteket okozhat, mint hányás, gyomor -bélrendszeri vérzés, hasmenés, szédülés, fülzúgás vagy görcsök. Jelentős mérgezés esetén akut veseelégtelenség és májkárosodás lehetséges.
Terápiás intézkedések
Az akut NSAID -mérgezés - beleértve a diklofenakot is - kezelése lényegében támogató intézkedésekből és tüneti kezelésből áll. Komplikációk, például hypotensio, veseelégtelenség, rohamok, gyomor -bélrendszeri zavarok és légzési depresszió esetén támogató intézkedéseket és tüneti kezelést kell alkalmazni.
A specifikus terápiák, mint például a kényszerített diurézis, a dialízis vagy a hemoperfúzió, nagy valószínűséggel nem segítenek megszüntetni a nem szteroid gyulladáscsökkentő szereket, beleértve a diklofenakot, mivel magas plazmafehérje -kötődésük és kiterjedt metabolizmusuk van.
05.0 FARMAKOLÓGIAI TULAJDONSÁGOK -
05,1 "Farmakodinamikai tulajdonságok -
Farmakoterápiás csoport: gyulladásgátló, nem szteroid gyógyszerek (NSAID-ok).
ATC kód: M01AB05.
Terápiás alcsoport: mozgásszervi rendszer / gyulladáscsökkentő gyógyszerek és nem-szteroid antireumatikus gyógyszerek / ecetsav-származékok és rokon anyagok.
A cselekvés mechanizmusa:
Az AKIS oldatos injekció nem szteroid szer, amely kifejezett fájdalomcsillapító és gyulladásgátló tulajdonságokkal rendelkezik. A prosztaglandin-szintézis (ciklo-oxigenáz) inhibitora. Diklofenák -nátrium in vitro nem gátolja a proteoglikánok bioszintézisét a porcokban az emberben elért koncentrációval egyenértékű koncentrációban.A műtét utáni fájdalom kezelésére opioidokkal egyidejűleg alkalmazva a diklofenak gyakran csökkenti ezek szükségességét.
Klinikai hatékonyság:
Az AKIS 25, 50 és 75 mg oldatos injekció fájdalomcsillapító hatékonyságát két kulcsfontosságú fogászati fájdalom vizsgálatban értékelték.
Egy vizsgálatban a szubkután beadott AKIS 25, 50 és 75 mg / ml fájdalomcsillapító hatékonyságát hasonlították össze a placebóval. Az AKIS minden dózisa statisztikailag magasabb és statisztikailag szignifikáns fájdalomcsökkenést eredményezett (a vizuális analóg skála VAS szerint mérve) placebóhoz (p
A második fogászati fájdalom vizsgálatban a szubkután beadott AKIS 75 mg / ml fájdalomcsillapító hatékonyságát hasonlították össze az intramuszkulárisan beadott 75 mg / 3 ml Voltaroléval. A két kezelés között nem volt szignifikáns különbség. Az alkalmazás utáni 8 órában. 1,5 órával az adagolás után (a vizsgálat hatékonyságának elsődleges mértékegysége) a 95% -os megbízhatósági intervallum a két kezelés közötti különbséghez képest teljes mértékben meghaladta a nem-inferioritás határát (-15 mm). Ezért az AKIS terápiás szempontból egyenértékű volt a A két kezelés közötti átlagos különbségek és a 95% -os megbízhatósági intervallumok mindegyik kontroll között a gyógyszer beadását követő 8 órában az alábbi táblázatban láthatók.
05,2 "Farmakokinetikai tulajdonságok -
Abszorpció
Intramuszkuláris injekció
Az AKIS 75 mg / ml oldatos injekció intramuszkuláris úton történő beadása után a felszívódás gyors, és a plazma csúcskoncentrációja 2,603 ± 0,959 mcg / ml (2,5 ug / ml körülbelül 8 mcmol / l -nek felel meg) 34 perc elteltével.
A koncentrációs görbe alatti terület (AUC) egyenlő AUC0-t 250,07 ± 46,89 mcg / ml.min. Összehasonlító klinikai vizsgálatokban az intramuszkuláris Voltarol (75 mg / 3 ml) fő plazma csúcskoncentrációja 2,242 ± 0,566 mcg / ml, és 27 perc elteltével érik el, míg az AUC0-t értéke 246,70 ± 39,74 mcg / ml.min.
Subcutan injekció
Az AKIS 75 mg / ml oldatos injekció beadása után az abszorpció gyors, és a plazma csúcskoncentráció 2138 ± 0,646 mcg / ml (2,5 mcg / ml körülbelül 8 mcmol / l) 40 perc alatt érhető el.
Az AUC0-t 261,94 ± 53,29 mcg / ml.min. Összehasonlító klinikai vizsgálatokban az intramuszkuláris Voltarol plazma csúcskoncentrációja 27 perc alatt 2,242 ± 0,566 mcg / ml, míg az AUC0-t értéke 246,70 ± 39,74 mcg / ml.min .
A szubkután beadott AKIS 75 mg bioekvivalens volt az intramuszkulárisan adott Voltarol 75 mg / 3 ml -rel mind az AUC, mind a Cmax tekintetében. Az AUC szubkután beadás után megközelítőleg kétszerese az orális vagy rektális adagolásénak, mivel ez az útvonal elkerüli a máj első lépést.
A diklinofenak szubkután beadását követően az AUC tekintetében az adag lineáris volt. A Cmax nem volt dózisarányos, az átlagos Cmax értékek 1090 ng / ml, 1648,9 ng / ml és 1851,1 ng / ml, 25 mg, 50 mg és 75 mg AKIS beadása után.
terjesztés
A diklofenák 99,7% -ban kötődik a plazmafehérjékhez, főként albuminhoz (99,4%). A diklofenák behatol az ízületi folyadékba, ahol a maximális koncentrációt 2-4 órával a plazmacsúcsok elérése után észlelik. Az ízületi folyadékokból látható látszólagos felezési idő 3-6 órák. Két órával a plazmacsúcsok elérése után a hatóanyag koncentrációja magasabb az ízületi folyadékban, mint a plazmában, és akár 12 órán keresztül is az marad.
Biotranszformáció
A diklofenak biotranszformációja részben a molekula glükuronidálásával, de főleg "egyszeri vagy többszörös hidroxilezéssel és metoxilezéssel történik, ami számos fenolos metabolitot eredményez, amelyek közül sok glükuron konjugátummá alakul. Két fenolos metabolit biológiailag aktív, de nagymértékben alacsonyabb, mint a diklofenaké.
Kiküszöbölés
A diklofenák teljes szisztémás clearance -e a plazmában 263 ± 56 ml / perc (átlagos érték ± SD). A terminális felezési idő a plazmában 1-2 óra, a metabolitok közül négy, köztük a két aktív, szintén rövid, 1-3 órás felezési idővel rendelkezik.
A beadott adag körülbelül 60% -a ürül a vizelettel a molekula glükuronsav -konjugátuma formájában, mint ilyen és metabolitok formájában, amelyek közül sok glükuron konjugátummá alakul át; kevesebb, mint 1% ürül változatlan anyagként, A beadott adag fennmaradó része az epével és a széklettel ürül.
A betegek jellemzői
Idős államporgárok: Nem figyeltek meg lényeges különbségeket az életkorfüggő gyógyszerek felszívódásában, metabolizmusában vagy kiválasztásában.
Vesebetegségben szenvedő betegek: veseelégtelenségben szenvedő betegeknél, ha a szokásos adagolási rendet betartják, a kinetikai vizsgálatokban nem figyelhető meg a hatóanyag felhalmozódása az egyszeri adag beadása után. Kreatinin clearance értékek mellett a hidroxilezett metabolitok egyensúlyi állapotú plazmaszintje körülbelül négyszer magasabb, mint a normál alanyoké. A metabolitok azonban az epével eliminálódnak.
Májbetegségben szenvedő betegek: krónikus hepatitisben vagy dekompenzált cirrhosisban szenvedő betegeknél a diklofenak kinetikája és metabolizmusa ugyanaz, mint a májbetegségben nem szenvedő betegeknél.
05.3 A preklinikai biztonságossági adatok -
A diklofenák -nátriummal kapcsolatban nem végeztek új preklinikai vizsgálatokat. A termék biztonsági profilja jól ismert.
A helyi tolerancia vizsgálat kimutatta, hogy a készítmény nem okoz jelentős vagy váratlan helyi toxicitást sem intramuszkuláris vagy szubkután beadást követően.
06.0 GYÓGYSZERÉSZETI INFORMÁCIÓK
06.1 Segédanyagok -
Hidroxipropil -béta -ciklodextrin,
Poliszorbát 20,
Injekcióhoz való víz
06.2 Inkompatibilitás "-
Inkompatibilitási vizsgálatok hiányában ezt a gyógyszert nem szabad más termékekkel keverni.
06.3 Érvényességi idő "-
2 év
A gyógyszert felbontás után azonnal fel kell használni: a maradék oldatot meg kell semmisíteni.
06.4 Különleges tárolási előírások -
Legfeljebb 25 ° C -on tárolandó. Hűtőszekrényben nem fagyasztható.
Az eredeti csomagolásban tárolandó, hogy a gyógyszert fénytől védje.
06.5 A közvetlen csomagolás jellege és a csomagolás tartalma -
I. típusú átlátszó üveg injekciós üveg.
1, 3 és 5 ampulla csomagolásban.
Nem feltétlenül mindegyik kiszerelés kerül kereskedelmi forgalomba.
06.6 Használati és kezelési útmutató -
Minden injekciós üvegben túladagolás van, hogy 1 ml oldatot extraháljunk.
Injekciós üvegek: Nincsenek speciális utasítások.
A terméket nem szabad használni, ha kristályokat vagy csapadékot észlel.
A fel nem használt gyógyszert és a gyógyszerből származó hulladékot a helyi előírásoknak megfelelően kell megsemmisíteni
07.0 A „FORGALOMBA HOZATALI ENGEDÉLY” TULAJDONOSA -
IBSA Farmaceutici Italia Srl, Martiri di Cefalonia útján, 2, 26900 Lodi
08.0 A FORGALOMBA HOZATALI ENGEDÉLY SZÁMA -
AKIS "75 mg / ml oldatos injekció" 1 ampulla - AIC: 040528073;
AKIS "75 mg / ml oldatos injekció" 3 ampulla - AIC: 040528085;
AKIS "75 mg / ml oldatos injekció" 5 ampulla - AIC: 040528097;
AKIS "50 mg / ml oldatos injekció" 1 injekciós üveg - AIC: 040528061;
AKIS "50 mg / ml oldatos injekció" 3 ampulla - AIC: 040528059;
AKIS "50 mg / ml oldatos injekció" 5 ampulla - AIC: 040528046;
AKIS "25 mg / ml oldatos injekció" 1 injekciós üveg - AIC: 040528010;
AKIS "25 mg / ml oldatos injekció" 3 ampulla - AIC: 040528022;
AKIS "25 mg / ml oldatos injekció" 5 ampulla - AIC: 040528034;
09.0 AZ ELSŐ ENGEDÉLYZÉS ÉS A JÓVÁHAGYÁS MEGÚJÍTÁSÁNAK DÁTUMA -
Az első engedélyezés időpontja: 2013. november 22
10.0 A SZÖVEG FELÜLVIZSGÁLÁSÁNAK DÁTUMA -
09/2016