2,3 -difoszfoglicerát (2,3 DPG) a glikolízis köztes termékéből származó vegyület; különösen a vörösvértestek szintjén koncentrálódik, mivel a vörösvértestek - mitokondriumok nélkül - az anaerob tejsav -anyagcserét (a glükóz homolaktikus fermentációját) használják ki, hogy energiát nyerjenek.

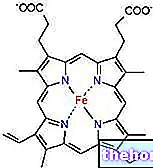
A hemoglobin egy tetramer fehérje, amely négy alegységből, két alfa- és két béta -alegységből áll, mindegyik egy fehérje részből (globin) és egy hemből (protéziscsoport, amely megköti az oxigént). A 2,3-difoszfoglicerát a Béta-láncokhoz kapcsolódik, tömöríti őket és csökkenti a hemoglobin oxigén-affinitását.
A 2,3 DPG -nek a hemoglobinhoz való kötődése akkor következik be, amikor az oxigénmentesített formában van, míg a tüdőben feloldódik a hemoglobin oxigénhez való kötődésével. Valójában, amikor a hemoglobin eléri a szöveteket, a β -láncok elsőként bocsátják ki az oxigént, és ez a veszteség magában foglalja a monomerek elmozdulását a középpontból. Amint a belső hidrofil üreg kinyílik, a DPG belép és kötődik a tetramerhez, és heteropoláris kötéseket képez negatív töltésű csoportjai, valamint a lizin és a hisztidin között a Béta láncok maradéka, pozitív töltésű A stabilizált szerkezet a két α lánc oxigénjét is felszabadíthatja. A tüdőben azonban fordított folyamat megy végbe; magas oxigénnyomás esetén az α-láncok kötik le először, és a DPG-t "összenyomják" és kilökik a tetramerből, lehetővé téve a könnyebb oxigén-β lánc kötést.
A 2,3 -biszfoszfoglicerát nem tud kötődni a magzati hemoglobinhoz, mivel ez a molekula nem tartalmaz B -láncokat, amelyekhez a 2,3 DPG kötődik. Ez megmagyarázza a magzati hemoglobin oxigénnel szembeni nagyobb affinitását, mint az anyai hemoglobin, ami lehetővé teszi a magzati vér oxigént von ki az anyai vérből.