Milyen típusú gyógyszer a Targretin?
A Targretin egy bexarotén hatóanyagot tartalmazó gyógyszer. Fehér lágy kapszula (75 mg) formájában kapható.
Milyen betegségek esetén alkalmazható a Targretin?
A Targretint a bőr T-sejtes limfóma (CTCL) betegeknél látható bőrkiütések kezelésére alkalmazzák. A bőr T-sejtes limfóma a limfóma ritka típusa (a nyirokszövet rákja), amely akkor fordul elő, amikor egy bizonyos típusú fehérvérsejt (T-sejt) nő a bőrben. A Targretint olyan betegeknél alkalmazzák, akik előrehaladott betegségben szenvednek, és akik nem reagáltak legalább egy korábbi kezelésre.
A gyógyszer csak receptre kapható.
Hogyan kell alkalmazni a Targretint?
A Targretin-kezelést csak a bőr T-sejtes limfómájában szenvedő betegek kezelésében jártas orvosok kezdhetik és folytathatják A Targretin adagja a beteg testfelületétől függ, négyzetméterben (m2) mérve. Az ajánlott kezdő adag 300 mg / m2 / nap. Az adag a beteg kezelésre adott válaszának vagy a mellékhatásoknak megfelelően módosítható. A terápiát addig kell folytatni, amíg a beteg hasznot húz belőle. További részletekért kérjük, tekintse meg az EPAR -ban található alkalmazási előírást.
A Targretin kapszulákat napi egyszeri adagban, étkezés közben kell bevenni.
Hogyan fejti ki hatását a Targretin?
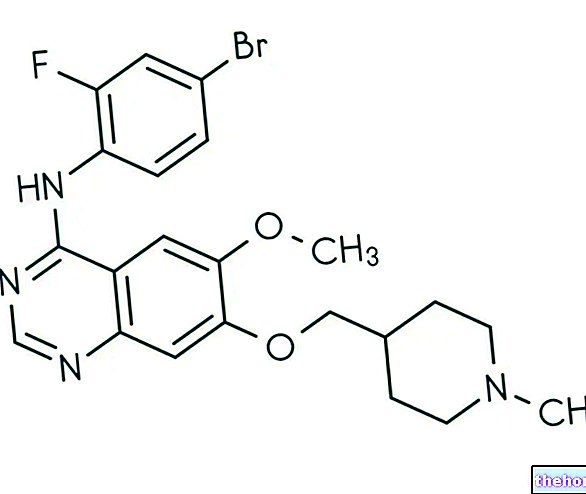
A Targretin hatóanyaga, a bexarotén, rákellenes szer, amely a retinoidok csoportjába tartozik, az A -vitaminból származó anyagok. A bexaroten pontos hatásmechanizmusa a CTCL -ben nem ismert.
Milyen módszerekkel vizsgálták a Targretint?
A Targretin hatékonyságát két vizsgálatban vizsgálták, amelyekben összesen 193 CTCL -es beteg vett részt, akik nem reagáltak legalább két korábbi kezelésre. Ezek közül 93 beteg volt a betegség előrehaladott stádiumában, és nem reagáltak más kezelésekre. 61 beteget 300 mg / m2 / nap kezdő dózissal kezeltek. A hatékonyság fő mértéke a kezelésre adott válasz 16 hét után volt, az orvos értékelése a EMEA 2007 javulásról és 5 klinikai tünet (érintett bőrfelület, bőrpír, kiemelkedő területek, pikkelyes bőr és festés) alapján kapott pontszám alapján.
Milyen előnyei voltak a Targretin alkalmazásának a vizsgálatok során?
A két vizsgálatban a 300 mg / m2 -rel kezelt betegek körülbelül fele reagált a kezelésre, az orvos értékelése szerint, illetve a következő százalékok: 36% és 27%.
Milyen kockázatokkal jár a Targretin alkalmazása?
A Targretin leggyakrabban észlelt mellékhatásai (10 beteg közül több mint 1 -nél) a leukopenia (a fehérvérsejtek számának csökkenése a vérben), hypothyreosis (elégtelen pajzsmirigy -aktivitás), hiperlipémia (magas vérzsírszint) ), hiperkoleszterinémia (magas vérkoleszterinszint), exfoliatív dermatitis (bőrhámlás), viszketés, bőrpír, fájdalom, fejfájás és aszténia (gyengeség) A Targretin alkalmazásával kapcsolatban jelentett mellékhatások teljes listáját lásd a betegtájékoztatóban.
A Targretin nem alkalmazható olyan betegeknél, akik túlérzékenyek (allergiásak) lehetnek a bexaroténre vagy bármely más anyagra. A Targretin nem adható továbbá:
- terhes vagy szoptató nők;
- nők, akik teherbe eshetnek;
- emberek, akik korábban hasnyálmirigy -gyulladásban (hasnyálmirigy -gyulladásban) szenvedtek;
- ellenőrizetlen hiperkoleszterinémiában (magas koleszterinszint) szenvedő emberek;
- ellenőrizetlen hypertrigliceridémiában szenvedők (magas triglicerid [zsírok] szintje a vérben);
- hipervitaminosis A -ban szenvedők (magas A -vitamin -szint a szervezetben);
- ellenőrizetlen pajzsmirigy -betegségben szenvedők;
- májbetegségben szenvedők;
folyamatos fertőzésben szenvedő emberek.
Miért engedélyezték a Targretin forgalomba hozatalát?
Az emberi felhasználásra szánt gyógyszerek bizottsága (CHMP) úgy döntött, hogy a Targretin előnyei meghaladják a kockázatokat a bőr megnyilvánulásainak kezelésében azokban a betegekben, akik előrehaladott, legalább egy szisztémás kezelésre nem reagáló, előrehaladott bőrű T-sejtes limfómában szenvednek, ezért javasolta a "engedély a termék forgalmazására".
Egyéb információ a Targretin -ről:
2001. március 29 -én az Európai Bizottság a Targretinre vonatkozóan kiadta az Európai Unió egész területére érvényes "forgalomba hozatali engedélyt". A "forgalomba hozatali engedélyt" 2006. március 29 -én megújították. A forgalomba hozatali engedély jogosultja az Eisai Ltd.
A Targretin EPAR teljes verziójáért kattintson ide.
Az összefoglaló utolsó frissítése: 2007-2003.
Az ezen az oldalon közzétett információk a Targretin - bexaroténről elavultak vagy hiányosak lehetnek. Ezen információk helyes használatához tekintse meg a Jogi nyilatkozat és a hasznos információk oldalt.

















.jpg)