Hatóanyagok: Urapidil
URAPIDIL STRAGEN 25 mg oldatos injekció
URAPIDIL STRAGEN 50 mg oldatos injekció
Miért alkalmazzák az Urapidil Stragen -t? Mire való?
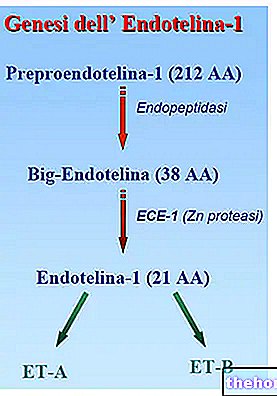
Az URAPIDIL STRAGEN hatóanyaga az Urapidil.
Az URAPIDIL STRAGEN az alfa -blokkoló gyógyszerek csoportjába tartozik. A gyógyszer hatása az erekben (pl. Artériákban és vénákban) lokalizálódik, és csökkenti a vérnyomást az erek falának ellazításával.
Az URAPIDIL STRAGEN a magas vérnyomás súlyos eseteinek kezelésére szolgál:
- vészhelyzet esetén, amikor magas a vérnyomás, és szervi sérüléssel, amely gyorsan életveszélyes;
- műtét alatt és / vagy után.
Ellenjavallatok Ha az Urapidil Stragen nem alkalmazható
Ne alkalmazza az URAPIDIL STRAGEN -t
- ha allergiás az urapidilre vagy a gyógyszer (6. pontban felsorolt) egyéb összetevőjére.
- - ha aorta -szűkületként ismert szívműködési rendellenességben vagy szív -shuntként ismert véredény -rendellenességben szenved (kivéve a dialízisben részesülő betegek szívöntését).
Az alkalmazással kapcsolatos óvintézkedések Mit kell tudnia az Urapidil Stragen szedése előtt?
Az URAPIDIL STRAGEN alkalmazása előtt orvosának ellenőriznie kell:
- - ha valaha hasmenése vagy hányása volt (vagy bármilyen más oka a szervezetben lévő folyadékmennyiség csökkenésének);
- ha csökkent a nátrium a vérben.
Kölcsönhatások Mely gyógyszerek vagy élelmiszerek módosíthatják az Urapidil Stragen hatását
Feltétlenül tájékoztassa kezelőorvosát a jelenleg vagy nemrégiben szedett egyéb gyógyszereiről.
A gyógyszer alkalmazása előtt tájékoztassa kezelőorvosát, ha az alábbi gyógyszerek bármelyikét szedi, mivel ezek kölcsönhatásba léphetnek az URAPIDIL STRAGEN i.v. és ez megváltoztathatja hatékonyságukat, vagy nagyobb valószínűséggel okozhat mellékhatásokat:
- Alfa -blokkoló gyógyszerek, amelyeket prosztata betegség okozta húgyúti problémákra használnak
- Bármilyen gyógyszer, amely csökkenti a vérnyomást
- Beklofén (izomgörcsök kezelésére használják)
- Cimetidin (gyomorsav -termelés gátlására használják)
- Imipramin és neuroleptikumok (depresszió kezelésére használják)
- Kortikoidok (gyulladáscsökkentők, néha "szteroidoknak" is nevezik).
URAPIDIL STRAGEN és alkohol
Vigyázzon, ha alkoholt fogyaszt az URAPIDIL STRAGEN kezelés alatt, mert ez fokozhatja az Urapidil hatását.
Figyelmeztetések Fontos tudni, hogy:
Terhesség és szoptatás
Az URAPIDIL STRAGEN iv. Alkalmazása terhesség alatt nem ajánlott. Nincs megfelelő információ az Urapidil terhes nőknél történő alkalmazásának biztonságosságának értékeléséhez.
Ha a terhesség alatt emelkedik a vérnyomása, és kezelni kell ezzel a gyógyszerrel, a vérnyomáscsökkenésnek fokozatosnak kell lennie, és minden esetben orvosnak kell figyelnie.
Nincs adat az Urapidil anyatejbe történő bejutásáról. Biztonsági okokból a szoptatás nem javasolt az URAPIDIL STRAGEN kezelés alatt.
Ha Ön terhes, szoptat, illetve ha fennáll Önnél a terhesség lehetősége vagy gyermeket szeretne, a gyógyszer alkalmazása előtt beszéljen kezelőorvosával.
A készítmény hatásai a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre
Az URAPIDIL STRAGEN alkalmazása befolyásolhatja a gépjárművezetéshez és a gépek kezeléséhez szükséges képességeket, különösen: - a kezelés kezdetén vagy a kezelés megváltoztatásakor; - alkoholos italok egyidejű fogyasztása esetén. Ha rosszul érzi magát, nem ajánlott gépjárművet vezetni vagy gépeket kezelni a tünetek elmúlásáig. U
A RAPIDIL STRAGEN polipropilénglikolt tartalmaz. Ez az összetevő alkoholszerű tüneteket okozhat.
Az URAPIDIL STRAGEN kevesebb mint 23 mg nátriumot tartalmaz injekciós üvegenként, azaz lényegében "nátriummentes". Ez azt jelenti, hogy akkor is használhatja, ha sószegény diétát tart.
Adagolás, alkalmazás és idő Az Urapidil Stragen alkalmazásának módja: Adagolás
Az URAPIDIL STRAGEN -t mindig az orvos által elmondottaknak megfelelően szedje, és ha azt képzett egészségügyi szakember adta be.
Adagolás
Orvosa az Ön egészségi állapota alapján határozza meg a megfelelő adagolást.
Speciális betegcsoportok
- Alkalmazása 18 év alatti gyermekeknél nem javasolt a biztonságosságra és a hatásosságra vonatkozó információk hiánya miatt.
- Idősebb emberek (65 év felett) esetében szükség lehet a bevitel csökkentésére.
- Ha májbetegsége (súlyos májelégtelensége) van, az adagot csökkenteni kell.
- Ha Ön vesebetegségben (veseelégtelenségben) szenved, vizsgálatokra lehet szükség a vérkeringés ellenőrzésére.
- Ha mechanikai károsodás okozta szívelégtelenségben szenved, különleges óvintézkedéseket kell tenni.
Az alkalmazás módja
Az URAPIDIL STRAGEN -t vénába adják.
A kezelés időtartama
Az URAPIDIL STRAGEN kezelés időtartama nem haladhatja meg a 7 napot.
Túladagolás Mi a teendő, ha túl sok Urapidil Stragen -t vett be?
A túladagolás fő eseménye a vérnyomás hirtelen csökkenése felálláskor, ami szédülést, szédülést vagy ájulást okoz (ortosztatikus hipotenzió). Ebben az esetben a beteget a hátára kell helyezni felemelt lábakkal. Ha a tünetek továbbra is fennállnak, azonnal forduljon orvosához.
Ha bármilyen további kérdése van a gyógyszer alkalmazásával kapcsolatban, kérdezze meg kezelőorvosát.
Mellékhatások Melyek az Urapidil Stragen mellékhatásai?
Mint minden gyógyszer, így ez a gyógyszer is okozhat mellékhatásokat, amelyek azonban nem mindenkinél jelentkeznek.
A kezelés során az alábbi mellékhatások jelentkezhetnek. Forduljon orvosához, aki eldönti, hogy leállítja vagy folytatja a kezelést.
Gyakori: 10 beteg közül legfeljebb 1 beteget érinthet: Hányinger, szédülés és fejfájás.
Nem gyakori: 100 beteg közül legfeljebb 1 beteget érinthet: Palpitáció, fokozott vagy csökkent szívfrekvencia, nyomásérzés a mellkasban és légzési nehézség, hányás, fáradtság és izzadás.
Ritka: 1000 beteg közül legfeljebb 1 beteget érinthet: hosszan tartó és fájdalmas erekció, orrdugulás, allergiás bőrreakciók (viszketés, szokatlan bőrpír, kiütés).
Nagyon ritka: 10 000 -ből legfeljebb 1 beteget érinthet: A vérlemezkék számának csökkenése (alvadó vörösvértestek); gyengeség, nyugtalanság.
Ha bármely mellékhatás súlyossá válik, vagy ha a betegtájékoztatóban felsorolt mellékhatások bármelyikét észleli, kérjük, forduljon orvosához.
Ha Önnél bármilyen mellékhatás jelentkezik, tájékoztassa erről kezelőorvosát, beleértve a betegtájékoztatóban fel nem sorolt bármilyen lehetséges mellékhatást is.
Lejárat és megőrzés
A gyógyszer gyermekektől elzárva tartandó!
A dobozon és az injekciós üvegen feltüntetett lejárati idő (EXP) után ne alkalmazza ezt a gyógyszert. A lejárati idő az adott hónap utolsó napjára vonatkozik.
30 ° C alatt tárolandó.
Az első felbontás / hígítás után
Fizikai és kémiai stabilitása 50 órán keresztül bizonyított 15-25 ° C-on.
Mikrobiológiai szempontból a készítményt azonnal fel kell használni.
Ha nem használják fel azonnal, a tárolás időtartama és körülményei a felhasználó felelőssége, és nem haladhatják meg a 24 órát 2-8 ° C-on, kivéve, ha a feloldást / hígítást ellenőrzött és validált körülmények között hajtották végre.
Csak egyszeri használatra.
Az injekciós üveg első felnyitása után azonnal fel kell használni.
Semmilyen gyógyszert ne dobjon a szennyvízbe vagy a háztartási hulladékba. Kérdezze meg gyógyszerészét, hogy mit tegyen a már nem használt gyógyszereivel. Ez elősegíti a környezet védelmét.
Határidő "> Egyéb információ
Mit tartalmaz az URAPIDIL STRAGEN?
A hatóanyag az Urapidil.
- Egy 5 ml -es ampulla 25 mg Urapidilt tartalmaz.
- Egy 10 ml -es ampulla 50 mg Urapidilt tartalmaz.
- Egy 20 ml -es ampulla 100 mg Urapidilt tartalmaz.
Egyéb összetevők: propilénglikol (lásd 2. pont), nátrium -dihidrogén -foszfát -dihidrát, sósav (37% m / m), dinátrium -foszfát -dihidrát, sósav (3,7% w / w), nátrium -hidroxid (4% w / p) ), Injekcióhoz való víz.
Milyen az URAPIDIL STRAGEN külleme és mit tartalmaz a csomagolás?
Az URAPIDIL STRAGEN 25 mg oldatos injekció ampullában.
Az URAPIDIL STRAGEN 50 mg oldatos injekció ampullában.
Az URAPIDIL STRAGEN 100 mg koncentrátum oldatos infúzióhoz ampullában.
Egy doboz 5 ampullát tartalmaz.
Forrás betegtájékoztató: AIFA (Olasz Gyógyszerügynökség). A tartalom 2016 januárjában jelent meg. A jelenlévő információk nem feltétlenül naprakészek.
A legfrissebb verzióhoz való hozzáféréshez ajánlatos az AIFA (Olasz Gyógyszerügynökség) webhelyét elérni. Jogi nyilatkozat és hasznos információk.
01.0 A GYÓGYSZER MEGNEVEZÉSE -
URAPIDIL STRAGEN
02.0 MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL -
1 ml 5 mg urapidilt tartalmaz.
Az 5 ml -es ampulla 25 mg urapidilt tartalmaz.
A 10 ml -es injekciós üveg 50 mg urapidilt tartalmaz.
A 20 ml -es injekciós üveg 100 mg urapidilt tartalmaz.
A segédanyagok teljes listáját lásd a 6.1 pontban.
03.0 GYÓGYSZERFORMA -
25 mg / 50 mg: oldatos injekció, amely infúzióhoz is hígítható.
100 mg: koncentrátum oldatos infúzióhoz.
Tiszta, színtelen oldat, pH -ja 5,6-6,6.
Látható részecskék nélkül.
04.0 KLINIKAI INFORMÁCIÓK -
04.1 Terápiás javallatok -
Hipertóniás vészhelyzetek (pl. Kritikus vérnyomás-emelkedés), hipertóniás betegség súlyos és nagyon súlyos formái, kezelésre rezisztens magas vérnyomás.
Kontrollált vérnyomáscsökkenés hipertóniás betegeknél a műtét alatt és / vagy azt követően.
04.2 Adagolás és alkalmazás
Hipertóniás vészhelyzetek, súlyos és nagyon súlyos hipertónia formák, valamint kezeléssel szemben ellenálló magas vérnyomás
Intravénás injekció
10-50 mg urapidilt lassan, intravénás injekcióban adnak be állandó vérnyomás-szabályozás mellett. A vérnyomáscsökkentő hatás általában 5 percen belül jelentkezik.
az adminisztrációtól. A 10-50 mg urapidil injekcióját meg lehet ismételni a vérnyomás alakulásával összefüggésben.
Az intravénás infúziót vagy fecskendőpumpát az injekcióval elért vérnyomásszint fenntartására használják.
A gyógyszer beadás előtti hígítására vonatkozó utasításokat lásd a 6.6 pontban.
A maximális kompatibilis mennyiség 4 mg urapidil / ml oldatos infúzió.
Az alkalmazás sebessége: Az infúzió sebességét az egyéni vérnyomáshelyzet határozza meg. Az ajánlott kezdő adag infúziós sebessége: 2 mg / perc.
Fenntartó adag: Átlagosan 9 mg / óra, 250 mg urapidilre vonatkoztatva, 500 ml infúziós oldathoz adva, ami 1 mg -nak felel meg = 44 csepp = 2,2 ml.
Kontrollált vérnyomáscsökkenés műtét közben és / vagy azt követően fellépő vérnyomás -emelkedés esetén
Az intravénás infúziót vagy fecskendőpumpát az injekcióval elért vérnyomásszint fenntartására használják.
Adagolás
jegyzet
Urapidil Stragen i.v. intravénásan adják be infúzióval vagy injekcióval a betegnek fekvő helyzetben. Az adag beadható egy vagy több injekció formájában vagy lassú intravénás infúzió formájában. Az injekciók kombinálhatók ezt követő lassú infúzióval.
Idős államporgárok
Idősebb betegeknél a vérnyomáscsökkentő gyógyszereket óvatosan és kezdetben kisebb adagokban kell alkalmazni, mivel ezeknél a betegeknél az ilyen készítményekkel szembeni érzékenység gyakran módosul.
Károsodott vese- és / vagy májfunkciójú betegek
Károsodott máj- és vesefunkciójú betegeknél szükség lehet az urapidil adagjának csökkentésére.
Gyermekpopuláció
Az urapidil biztonságosságát és hatásosságát intravénás alkalmazásra 0-18 éves gyermekeknél nem igazolták, az adagolásra vonatkozó javaslat nem adható.
A kezelés időtartama
Toxikológiai szempontból biztonságosnak tekinthető 7 napos kezelési időszakban; általában ezt az időszakot nem szabad túllépni parenterális vérnyomáscsökkentő gyógyszerekkel. Ismételt parenterális kezelés lehetséges, ha a vérnyomás ismét emelkedik.
Lehetséges az akut parenterális terápia átfedése az orális vérnyomáscsökkentő szerekkel történő folyamatos kezelésre való áttéréssel.
04.3 Ellenjavallatok -
Az Urapidil Stragen nem alkalmazható a hatóanyaggal vagy bármely segédanyaggal szembeni túlérzékenység (allergia) esetén. Urapidil Stragen i.v. nem használható az isthmus aorta szűkülete vagy arteriovenosus shunt esetén (kivéve a nem hemodinamikailag aktív dialízis shunt).
04.4 Különleges figyelmeztetések és a használattal kapcsolatos óvintézkedések -
Használati óvintézkedések
- szívelégtelenségben, amelyet mechanikai eredetű funkcionális károsodás okoz, például az aorta vagy a mitrális billentyű szűkülete, tüdőembólia vagy a szívműködés gyengülése perikardiális betegség miatt;
- májműködési zavarban szenvedő betegeknél;
- Közepesen súlyos vagy súlyos vesekárosodásban szenvedő betegeknél;
- Idős betegeknél;
- Cimetidinnel egyidejűleg kezelt betegeknél (lásd 4.5 pont)
"Kölcsönhatások más gyógyszerekkel és más interakciók").
Ha az urapidilt nem adták be első vonalbeli vérnyomáscsökkentő szerként, akkor ezt addig nem szabad alkalmazni, amíg a korábban beadott vérnyomáscsökkentő gyógyszer hatása el nem múlik.
A túl gyors vérnyomásesés bradycardiát vagy szívmegállást okozhat.
Az Urapidil Stragen intravénás adagolásakor a propilénglikol jelenléte miatt alkoholszerű tünetek figyelhetők meg.
Ez a gyógyszer kevesebb, mint 1 mmol (23 mg) nátriumot tartalmaz adagonként, lényegében nátriummentes.
04.5 Kölcsönhatások más gyógyszerekkel és egyéb interakciók -
Az urapidil vérnyomáscsökkentő hatását fokozhatja az alfa -receptor -blokkolók, beleértve az urológiai állapotok kezelésére alkalmazott szereket, az értágítókat és más vérnyomáscsökkentő szereket, a kimerült állapotokat (hasmenés, hányás) és az alkoholt.
Az urapidil és a baklofen kombinációját nagyon alaposan meg kell fontolni, mivel a baklofen fokozhatja a vérnyomáscsökkentő hatást.
A cimetidin egyidejű alkalmazása gátolja az urapidil metabolizmusát.Az urapidil koncentrációja a szérumban 15%-kal emelkedhet, ezért fontolóra lehet venni az adag csökkentését.
A következő egyidejű alkalmazásokat kell figyelembe venni:
- imipramin (vérnyomáscsökkentő hatás és ortosztatikus hipotenzió kockázata);
- neuroleptikumok (vérnyomáscsökkentő hatás és ortosztatikus hipotenzió kockázata);
- kortikoidok (a vérnyomáscsökkentő hatás csökkentése nátrium -vízvisszatartás révén).
Mivel az ACE -gátlók egyidejű alkalmazásáról még nem állnak rendelkezésre megfelelő információk, ez a kezelés jelenleg nem javasolt.
04.6 Terhesség és szoptatás -
Terhesség
Az Urapidil Stragen alkalmazása terhesség alatt nem ajánlott. Nincs megfelelő információ az urapidil terhes nőkön történő alkalmazásáról.
Állatkísérletek teratogenitás nélküli reprodukciós toxicitást mutattak (5.3 pont). A korlátozott vizsgálatok miatt a lehetséges kockázat emberben nem ismert.
Etetési idő
Az anyatejbe történő kiválasztódásra vonatkozó adatok hiánya miatt a szoptatás nem javasolt urapidil -kezelés esetén.
04.7 Hatások a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre -
Ez a gyógyszer kismértékben befolyásolja a gépjárművezetéshez és gépek kezeléséhez szükséges képességeket.
Az egyéni válasz a kezelésre betegekenként eltérő lehet, ez különösen igaz a kezelés kezdetén, a kezelés megváltoztatásakor vagy alkohollal történő egyidejű alkalmazásakor.
04.8 Nemkívánatos hatások -
Az alábbi mellékhatások közül sok a hirtelen vérnyomásesés következménye, de a tapasztalatok azt mutatják, hogy percek alatt eltűnnek, még a lassú infúzió során is; azonban a nemkívánatos hatások súlyosságával összefüggésben a kezelés felfüggesztését is meg kell fontolni.
04.9 Túladagolás -
Tünetek
A túladagolás tünetei: szédülés, ortosztatikus hipotenzió, összeomlás, fáradtság és csökkent reakciósebesség.
Túladagolásos kezelés
A túlzott nyomásesést a lábak felemelésével vagy a vértérfogat helyreállításával lehet enyhíteni. Ha ezek az intézkedések nem megfelelőek, az érszűkítő gyógyszert lassan, intravénásan kell beadni, figyelve a vérnyomást. Nagyon ritka esetekben intravénás katekolamin -injekció szükséges (pl. -1,0 izotóniás nátrium -klorid -oldattal 10 ml -re hígítva).
05.0 FARMAKOLÓGIAI TULAJDONSÁGOK -
05,1 "Farmakodinamikai tulajdonságok -
Farmakoterápiás csoport: Perifériás hatású antiadrenerg anyagok, alfa-adrenerg receptor blokkolók.
ATC kód: C02CA06
Az Urapidil csökkenti a szisztolés és a diasztolés nyomást a perifériás ellenállás csökkentésével.
A pulzus nagyrészt állandó.
A szívteljesítmény változatlan: bár növekedhet azokban az esetekben, amikor az utóterhelés növekedése miatt csökken.
A cselekvés mechanizmusa
Az Urapidil központi és perifériás hatással is rendelkezik.
• Perifériás: Az Urapidil elsősorban a posztszinaptikus alfa -receptorokat blokkolja, következésképpen gátolja a katekolaminok érszűkítő hatását.
• Központi szinten: Az Urapidil központi hatással is rendelkezik, és modulálja a keringési rendszert szabályozó agyközpontok tevékenységét. Így gátolja a szimpatikus idegrendszer tónusának reflexemelkedését, vagy csökkenti a szimpatikus hangot.
05,2 "Farmakokinetikai tulajdonságok -
25 mg urapidil intravénás beadása után kétfázisú tendencia figyelhető meg koncentrációjában a vérben (kezdeti eloszlási fázis, utolsó eliminációs fázis). Az eloszlási fázis felezési ideje körülbelül 35 perc, az eloszlási térfogat 0,8 (0,6-1,2) l / kg.
Az urapidil elsősorban a májban metabolizálódik. A fő metabolit a fenilgyűrű 4. helyzetében lévő urapidil -hidroxilezett, amely nem rendelkezik érezhető vérnyomáscsökkentő hatással. Az O-dezmetil-urapidil metabolit közel azonos biológiai aktivitással rendelkezik, mint az urapidil, de csak kis mennyiségben van jelen.
Az urapidil és metabolitjai emberben eliminálódnak, akár 50-70% -ban a vesén keresztül; amelynek a beadott adag 15% -a farmakológiailag aktív urapidil; a többi, főleg para-hidroxilezett urapidilből áll, vérnyomáscsökkentő hatás nélkül, a széklettel választódik ki.
A szérum felezési ideje intravénás bolus beadás után 2,7 óra (1,8-3,9 óra). Az urapidil plazmafehérje-kötődése humán szérumban 80% in vitro. Az urapidil plazmafehérjékhez való viszonylag alacsony kötési affinitása megmagyarázhatja, hogy miért nincs ismert kölcsönhatás az urapidil és az erősen plazmafehérje -kötő gyógyszerek között.
Idős betegeknél és kifejezett máj- és / vagy veseelégtelenségben szenvedő betegeknél az urapidil eloszlási térfogata és clearance-e csökken, a plazma felezési ideje pedig hosszabb.
05.3 A preklinikai biztonságossági adatok -
Akut toxicitás
Urapidil -hidrokloriddal végzett vizsgálatokat egereken és patkányokon végeztek az akut toxicitás vizsgálatára.
Az LD50 (urapidil -bázisra utalva) orális adagolás után 508 és 750 mg / testtömeg -kg, intravénás beadása után pedig 140 és 260 mg / testtömeg -kg között van. A toxicitást elsősorban nyugtatás, ptosis, csökkent mozgékonyság, védőreflex és hipotermia, légszomj, cianózis, remegés és görcsök formájában figyelték meg.
Krónikus toxicitás / Szubkrónikus toxicitás
Krónikus toxicitási vizsgálatokat végeztek patkányokon, étkezés után, több mint 6 és 12 hónapig, 250 mg / testtömeg -kilogramm / nap dózisig. Szedációt, ptosist, csökkent súlygyarapodást, a menstruációs ciklus meghosszabbodását és a méh súlyának csökkenését figyelték meg.
Krónikus toxicitást figyeltek meg kutyákon 6 és 12 hónapos vizsgálatok során, legfeljebb 64 mg / testtömeg / nap dózisban. A 30 mg / ttkg / nap feletti adagok szedációt, hipersalivációt és remegést okoztak. Klinikai vagy szövettani elváltozásokra utaló jeleket nem észleltek.
Lehetőség genetikai mutáció és tumor kiváltására
Bakteriális vizsgálatokban (AMES teszt, gazdaszervezet által közvetített vizsgálat), humán limfocitákon és egér csontvelő metafázisos vizsgálatokon az urapidil nem mutatott mutagén tulajdonságokat.
Az egereken és patkányokon végzett karcinogén vizsgálatok 18 és 24 hónapos korban nem mutattak ki releváns jelzést az emberekben a tumor indukálására. Patkányokon és egereken végzett speciális vizsgálatokban az urapidil hozzájárult a prolaktin szintjének növekedéséhez, rágcsálóknál a prolaktin szintjének növekedése az emlőszövet növekedéséhez vezet. Tekintettel a hatásmechanizmusról ismert tényekre, ez a hatás nem várható terápiás dózisban részesülő emberekben, és nem határozható meg klinikai vizsgálatok során.
Reprodukciós toxicitás
Patkányokon, egereken és nyulakon végzett reprodukciós toxicitási vizsgálatok nem mutattak utalást a teratogén hatásra.
Patkányokon és nyulakon végzett vizsgálatok nem mutatták ki az urapidil reprodukciós toxicitását. A mellékhatások a patkányok terhességi arányának csökkenését eredményezték; nyulakban a testtömeg, valamint az élelmiszer- és vízbevitel csökkenésében; az élő nyúlmagzatok százalékos arányának csökkenése; valamint a perinatális magzatok túlélési arányának csökkenése és az újszülött patkányok testtömegének növekedése.
A reprodukciós vizsgálat megállapította, hogy a nőstény patkányok menstruációs ciklusa meghosszabbodott, amint azt a krónikus toxicitási vizsgálat is megállapította. Ezt a hatást, akárcsak a méh súlyának csökkenését a krónikus vizsgálatban, a prolaktin szintjének növekedésének tekintik, amely rágcsálóknál jelentkezik az urapidil -kezelés után. A nők termékenysége nincs veszélyben.
A fajok közötti jelentős különbségek miatt azonban ezek az eredmények nem tekinthetők alkalmazhatók az emberekre. Hosszú távú klinikai vizsgálatok során nem lehetett megállapítani, hogy a nők milyen hatással lennének az agyalapi mirigy tengelyére.
06.0 GYÓGYSZERÉSZETI INFORMÁCIÓK
06.1 Segédanyagok -
Propilén-glikol,
Nátrium -dihidrogén -foszfát -dihidrát,
Sósav (37 tömeg%),
Dinátrium -foszfát -dihidrát,
Sósav (3,7% w / w),
Nátrium -hidroxid (4 tömeg%),
Injekcióhoz való víz.
06.2 Inkompatibilitás "-
Ez a gyógyszer nem keverhető más gyógyszerekkel, kivéve a 6.6 pontban említetteket.
A következő hatóanyagokat [vagy feloldásra / hígításra szolgáló oldatot] nem szabad egyidejűleg beadni:
lúgos oldatok injekcióhoz és infúzióhoz.
Ez zavarosságot vagy pelyhesedést okozhat.
06.3 Érvényességi idő "-
3 év.
Az első felbontás / hígítás után:
Fizikai és kémiai stabilitása 50 órán keresztül bizonyított 15-25 ° C-on.
Mikrobiológiai szempontból a készítményt azonnal fel kell használni.
Ha nem használják fel azonnal, a tárolás időtartama és körülményei a felhasználó felelőssége, és nem haladhatják meg a 24 órát 2-8 ° C-on, kivéve, ha a feloldást / hígítást ellenőrzött és validált körülmények között hajtották végre.
06.4 Különleges tárolási előírások -
30 ° C alatt tárolandó.
A hígított gyógyszer tárolási feltételeit lásd a 6.3 pontban.
06.5 A közvetlen csomagolás jellege és a csomagolás tartalma -
Átlátszó üvegcsék (I. típus, Ph. Eur.)
Kiszerelés: 5 ampulla.
06.6 Használati és kezelési útmutató -
A 100 mg -os injekciós üveg infúzióval stabilizálhatja a vérnyomást. A kezdeti kezeléshez 25 mg és 50 mg urapidilt tartalmazó ampullák állnak rendelkezésre. Ezek az adagok hígítás után intravénás infúzióhoz is használhatók.
A hígítás aszeptikus körülmények között történik.
Az oldatot beadás előtt szemrevételezéssel ellenőrizni kell, hogy nincsenek -e benne részecskék és nem színeződtek -e el, csak tiszta, színtelen oldatokat szabad használni.
A hígított oldat elkészítése
- Intravénás infúzió:
Adjon 250 mg urapidilt (2 üveg 100 mg urapidilt + 1 üveg 50 mg urapidilt) 500 ml egyik kompatibilis oldószerhez.
- Fecskendő szivattyú:
Fecskendőpumpa segítségével szívjon fel 100 mg urapidilt, és hígítsa fel 50 ml -es térfogatra valamelyik kompatibilis oldószerrel.
Kompatibilis oldószerek a hígításhoz
- 9 mg / ml (0,9%) nátrium -klorid oldatos infúzió
- Glükóz 50 mg / ml (5%)
- Glükóz 100 mg / ml (10%)
Csak egyszeri használatra.
A fel nem használt oldatot és a "tasakokat / tasakokat" megfelelően kell megsemmisíteni a helyi előírásoknak megfelelően.
07.0 A „FORGALOMBA HOZATALI ENGEDÉLY” TULAJDONOSA -
Stragen Nordic A / S
Helsingorsgade 8C
DK-3400 Hillerád
Dánia
08.0 A FORGALOMBA HOZATALI ENGEDÉLY SZÁMA -
AIC n.040876017 - "25 mg oldatos injekció" 5 5 ml -es üveg ampulla
AIC n.040876029 - "50 mg oldatos injekció" 5 db 10 ml -es üveg ampulla
AIC n.040876031 - "100 mg koncentrátum oldatos infúzióhoz" 5 üveg ampulla
20 ml -re
09.0 AZ ELSŐ ENGEDÉLYZÉS ÉS A JÓVÁHAGYÁS MEGÚJÍTÁSÁNAK DÁTUMA -
13.05.2013
10.0 A SZÖVEG FELÜLVIZSGÁLÁSÁNAK DÁTUMA -
13.05.2013






















.jpg)