Általánosság
„Adj lázat, és minden betegséget meggyógyítok”: ez a kijelentés, amelyet Hippokratész görög orvosnak (i. E. 400) tulajdonítanak, azt tanúsítja, hogy az ember régóta érti a hő terápiás lehetőségeit.
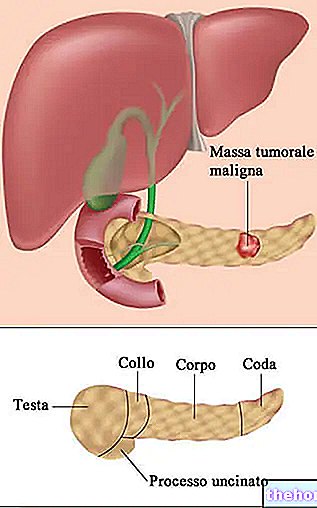
Az első dokumentált bizonyíték a magas hőmérséklet lehetséges gyógyító hatásáról a daganatok kezelésében 1866 -ból származik, amikor Busch német orvos megfigyelte a szarkóma teljes remisszióját egy beteg arcán, miután ismételten magas lázba került.

Ma ennek a technikának a lehetséges terápiás előnyei miatt a hipertermiát az onkológia negyedik pillérének ismerik el.
Mi az onkológiai hipertermia?
Az onkológiai hipertermia a rosszindulatú daganatok kezelésére szolgáló klinikai kezelés, amely önmagában vagy gyakrabban alkalmazható sugárterápiával és kemoterápiás kezelésekkel kombinálva. Jelenleg valójában ezt a technikát nem annyira alternatívaként, hanem kiegészítőként alkalmazzák. más rákellenes kezelések, ez az összefüggés lehetővé teszi a terápiás hatékonyság kölcsönös megerősítését. Ezenkívül a hipertermiával való összefüggés lehetővé teszi a kemoterápia és a sugárzás dózisának csökkentését, jelentősen csökkentve a standard terápiákkal kapcsolatos mellékhatásokat.
A hipertermia típusai
A hipertermia terápiás hatása a daganatok kezelésére különböző megközelítések és technológiák segítségével kihasználható.
A daganatformák, amelyek jól reagáltak a hipertermiára:
- Melanoma és a bőrrák más formái
- Mellrák
- Lágyszöveti szarkóma
- Húgyhólyagrák
- Fej- és nyaki karcinómák
- Méhnyak- és petefészekrák
- Prosztata rák
- Végbélrák
- A hónalj vagy a mellkas karcinómái
A hőmérséklet és a hőhatás időtartama a két alapvető mennyiség, amelyet kalibrálni kell a kívánt terápiás eredmény elérése érdekében. Az elért hőmérséklet és a hő alkalmazásának ideje mellett azonban nagyon fontos a fűtést előállító forrás és az alkalmazás helyének értékelése. Például mikrohullámok, rádiófrekvenciák, nanorészecskék, ultrahangok, lézerek használhatók stb., külsőleg vagy belsőleg a testre helyezve.
Mindezeket a változókat az onkológus választja ki a különböző klinikai esetek jellemzői alapján.
Eredmények
Az onkológiában a rosszindulatú daganatból való gyógyulás esélyei sok tényezőtől függenek, például a daganat típusától és stádiumától, méretétől és helyétől, a beteg korától és általános egészségi állapotától.
Mindezeket szem előtt tartva számos tanulmány kimutatta, hogy a hipertermia kiváló adjuvánst jelent a daganatok klasszikus kezelési technikáihoz, és kevés ellenjavallatot jelent a betegek számára.
Bizonyos típusú daganatok esetében, amelyek a sugárterápiát (és / vagy kemoterápiát) hipertermiához társítják, a teljes remissziós arány és / vagy a túlélési arány 30 és 100% közötti növekedését érte el 2 és 5 éves korban, összehasonlítva az önmagában alkalmazott sugárterápiával (és / vagy kemoterápia). Egyes rákos megbetegedések, például a végbélrák esetében a kezelési eredmények még biztatóbbnak bizonyultak (az ötéves túlélési arány + 500% -a).
Klasszikus hipertermia 41-45 ° C
A klasszikus onkológiai hipertermia célja a rákos sejtek felmelegedése a környező egészséges szövetek károsítása nélkül.
- Ha a hőmérséklet 41-43 ° C között van (enyhe hipertermia) a fő cél a daganat sugárkezelésre és / vagy kemoterápiás kezelésre való érzékenységének növelése.
- Ha az elért hőmérséklet 43 és 46 ° C között van, a hő közvetlen hatása a ráksejtek elpusztítására egyre fontosabbá válik.
Az esettől függően a klasszikus hipertermia kezelés átlagosan 40-60 percig tart, és hetente kétszer -háromszor megismétlődik. A gyakoribb kezelések valójában hajlamosak hőrezisztenciát (vagy ha úgy tetszik, hőtoleranciát) okozni a rákos sejtekben, így jobban ellenállnak a magas hőmérsékletnek.
Az esettől függően a hőforrás különböző méretű lehet, és különböző mélységekben, különböző szervekben vagy az emberi test anatómiai részeiben helyezkedhet el. Például a modern hipertermia technikák között lehetőség van arra is, hogy mikrohullámú antennákat közvetlenül a szubkutiszba ültessünk.
Hogyan működik
A tumorsejtek közvetlen károsodása
Az onkológiai hipertermia hatékonysága a daganatos szövetek kaotikus angiogenezisén alapul, alapvetően a tumor mikrokörnyezete szinte mindig kaotikus és rendezetlen érrendszeri állványt mutat; ennek következtében a nagy daganatterületek (különösen a központi tömeg) nem kapnak elegendő mennyiségű vért és oxigént. Az erek ezen elváltozásai miatt a neoplasztikus tömeg nem képes eloszlatni a hőt, mint a normál szövetek; más szóval a daganatok általában sokkal több meleget szenvednek, mint az egészséges szövetek, mert egyes területeik kevés vért kapnak (ami igazi hűtőfolyadékként működik); ugyanezen okból ezek a területek már szenvednek az oxigén- és tápanyaghiánytól, valamint a salakanyagok bőségétől (túlsavasodás).
A hipertermia által leadott hő károsítja a plazmamembránt, a sejtvázat és a sejtmagot; ha a hipertermia mértéke és időtartama elegendő, ez a károsodás közvetlenül a tumorsejt halálához vezet. A közvetlen károsodás jelentős lesz> 43 ° C hőmérsékleten: a közvetett károsodás, amelyet rövidesen látni fogunk, inkább az úgynevezett "enyhe hipertermiára" (42-43 ° C) jellemző.
KÖZVETLEN KÁROSÍTÁS: BEÁLLÍTOTT HYPERTHERMIA
Testünk úgy reagál a helyi hőmérséklet -emelkedésre, hogy fokozza a véráramlást az érintett területre. Ily módon a nagyobb mennyiségű keringő vér "elnyeli" a hőt, megóvva a szöveteket a termikus károsodástól. Ez a válasz a daganat szintjén is előfordul, így - a sajátos érrendszeri dezorganizáció határain belül - a kismértékű hőmérséklet -emelkedésnek kitett tumorsejtek nagyobb mennyiségű vért és oxigént kapnak:
- daganatellenes szerek lehetnek jelen a vérben, amelyek a hipertermia által kiváltott értágulatnak köszönhetően könnyebben elérik a kevésbé vaszkuláris daganatos területeket; ezen gyógyszerek hatását a sejtes (a plazmamembrán fokozott permeabilitása) és az enzimatikus hő okozta elváltozások (fehérje denaturáció).
Ha a daganat tömegének hőmérséklete meghaladja a 43 ° C -ot, ezzel szemben a tumor véráramának csökkenését regisztrálják, és ennek következtében a gyógyszermolekulák "csapdába esnek".
A hipertermia-kemoterápia kombináció előnyeit több tanulmány is megerősítette. A daganatellenes gyógyszerek, mint a Melphalan, Bleomycin, Adriamycin, Mitomycin C, Nitrosuree, Cisplatin, hatékonyabbak, ha hipertermia alatt adják be. E tekintetben azonban hangsúlyozni kell, hogy nem minden ismert kemoterápiás gyógyszer fokozza hatékonyságát, ha hipertermikus környezetben alkalmazzák. - A daganatszövet nagyobb oxigénellátása felerősíti a sugárterápia hatásait, amelyek elsősorban a sugárzás által előidézett reaktív oxigénfajok (szabad gyökök) által kiváltott DNS -károsodásokon alapulnak. sejtkompromisszum, amely a hipertermia által korábban okozott károkhoz kapcsolódik.
A hipertermia és a sugárkezelés közötti kölcsönös befejezés és megerősítés az abból fakad, hogy:- a hipertermia által kiváltott károsodás nagyobb azokon a területeken, ahol alacsony a vaszkularizáció (amelyek nem tudják hatékonyan elvezetni a hőt), például a daganatos csomó hipoxiás központi magjában;
- a sugárterápia által okozott károsodás ehelyett nagyobb azokon a területeken, ahol magas a vaszkularizáció (oxigénben gazdagabb), például a daganatcsomó perifériás köpenyterületein;
- a két kezelés a sejtciklus különböző fázisaiban végzi maximális károsító hatását a daganatra, és ebben az értelemben is kiegészíti egymást.
A maximális terápiás nyereséget úgy tűnik, ha a hipertermikus kezelést a sugárterápia után egy vagy két órán belül gyakorolják. Ami a termokemoterápiát illeti, a két kezelés egyidejűleg is elvégezhető.
Az onkológiai hipertermia hozzájárulhat a tumor tömegének csökkentéséhez, tekintettel a sebészeti eltávolításra.Előnyei vannak a fájdalomcsillapító hatás tekintetében is (a fájdalom csökkentése, amelyet a szövetek neoplasztikus tömeg által történő összenyomása vált ki).
A hipertermia egyéb formái
ÖSSZES TEST-HIPERTHERMIA
Ahogy a neve is sugallja, a hipertermia ezen formája biztosítja az egész szervezet felmelegedését. A cél ebben az esetben nem a daganat tömegének közvetlen megsemmisítése, hanem annak közvetett remissziójának meghatározása az immunrendszer erősítésével. Quest " Ez utóbbinak tulajdonképpen belső képessége van a rákos sejtek elpusztítására, és ez a képesség rendkívül megnő a magas testhőmérséklet mellett.
A teljes test hipertermia célja egy mesterséges láz kiváltása, amely 39-41 ° C körüli lázas rohamot szimulál. Ebben a tekintetben termikus vagy vízzel borított kamrák használhatók.
A teljes test felhasználása többnyire a diffúz áttétek kezelésére szolgáló kísérleti környezetre korlátozódik. A technika megköveteli a beteg szoros megfigyelését, hogy elkerülje a hipertermia okozta károsodásokat, amelyek szintén nagyon súlyosak lehetnek. Ez egyben adjuváns terápia is, ezért más rákellenes terápiákkal együtt kell alkalmazni.
INTERSTIZIÁLIS HYPERTHERMIA
Amint azt a brachyterápia esetében láthatjuk - ahol kis radioaktív forrásokat ültetnek be a célszövetbe -, az intersticiális hipertermia olyan eszközök beültetését foglalja magában, amelyek képesek "helyi hipertermiát generálni". Ebből a szempontból antennákat használnak, amelyek a mikrohullámú ellátásnak köszönhetően melegítenek.
INFUSIONAL HYPERTHERMIA és PERFUSION HYPERTHERMIA
Az intraperitoneális infúziós hipertermia a peritoneális mosás és gyógyászati oldatok magas hőmérsékleten történő használatán alapul. Nehezen kezelhető peritoneális daganatok, például peritoneális mesothelioma és gyomorrák esetén alkalmazzák. Más hipertermiás technikák ugyanezen az elven alapulnak, és magukban foglalják a terápiás oldatok infúzióját más üregekbe, például a mellhártya vagy a hólyag üregébe.
A perfúziós hipertermia esetén a testen kívüli keringést alkalmazzák, a vér egy részének felmelegítésével, majd a kemoterápiás gyógyszerek hozzáadásával történő újbóli bevezetésével, hogy magas hatóanyag-koncentrációt érjenek el a perfundált szövetben.
ABLATÍV HYPERTHERMIA
Ebben az esetben a hőmérséklet sokkal magasabb (50-100 ° C), de csak néhány percig alkalmazzák. Az ilyen hőmérsékletek képesek a kezelt szövetek azonnali és teljes nekrózisát előidézni. A hőt váltakozó elektromos áram elektródákon keresztül történő alkalmazása vagy lézer vagy elektromágneses sugárzás segítségével hozzák létre, közvetlenül a daganat tömegére (invazív kezelés). A fő nehézséget a daganatot körülvevő egészséges szövetek megőrzése jelenti.
Bár ez a technika kihasználja a hő terápiás hatását, a hatásmechanizmus szempontjából túlmutat a hipertermia hagyományos fogalmán.
ÚJ FEJLESZTÉSEK A "HIPERTHERMIA TERÜLETÉN"
A hipertermia tudománya folyamatosan fejlődik, hogy egyre szelektívebb kezeléseket fejlesszen ki a rákos sejtek elpusztítása érdekében, anélkül, hogy károsítaná az egészségeseket.
A legújabb fejlemények a mágneses rezonancia szkennerek (a különböző daganatterületek hőmérsékletének értékelése) alkalmazásával végzett nem invazív hőmérést, a hipertermia mágneses folyadékot és a hőérzékeny liposzómák használatát érintik. Az utóbbiak lipidvezikulákba zárt gyógyszerek, amelyek normál testhőmérsékleten stabilak, de képesek 40-43 ° C hőmérsékleten felszabadítani tartalmukat; ezért ezek a gyógyszerek ideális kombinációt képviselnek a regionális hipertermia kezelésekkel.
Korlátok
A hipertermia hatásmechanizmusainak megértése és az ebből adódó lehetséges előnyök a daganatok kezelésében az olvasó túlzott lelkesedéséhez vezethet az ilyen típusú kezelés iránt.
Bár a hatékonyság tisztességes bizonyítéka alátámasztja, a hipertermia alkalmazása az onkológiában megtart néhány kritikus kérdést. Először is, a klinikai gyakorlatban lehetnek ellenjavallatok vagy korlátok, amelyek kivitelezhetetlenné teszik a beavatkozást; egyes technikák például valós többé -kevésbé invazív sebészeti beavatkozásokat írnak elő; mások még mindig csak a kísérleti környezetre korlátozódnak. a hőkibocsátással, a behatolási mélységgel, a termikus mezők homogenitásával és a helyes termikus adagolás szükségességével kapcsolatos technikusok az egészséges szövetek károsodásának elkerülése érdekében. E tekintetben további tanulmányok és technológiai fejlesztések kívánatosak hatékony protokollokat dolgoznak ki és szabványosítanak, amelyeket különböző klinikai helyzetekben kell alkalmazni.