Hatóanyagok: Tolterodina
Detrusitol 1 mg és 2 mg filmtabletta
A Detrusitol csomagbetétek a következő csomagolási méretekhez kaphatók:- Detrusitol 1 mg és 2 mg filmtabletta
- Detrusitol Retard 2 mg és 4 mg retard kemény kapszula
Miért használják a Detrusitolt? Mire való?
A Detrusitol hatóanyaga a tolterodin. A tolterodin az antimuszkarin gyógyszerek csoportjába tartozik.
A Detrusitolt a hiperaktív hólyag szindróma tüneti kezelésére használják. Ha hiperaktív húgyhólyag -szindrómában szenved, észreveszi, hogy képtelen ellenőrizni a vizelést, és szükség van arra, hogy gyakran rohanjon a WC -hez figyelmeztető jelek nélkül.
Ellenjavallatok Amikor a Detrusitolt nem szabad használni
Ne szedje a Detrusitolt
- - ha allergiás (túlérzékeny) a tolterodinra vagy a gyógyszer egyéb összetevőjére
- - ha nehézségei vannak a vizelet kivezetésével a hólyagból (vizeletvisszatartás)
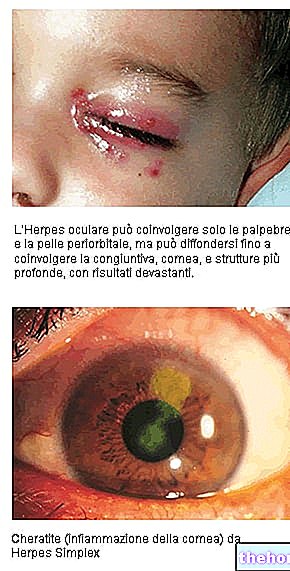
- Ha ellenőrizetlen keskeny szögű glaukómája van (magas szemnyomás, látásvesztéssel, nem megfelelő kezeléssel)
- - ha myasthenia gravisban szenved (túlzott izomgyengeség)
- Ha súlyos fekélyes vastagbélgyulladása (fekélye és vastagbélgyulladása) van
- Ha toxikus megakolonja van (akut vastagbél -tágulat)
Az alkalmazással kapcsolatos óvintézkedések Mit kell tudnia a Detrusitol szedése előtt
A Detrusitol fokozott elővigyázatossággal alkalmazható
- - ha nehézségei vannak a vizeletürítéssel és / vagy rossz a vizeletáramlása
- Ha gyomor -bélrendszeri rendellenességei vannak, amelyek befolyásolják az élelmiszer áthaladását és / vagy emésztését.
- - ha veseproblémái vannak (veseelégtelenség)
- Ha májproblémái vannak
- - ha idegbetegségei vannak, amelyek befolyásolják a vérnyomást, a bélrendszert vagy a szexuális funkciót (az autonóm idegrendszer bármely neuropátiája).
- Ha hiatus hernia (hasi szerv sérv) van
- Ha csökkent bélmotilitásban szenved, vagy súlyos székrekedésben szenved (csökkent gyomor-bélrendszeri motilitás)
- Ha szívproblémái vannak, például:
- A szív megváltozott nyomkövetése (EKG)
- Lassú szívverés (bradycardia)
- Fontos szívbetegségek, például:
- kardiomiopátia (a szívizom gyengülése)
- miokardiális ischaemia (csökkent véráramlás a szívbe),
- aritmia (szabálytalan szívverés)
- szív elégtelenség
- Ha vérében különösen alacsony a kálium (hypokalaemia), a kalcium (hypocalcaemia) vagy a magnézium (hypomagnesaemia) szintje.
Ha ezek közül bármelyik vonatkozik Önre, a kezelés megkezdése előtt tájékoztassa kezelőorvosát vagy gyógyszerészét.
Kölcsönhatások Mely gyógyszerek vagy élelmiszerek módosíthatják a Detrusitol hatását
A tolterodin, a Detrusitol hatóanyaga kölcsönhatásba léphet más gyógyszerekkel.
Nem javasolt a tolterodin alkalmazása:
- bizonyos antibiotikumok (például eritromicint, klaritromicint tartalmaznak);
- gombás fertőzések kezelésére szolgáló gyógyszerek (pl. ketokonazol, itrakonazol);
- a HIV kezelésére használt gyógyszerek.
A Detrusitolt óvatosan kell alkalmazni, ha együtt alkalmazzák:
- olyan gyógyszerek, amelyek befolyásolják az étkezést (például metoklopramidot és ciszapridot tartalmaznak)
- szabálytalan szívverés kezelésére szolgáló gyógyszerek (például amiodaront, szotalolt, kinidint, prokainamidot tartalmaznak)
- más, a Detrusitolhoz hasonló hatásmechanizmusú gyógyszerek (antimuszkarin tulajdonságok) vagy a Detrusitollal ellentétes hatásmechanizmusú gyógyszerek (kolinerg tulajdonságok). További kérdéseivel forduljon orvosához.
Tájékoztassa kezelőorvosát, ha jelenleg vagy nemrégiben bármilyen más gyógyszert szed, beleértve azokat is, amelyekre nincs szüksége orvosi rendelvényre.
A Detrusitol egyidejű bevétele étellel és itallal
A Detrusitol étkezés előtt, után vagy közben is bevehető.
Figyelmeztetések Fontos tudni, hogy:
Terhesség és szoptatás
Terhesség
A Detrusitolt nem szabad terhesség alatt szedni. Azonnal forduljon orvosához, ha terhes, ha úgy gondolja, hogy terhes, vagy ha terhességet tervez.
Etetési idő
Nincsenek adatok a tolterodin kiválasztódásáról az anyatejben.
A Detrusitol alkalmazása során a szoptatás nem ajánlott.
Mielőtt bármilyen gyógyszert elkezdene szedni, beszéljen kezelőorvosával vagy gyógyszerészével.
A készítmény hatásai a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre
A Detrusitol szédülést, fáradtságot vagy látásromlást okozhat. A gépjárművezetéshez és gépek kezeléséhez szükséges képességek károsodhatnak.
Adagolás és alkalmazás A Detrusitol alkalmazása: Adagolás
Adagolás
A Detrusitolt mindig az orvos által elmondottaknak megfelelően szedje. Ha bizonytalan, beszéljen kezelőorvosával vagy gyógyszerészével.
A szokásos adag naponta kétszer egy 2 mg -os tabletta, kivéve azokat a betegeket, akiknek vese- és májproblémái vannak, vagy mellékhatásokat tapasztalnak, amelyek esetén kezelőorvosa csökkentheti az adagot napi 1 mg -ra.
A Detrusitol gyermekeknek nem ajánlott.
A tablettákat szájon át kell bevenni, és egészben kell lenyelni.
A kezelés időtartama
Kezelőorvosa megmondja, mennyi ideig kell használni a Detrusitolt. Ne hagyja abba a kezelést a vártnál hamarabb, mert nem fogja látni azonnali hatást. A húgyhólyag beállítása némi időt vesz igénybe. Fejezze be az orvosa által előírt tabletták kezelését. Ha addig nem észlelt semmilyen hatást, beszéljen orvosával.
A kezelés előnyeit 2-3 hónap elteltével újra kell értékelni.
Mindig konzultáljon orvosával, ha a kezelés abbahagyásán gondolkozik.
Ha elfelejtette bevenni a Detrusitolt
Ha elfelejtett bevenni egy adagot a szokásos időben, akkor vegye be, amint eszébe jut, kivéve, ha túl közel van a következő adaghoz. Ebben az esetben hagyja ki az elfelejtett adagot, és folytassa a szokásos ütemtervvel.
Ne vegyen be kétszeres adagot a kihagyott adag pótlására.
Ha bármilyen további kérdése van a készítmény alkalmazásával kapcsolatban, kérdezze meg kezelőorvosát vagy gyógyszerészét.
Túladagolás Mi a teendő, ha túl sok Detrusitolt vett be?
Ha Ön vagy valaki más túl sok tablettát vett be, azonnal forduljon orvosához vagy gyógyszerészéhez.
Mellékhatások Mik a Detrusitol mellékhatásai?
Mint minden gyógyszer, így a Detrusitol is okozhat mellékhatásokat, amelyek azonban nem mindenkinél jelentkeznek.
Azonnal forduljon orvosához vagy a sürgősségi osztályhoz, ha angioödéma tüneteit tapasztalja, például:
- az arc, a nyelv vagy a garat duzzanata
- nyelési nehézség
- csalánkiütés és légzési nehézség
Túlérzékenységi reakciók (pl. Viszketés, kiütés, csalánkiütés, légzési nehézség) esetén is forduljon orvosához. Ez nem ritkán fordul elő (100 betegből kevesebb mint 1 -nél fordul elő).
Forduljon orvosához, vagy azonnal menjen a sürgősségi osztályra, ha az alábbi tünetek bármelyikét észleli:
- mellkasi fájdalom, légzési nehézség vagy hajlam a könnyű fáradtságra (még nyugalomban is), éjszakai légzési nehézség, duzzanat a lábakban.
Ezek szívelégtelenség tünetei lehetnek. Ez nem ritkán fordul elő (100 betegből kevesebb mint 1 -nél fordul elő).
A következő mellékhatásokat jelentették a Detrusitol -kezelés során, a következő gyakorisággal:
Nagyon gyakori mellékhatások (10 beteg közül több mint 1 beteget érint):
- Száraz száj
- Fejfájás
Gyakori mellékhatások (10 beteg közül kevesebb mint 1 beteget érint):
- Hörghurut
- Szédülés, álmosság, bizsergő érzés a kezekben és a lábakban
- Száraz szemek, homályos látás
- Szédülés
- Palpitáció
- - emésztési nehézség (diszpepszia), székrekedés, hasi fájdalom, túlzott mennyiségű levegő vagy gáz a gyomorban vagy a belekben, hányás
- A bőr kiszáradása
- Fájdalmas vagy nehéz vizelés, a hólyag kiürítésének képtelensége
- Fáradtság, mellkasi fájdalom, túlzott testnedvek, amelyek duzzanatot okoznak (pl. Bokák)
- Súlygyarapodás
- Hasmenés
Nem gyakori mellékhatások (100 beteg közül kevesebb mint 1 beteget érint):
- Allergiás reakciók
- Idegesség
- Fokozott pulzusszám, szívelégtelenség, szabálytalan szívverés
- Hasfájás
- Memóriazavar
Egyéb jelentett reakciók közé tartoznak a súlyos allergiás reakciók, zavartság, hallucinációk, bőrpír, angioödéma és dezorientáció. Arról is beszámoltak, hogy a demencia kezelésében részesülő betegeknél súlyosbodtak a demencia tünetei.
Ha bármely mellékhatás súlyossá válik, vagy ha a betegtájékoztatóban felsorolt mellékhatásokon kívül egyéb tünetet észlel, kérjük, értesítse orvosát vagy gyógyszerészét.
Mellékhatások bejelentése
Ha Önnél bármilyen mellékhatás jelentkezik, tájékoztassa erről kezelőorvosát vagy gyógyszerészét. Ez a betegtájékoztatóban fel nem sorolt bármilyen lehetséges mellékhatásra is vonatkozik. A nemkívánatos hatások közvetlenül bejelenthetők a (z) www.agenziafarmaco.gov.it/it/responsabili címen található nemzeti bejelentési rendszeren keresztül is. A mellékhatások bejelentésével Ön is hozzájárulhat ahhoz, hogy minél több információ álljon rendelkezésre a gyógyszer biztonságosságáról.
Lejárat és megőrzés
Gyermekektől elzárva tartandó!
A csomagoláson feltüntetett lejárati idő után ne használja a Detrusitolt. A lejárati idő a hónap utolsó napjára vonatkozik.
A tárolás során nincsenek különleges óvintézkedések.
A gyógyszereket nem szabad a szennyvízzel vagy a háztartási hulladékkal együtt megsemmisíteni. Kérdezze meg gyógyszerészét, hogy mit tegyen a már nem használt gyógyszereivel. Ez segít a környezet védelmében.
Határidő "> Egyéb információ
Mit tartalmaz a Detrusitol?
A készítmény hatóanyaga a tolterodin -tartarát.
Minden Detrusitol 1 mg tabletta 1 mg tolterodin -tartarátot tartalmaz, ami 0,68 mg tolterodinnak felel meg
Minden Detrusitol 2 mg tabletta 2 mg tolterodin -tartarátot tartalmaz, ami 1,37 mg tolterodinnak felel meg
A segédanyagok a következők:
- Mag: Mikrokristályos cellulóz Kétbázisú kalcium -foszfát -dihidrát Nátrium -keményítő -glikolát (B típus) Magnézium -sztearát Szilícium -dioxid, vízmentes kolloid
- Bevonó film: hipromellóz mikrokristályos cellulóz sztearinsav titán -dioxid (E171)
Milyen a Detrusitol külleme és mit tartalmaz a csomagolás?
A Detrusitol 1 mg tabletta fehér, kerek, mindkét oldalán domború felületű, a "TO" betűk fölött és alatt bemetszéssel.
A Detrusitol 2 mg tabletta fehér, kerek, mindkét oldalán domború felületű, a "DT" betűk fölött és alatt bemetszéssel.
A Detrusitol 1 mg és 2 mg tabletta a következő kiszerelésben kapható:
Hólyagok, amelyek tartalmazzák:
- 20 tabletta (2 x 10)
- 30 tabletta (3 x 10)
- 50 tabletta (5 x 10)
- 100 tabletta (10 x 10)
- 14 tabletta (1 x 14)
- 28 tabletta (2 x 14)
- 56 tabletta (4 x 14)
- 280 tabletta
- 560 tabletta
60 vagy 500 tablettát tartalmazó palackok.
Nem feltétlenül mindegyik kiszerelés kerül kereskedelmi forgalomba.
Forrás betegtájékoztató: AIFA (Olasz Gyógyszerügynökség). A tartalom 2016 januárjában jelent meg. A jelenlévő információk nem feltétlenül naprakészek.
A legfrissebb verzióhoz való hozzáféréshez ajánlatos az AIFA (Olasz Gyógyszerügynökség) webhelyét elérni. Jogi nyilatkozat és hasznos információk.
01.0 A GYÓGYSZER MEGNEVEZÉSE -
DETRUSITOL TABLETTA FÓLIÁVAL BEVONATT
02.0 MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL -
Minden filmtabletta 1 mg tolterodin-tartarátot vagy 2 mg-ot tartalmaz, ami 0,68 mg-nak, illetve 1,37 mg tolterodinnak felel meg.
A segédanyagok teljes listáját lásd a 6.1 pontban.
03.0 GYÓGYSZERFORMA -
Filmtabletta.
A filmtabletta fehér, kerek és mindkét oldalán domború felületű.
Az 1 mg -os tablettán a TO betűk fölött és alatt bevágások vannak, a 2 mg -os tablettákon pedig a DT betűk felett és alatt.
04.0 KLINIKAI INFORMÁCIÓK -
04.1 Terápiás javallatok -
A sürgősségi inkontinencia és / vagy a fokozott vizeletürítési gyakoriság és sürgősség tüneti kezelése hiperaktív hólyag szindrómában szenvedő betegeknél.
04.2 Adagolás és alkalmazás
Felnőttek (beleértve az idős betegeket is) :
Az ajánlott adag naponta kétszer 2 mg, kivéve máj- vagy súlyos vesekárosodásban szenvedő betegeket [GFR (inulin clearance)
A kezelés hatását 2-3 hónap múlva újra kell értékelni (lásd 5.1 pont).
Gyermekgyógyászati betegek :
A Detrusitol hatásosságát gyermekeknél nem igazolták (lásd 5.1 pont), ezért a Detrusitol gyermekeknek nem ajánlott.
04.3 Ellenjavallatok -
A tolterodin ellenjavallt olyan betegeknél, akik:
- Vizelet-visszatartás
- ellenőrizetlen keskeny szögű glaukóma
- Myasthenia gravis
- Ismert túlérzékenység a tolterodinnal vagy a segédanyagokkal szemben
- Súlyos fekélyes vastagbélgyulladás
- Mérgező megakolon
04.4 Különleges figyelmeztetések és a használattal kapcsolatos óvintézkedések -
A tolterodint óvatosan kell alkalmazni olyan betegeknél, akik:
- A hólyag kiáramlásának jelentős akadálya, vizeletvisszatartás veszélyével
- Obstruktív gyomor -bélrendszeri betegségek, pl. pylorus stenosis
- A vesefunkció megváltozása (lásd 4.2 pont)
- Májbetegség (lásd 4.2 és 5.2 pont)
- Az autonóm idegrendszert érintő neuropátia
- Hiatus hernia
- A gyomor -bélrendszer motilitásának csökkenésének kockázata
Megfigyelték, hogy a napi 4 mg (terápiás) és 8 mg (szupraterápiás) azonnali hatóanyag-leadású tolterodint többszöri adagban meghosszabbítják a QTc-intervallumot (lásd 5.1 pont). Ezen adatok klinikai jelentősége nem egyértelmű, és a beteg egyéni kockázatától függ tényezők és érzékenységek A tolterodint óvatosan kell alkalmazni olyan betegeknél, akiknél fennáll a QT -megnyúlás kockázati tényezője, beleértve:
- A veleszületett vagy szerzett és dokumentált QT megnyúlása
- Elektrolit -zavarok, például hypokalaemia, hypomagnesaemia és hypocalcemia
- Bradycardia
- Már meglévő súlyos koszorúér-betegség (kardiomiopátia, szívizom ischaemia, aritmia, szívelégtelenség)
- QT -intervallumot meghosszabbító gyógyszerek, köztük az 1A. Osztályú gyógyszerek (pl. Kinidin, prokainamid) és a III. Osztály (pl. Amiodaron, szotalol), antiarritmiás szerek egyidejű alkalmazása.
A tolterodint különösen óvatosan kell alkalmazni erős CYP3A4 -gátló szedésekor (lásd 5.1 pont). Kerülni kell az erős CYP3A4 inhibitorokkal történő egyidejű kezelést (lásd 4.5 pont).
A kezelés előtti vizeletürítési tünetek vagy sürgősségi inkontinencia minden más kezeléséhez hasonlóan figyelembe kell venni a sürgősség és a gyakoriság lehetséges szerves okait.
04.5 Kölcsönhatások más gyógyszerekkel és egyéb interakciók -
A CYP2D6 gyenge metabolizálói esetében a szisztémás kezelés erős CYP3A4 inhibitorokkal, például makrolid antibiotikumokkal (pl. Eritromicin és klaritromicin), gombaellenes szerekkel (pl. Ketokonazol és itrakonazol) és proteáz inhibitorokkal egyidejűleg nem ajánlott a megnövekedett szérumkoncentráció miatt. ) túladagolás veszélye (lásd 4.4 pont).
Más, antimuszkarin tulajdonságokkal rendelkező gyógyszerekkel történő egyidejű kezelés kifejezettebb terápiás hatást és mellékhatásokat eredményezhet. Ezzel szemben a tolterodin terápiás hatása csökkenhet kolinerg muszkarinreceptor agonistákkal történő egyidejű kezelés után.
A prokinetikus gyógyszerek, például a metoklopramid és a ciszaprid hatását a tolterodin csökkentheti .
A fluoxetinnel (a CYP2D6 hatékony inhibitora) történő egyidejű kezelés nem eredményez klinikailag jelentős kölcsönhatást, mivel a tolterodin és CYP2D6-függő metabolitja, az 5-hidroxi-metil-tolterodin egyenértékűek.
A gyógyszerkölcsönhatási vizsgálatok nem mutattak kölcsönhatást a warfarinnal vagy a kombinált orális fogamzásgátlókkal (etinilösztradiol / levonorgesztrel).
Egy klinikai vizsgálat azt mutatta, hogy a tolterodin nem metabolikus inhibitora a CYP2D6, 2C19, 2C9, 3A4 vagy 1A2 enzimeknek. Ezért nem várható az ezen izoenzimeken keresztül metabolizált gyógyszerek plazmaszintjének növekedése, ha tolterodinnal kombinációban alkalmazzák.
04.6 Terhesség és szoptatás -
Terhesség
Nincsenek megfelelő adatok a tolterodin terhes nőkön történő alkalmazásáról.
Az állatokon végzett vizsgálatok reprodukciós toxicitási hatásokat mutattak (lásd 5.3 pont) A lehetséges kockázat emberekben nem ismert.
Ezért a DETRUSITOL nem ajánlott terhesség alatt.
Etetési idő
Nincs adat a tolterodin anyatejbe történő kiválasztódásáról. A tolterodin alkalmazását kerülni kell a szoptatás alatt.
04.7 Hatások a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre -
Mivel ez a gyógyszer alkalmazkodási zavart okozhat vagy befolyásolhatja a reakcióidőt, ez hátrányosan befolyásolhatja a gépjárművezetéshez és gépek kezeléséhez szükséges képességeket.
04.8 Nemkívánatos hatások -
Farmakológiai hatását tekintve a tolterodin enyhe vagy közepes súlyosságú antimuszkarin hatást okozhat, például szájszárazságot, diszpepsziát és szemszárazságot.
Az alábbi táblázat a DETRUSITOL-nal klinikai vizsgálatokban és a forgalomba hozatalt követően szerzett adatokat mutatja be. A leggyakrabban jelentett mellékhatás a szájszárazság volt, amely a DETRUSITOL tablettával kezelt betegek 35% -ánál és a placebóval kezelt betegek 10% -ánál fordult elő. szintén nagyon gyakran jelentették, a DETRUSITOL tablettával kezelt betegek 10,1% -ánál és a placebóval kezelt betegek 7,4% -ánál fordult elő.
A tolterodin -kezelés megkezdése után olyan betegeknél, akik kolinészteráz -gátlókat szednek demencia kezelésére, beszámoltak a demencia tüneteinek (pl. Zavartság, tájékozódási zavar, téveszme) romlásáról.
Gyermekgyógyászati betegek
Két randomizált, kettős vak, placebo-kontrollos fázis III gyermekgyógyászati vizsgálatban 710 gyermekbetegen 12 héten keresztül a húgyúti fertőzésben, hasmenésben és rendellenes viselkedésben szenvedő betegek aránya magasabb volt a tolterodinnal kezelt betegeknél, mint a placebóval kezelt betegeknél. (húgyúti fertőzés: tolterodin 6,8%, placebo 3,6%; hasmenés: tolterodin 3,3%, placebo 0,9%; rendellenes viselkedés: tolterodin 1,6%, placebo 0,4%(lásd 5.1 pont).
A feltételezett mellékhatások bejelentése
A gyógyszer engedélyezése után jelentkező feltételezett mellékhatások bejelentése fontos, mivel lehetővé teszi a gyógyszer előny / kockázat arányának folyamatos nyomon követését. Az egészségügyi szakembereket kérjük, hogy jelentsék be a feltételezett mellékhatásokat a nemzeti bejelentési rendszeren keresztül. "Cím: www .agenziafarmaco.gov.it/it/Responsabili.
04.9 Túladagolás -
A tolterodin-L-tartarát legmagasabb dózisa egészséges önkénteseknek egyszeri adagként 12,8 mg volt. A legsúlyosabb megfigyelt káros hatások a szállás zavarai és a vizelési nehézségek voltak.
Túladagolás esetén végezzen gyomormosást és adjon be aktív szenet.
Kezelje a tüneteket az alábbiak szerint:
* súlyos központi antikolinerg hatások (pl. hallucinációk, súlyos izgalom): fizosztigmin alkalmazása.
* Görcsök vagy kifejezett gerjesztés: benzodiazepinek beadása.
* Légzési elégtelenség: mesterséges lélegeztetést kell végezni.
* Tachycardia: adjon be β-blokkolókat.
* Vizeletvisszatartás: a katéter használata.
* Mydriasis: pilocarpine szemcseppek beadása és / vagy a beteg sötétben tartása.
A QT-intervallum növekedését figyelték meg napi egyszeri 8 mg-os azonnali hatóanyag-leadású tolterodin adaggal (a szokásos készítmény ajánlott napi adagjának kétszerese és a nyújtott hatóanyag-leadású készítmény maximális expozíciójának háromszorosa) 4 nap alatt. A tolterodin túladagolása esetén standard támogató intézkedéseket kell alkalmazni a QT -intervallum megnyúlásának kezelésére.
05.0 FARMAKOLÓGIAI TULAJDONSÁGOK -
05,1 "Farmakodinamikai tulajdonságok -
Farmakoterápiás csoport: húgyúti görcsoldók.
ATC kód: G04BD07.
A tolterodin egy specifikus versenyképes muszkarin receptor antagonista, amely in vivo szelektivitást mutat a húgyhólyagra a nyálmirigyekkel szemben. A tolterodin (5-hidroxi-metil-származék) egyik metabolitja hasonló farmakológiai profillal rendelkezik, mint az anyavegyület. Az extenzív metabolizálóknál ez a metabolit jelentősen hozzájárul a tolterodin terápiás hatásához (lásd 5.2 pont).
A kezelés hatása 4 héten belül várható.
A 2 mg Detrusitollal végzett kezelés hatása naponta kétszer, 4, illetve 12 hét után, összehasonlítva a placebóval (összesített adatok). Abszolút és százalékos változások a kiindulási értékhez képest.
n.s. = nem jelentős; * = p
A tolterodin hatásait olyan betegeknél értékelték, akiket megvizsgáltak az alapvető urodinamikai értékelés szempontjából, akik az urodinamikai tesztek eredményét követően pozitív urodinamikai (motoros sürgősség) vagy negatív urodinamikai (érzéki sürgősség) csoportba kerültek. Az egyes csoportokban a betegeket randomizálták, hogy tolterodint és placebót is kapjanak.
A tolterodin QT intervallumra gyakorolt klinikai hatásai több mint 600 kezelt beteg EKG-ján alapulnak, beleértve az idős betegeket és a már meglévő szív- és érrendszeri betegségekben szenvedő betegeket is.
A tolterodin QT-megnyúlásra gyakorolt hatását 48 egészséges, önkéntes (férfi és nő) 18-55 éves korban vizsgálták tovább. Az alanyoknak 2 mg-ot adtak licit és 4 mg licit tolterodin azonnali felszabadulású készítményben. Az eredmények (Fridericia képletével korrigálva) a maximális tolterodin -koncentrációnál (1 óra) a QTc -intervallum átlagos növekedését mutatják 5,0 és 11,8 ms -mal a 2 mg -os tolterodin adagok esetében. licit és 4 mg licit és 19,3 ms a mofloxacinhoz (400 mg), mint kontroll hatóanyag. Egy farmakokinetikai / farmakodinamikai modell azt mutatta, hogy a QTc-intervallum megnövekszik a gyenge metabolizálók (CYP2D6-mentes) kezelésében, 2 mg tolterodinnal kezelve licit hasonló a 4 mg -mal kezelt gyors metabolizálókéhoz licit. A tolterodin mindkét dózisánál egyik alany sem, metabolikus profiljától függetlenül, meghaladta az abszolút QTcF érték 500 ms -os értékét, vagy nem mutatott változásokat a kiindulási értékhez képest 60 ms -ig. Ezeket a változásokat különösen jelentős küszöbértékeknek tekintik. Az adag 4 mg licit maximális expozíciónak (Cmax) felel meg, amely háromszorosa a Detrusitol retard kapszulák legnagyobb terápiás dózisának.
Gyermekgyógyászati betegek
A hatékonyságot gyermekgyógyászati populációban nem igazolták. Két 12 hetes randomizált, kettős vak, placebo-kontrollos fázis III vizsgálatot végeztek elnyújtott hatóanyag-leadású tolterodin kapszulákkal. 710 gyermekbeteg (486 tolterodinnal és 224 placebóval kezelt) 5-10 év, fokozott vizeletürítési gyakorisággal és sürgősséggel.
Mindkét vizsgálatban nem észleltek szignifikáns változást a kiindulási értékhez képest a két csoport között az inkontinencia epizódok / hét teljes számában (lásd 4.8 pont).
05,2 "Farmakokinetikai tulajdonságok -
Az erre a készítményre jellemző farmakokinetikai jellemzők: A tolterodin gyorsan felszívódik. Mind a tolterodin, mind az 5-hidroxi-metil-metabolit eléri a maximális szérumkoncentrációt 1-3 órával a beadás után.
A tabletta formájában vett tolterodin felezési ideje 2-3 óra az extenzív metabolizálóknál és körülbelül 10 óra a gyenge metabolizálóknál (CYP2D6-mentes).
Az extenzív metabolizálóknál az élelmiszer nem befolyásolja a kötetlen tolterodin és az aktív metabolit 5-hidroxi-metil expozícióját, bár a tolterodin szintje emelkedik, ha étkezés közben veszik be.
Hasonlóképpen nem várható klinikailag jelentős változás a gyenge metabolizálókban.
Abszorpció: Orális adagolás után a tolterodin CYP2D6 által katalizált első lépcsős metabolizmuson megy keresztül a májban, ami az 5-hidroxi-metil-metabolit, egy fő farmakológiailag egyenértékű metabolit képződéséhez vezet.
A tolterodin abszolút biohasznosulása 17% az extenzív metabolizálóknál és 65% a gyenge metabolizálóknál (CYP2D6 hiány).
terjesztés: A tolterodin és az 5-hidroxi-metil-metabolit elsősorban az orosomucoidhoz kötődik. A nem kötődő frakciók 3,7%, illetve 36%. A tolterodin eloszlási térfogata 113 liter.
Kizárás: Orális adagolás után a tolterodin nagymértékben metabolizálódik a májban.
Az elsődleges metabolikus útvonalat a CYP2D6 polimorf enzim közvetíti, és az 5-hidroxi-metil-metabolit képződéséhez vezet. A további metabolizmusok 5-karbonsav és N-dealkilált 5-karbonsav metabolitok képződéséhez vezetnek, amelyek 51% -ot és A vizeletben található metabolitok 29% -a. A lakosság egy részének (kb. 7%-a) hiányos a CYP2D6 aktivitása. Ezeknél a betegeknél (gyenge anyagcsere-képességgel) azonosított anyagcsere-profil a CYP3A4 enzimeken keresztüli dealkiláció dealkilált N-tolterodinná, ami nem okoz klinikai hatásokat.
A populáció többi része gyors metabolizálókból áll. Az extenzív metabolizálóknál a tolterodin szérum szisztémás clearance -e körülbelül 30 l / óra. Gyenge metabolizálóknál a csökkent clearance jelentősen megnöveli a szérum tolterodin koncentrációját (körülbelül 7-szeresére), és az 5-hidroxi-metil-metabolit kimutathatatlan koncentrációját találjuk.
Az 5-hidroxi-metil-metabolit farmakológiailag aktív és egyenértékű a tolterodinnal szemben. A tolterodin és az 5-hidroxi-metil-metabolit fehérje-kötési jellemzőiben mutatkozó különbségek miatt a szabad tolterodin expozíciója (AUC) rossz metabolikus kapacitású betegeknél hasonló a szabad tolterodin és 5-hidroxi-metil-származék kombinációjához a CYP2D6-aktivitású betegeknél ugyanazon dózisban adva A biztonság, a tolerálhatóság és a klinikai válasz hasonló a fenotípustól.
A [14C] -tolterodin beadása után a radioaktivitás kiválasztása megközelítőleg 77% a vizeletben és 17% a székletben. A dózis kevesebb, mint 1% -a ürül változatlan formában, és körülbelül 4% -a 5-hidroxi-metil-metabolitként.
A terápiás dózistartományban a farmakokinetika lineáris.
A betegek meghatározott csoportjai
Károsodott májfunkció: Májcirrhosisban szenvedő betegeknél a szabad tolterodin és metabolitja, az 5-hidroximetil körülbelül kétszer nagyobb expozíciója tapasztalható (lásd 4.2 és 4.4 pont).
Vesekárosodás: A szabad tolterodin és metabolitja, az 5-hidroximetil átlagos expozíciója megduplázódik súlyos vesekárosodásban szenvedő betegeknél [inulin clearance (GFR)
Ezeknél a betegeknél a többi metabolit plazmaszintje jelentősen (12-szeresére) emelkedett. Ezen metabolitok fokozott expozíciójának klinikai jelentősége nem ismert, enyhe vagy közepesen súlyos vesekárosodás esetén nincs adat (lásd 4.2 és 4.4 pont).
Gyermekgyógyászati betegek
A hatóanyag expozíciója dózisonként / mg felnőtteknél és serdülőknél hasonló. A hatóanyag / dózis / mg hatóanyag átlagos expozíciója körülbelül kétszer nagyobb 5–10 éves gyermekeknél, mint felnőtteknél (lásd 4.2 és 5.1 pont)
05.3 A preklinikai biztonságossági adatok -
A toxikológiai, mutagenezis, karcinogenezis és farmakológiai biztonságossági vizsgálatok során nem észleltek klinikailag jelentős hatásokat, kivéve azokat, amelyek a gyógyszer farmakológiai hatásaival kapcsolatosak.
Szaporodási vizsgálatokat végeztek egereken és nyulakon.
Egerekben a tolterodin nem volt hatással a termékenységre vagy a reproduktív funkcióra.
A tolterodin embrionális mortalitást és magzati rendellenességeket eredményezett a plazma expozíciót követően (Cmax vagy AUC) 20 vagy 7 -szer magasabb, mint a kezelt férfiaknál. Nyulakon nem figyeltek meg malformációkra gyakorolt hatást, de vizsgálatokat végeztek olyan plazma expozíciós értékekkel (Cmax vagy AUC), amelyek 20 vagy 3 -szor magasabbak voltak, mint az embereknél a terápiás dózisok után vártak.
A tolterodin és aktív metabolitjai emberekben meghosszabbítják az akciós potenciál időtartamát (a repolarizáció 90% -a) a kutya purkinje szálaiban (a terápiás szintek 14-75-szerese), és gátolják a K + áramlását a hERG csatornákban (klónozott humán éter). a-go-go-rokon gén) (a terápiás szintek 0,5-26,1-szerese).
A kutyákon végzett vizsgálatokban a tolterodin és aktív metabolitjai embereknek történő beadását követően (a terápiás szintek 3,1-61,0 -szerese nagyobb dózisok) a QT -intervallum meghosszabbodását figyelték meg. Ennek a hatásnak a klinikai jelentősége nem ismert.
06.0 GYÓGYSZERÉSZETI INFORMÁCIÓK
06.1 Segédanyagok -
Sejtmag :
Mikrokristályos cellulóz
Kétbázisú kalcium -foszfát -dihidrát
Nátrium -keményítő -glikolát (B típus)
Magnézium-sztearát
Vízmentes kolloid szilícium -dioxid
Bevonó film :
Bevonó granulátumok, amelyek tartalmazzák:
Hipromellóz
Mikrokristályos cellulóz
Sztearinsav
Titán -dioxid (E171)
06.2 Inkompatibilitás "-
Nem releváns.
06.3 Érvényességi idő "-
3 év.
06.4 Különleges tárolási előírások -
Nincsenek különleges tárolási óvintézkedések.
06.5 A közvetlen csomagolás jellege és a csomagolás tartalma -
A tablettákat PVC / PVDC és alumínium fólia buborékcsomagolásba csomagolják PVDC hővédő bevonattal, vagy HDPE palackokba, LDPE kupakkal.
Kiszerelés: A Detrusitol tabletta 2x10, 3x10, 5x10 és 10x10 tabletta, 1x14, 2x14 és 4x14 tabletta, 280 és 560 tablettát tartalmazó buborékcsomagolásban, valamint 60 és 500 tablettát tartalmazó palackokban kapható.
Nem feltétlenül mindegyik kiszerelés kerül kereskedelmi forgalomba.
06.6 Használati és kezelési útmutató -
A fel nem használt terméket vagy hulladékot a helyi előírásoknak megfelelően kell megsemmisíteni.
07.0 A „FORGALOMBA HOZATALI ENGEDÉLY” TULAJDONOSA -
Pfizer Italia S.r.l.
Via Isonzo, 71 - 04100 Latina
08.0 A FORGALOMBA HOZATALI ENGEDÉLY SZÁMA -
DETRUSITOL 1 mg filmtabletta - 28 tabletta, AIC n. 034168017
DETRUSITOL 2 mg filmtabletta - 28 tabletta, AIC n. 034168029
09.0 AZ ELSŐ ENGEDÉLYZÉS ÉS A JÓVÁHAGYÁS MEGÚJÍTÁSÁNAK DÁTUMA -
1999. január 12. és 2006. március 23.